

Original Article - Year 2011 - Volume 26 -
Reconstrução mamária com expansor definitivo: enfoque diferenciado
Breast reconstruction with permanent expander: a differentiated approach
RESUMO
Introdução: As reconstruções de mama imediatas ou tardias com uso de expansores podem ocorrer em um ou mais de um tempo cirúrgico. Optou-se por reconstruções em mais de um tempo cirúrgico, com expansores definitivos tipo Becker. Este estudo teve como objetivo demonstrar a utilização da técnica de reconstrução mamária com expansor definitivo tipo Becker, com retalho dos músculos peitoral maior e menor, serrátil anterior e aponeurose do músculo reto abdominal para cobertura completa do expansor. Métodos: Estudo retrospectivo, por meio de análise de prontuário, incluindo 21 pacientes submetidas a reconstrução mamária com expansor permanente. Resultados: Na confecção do retalho muscular, é necessária a realização de dissecção abaixo do sulco submamário definido no pré-operatório, com o propósito de cobertura total do material aloplástico usado na reconstrução, englobando a aponeurose do músculo reto abdominal, 6 cm a 8 cm abaixo do sulco submamário, evitando-se lesão de sua continuidade com o músculo peitoral maior. Neste estudo, duas pacientes apresentaram infecção, uma delas na primeira semana de pós-operatório e a outra, no terceiro mês. Conclusões: A utilização do retalho dos músculos peitoral maior e menor, serrátil anterior e bainha do músculo reto abdominal é uma boa opção nas reconstruções mamárias com utilização de expansor definitivo de tecidos, visto que promove proteção adequada ao expansor e aos retalhos cutâneos que se posicionam sobre ele. Além disso, a técnica permite expansão tecidual, sem que os expansores fiquem encarcerados ou presos à loja muscular.
Palavras-chave: Neoplasias da mama. Mastectomia. Mamoplastia. Dispositivos para expansão de tecidos.
ABSTRACT
Background: Immediate or delayed breast reconstruction with tissue expanders can be performed in one or several surgical sessions. We opted to perform breast reconstruction over several sessions. The aim of this study was to report our experiences with the breast reconstruction technique involving Becker permanent tissue expanders and complete expander coverage with a flap comprising the pectoralis major, pectoralis minor, serratus anterior, and rectus abdominis aponeurosis. Methods: The medical records of 21 patients who underwent postmastectomy breast reconstruction with Becker permanent tissue expanders were retrospectively analyzed. Results: During muscle flap preparation, the aponeurotic dissection was performed 6-8 cm below the inframammary crease, aiming at full expander coverage without tension, enabling lower suturing in the inframammary crease, and avoiding disruption of the pectoralis major attachments. Only two patients developed infection, one in the first postoperative week and the other in the third postoperative month. Conclusions: The flap comprising the pectoralis major, pectoralis minor, serratus anterior, and rectus abdominis aponeurosis is a good choice for breast reconstruction with permanent tissue expanders because it ensures adequate expander and skin-flap protection. Moreover, the technique enables tissue expansion without confining the expanders in the submuscular cavity.
Keywords: Breast neoplasms. Mastectomy. Mammaplasty. Tissue expansion devices.
De acordo com o Instituto Nacional do Câncer1, o termo câncer é utilizado para denominar doenças que apresentam crescimento das células de forma desordenada, que invadem tecidos e/ou órgãos, podendo ser considerado maligno ou benigno conforme a agressividade da invasão. Esse fato leva as pessoas a terem receio de verbalizar o termo, que há muito tempo é sinônimo de dor, sofrimento, vergonha e morte. Segundo Sant'Anna2, quando o termo é utilizado para câncer de mama esses sentimentos ficam mais expressivos, pois a mama é considerada símbolo da identidade feminina.
O câncer de mama, segundo Menke et al.3, é a neoplasia maligna com maior incidência entre as mulheres, representando 20% dos tumores femininos e responsável por 15% das mortes por tumores em mulheres. No mundo, é considerado problema de saúde pública, com estimativa de cinco milhões de casos novos dentro do período de cinco anos. De acordo com dados do Instituto Nacional de Câncer4, as taxas de mortalidade no Brasil apresentam-se elevadas em decorrência do diagnóstico tardio. Mundialmente, esse é o câncer mais comum em mulheres, representando 22% dos casos novos a cada ano, com sobrevida média após cinco anos de 61%. No mundo, segundo a Organização Mundial da Saúde (OMS), a estimativa de novos casos para 2010 era de 49.240 casos. Em 2008, ocorreram 11.860 mortes por esse tipo de câncer, a quase totalidade (11.735 casos) em mulheres.
No Brasil, em 2010 esperava-se a ocorrência de 9.240 casos novos de câncer de mama no sexo feminino, com risco estimado de 49 casos a cada 100 mil mulheres. No Sul do Brasil, o risco estimado era de 64 casos novos para 100 mil mulheres, um dos maiores do País. No Rio Grande do Sul, a estimativa era de 4.750 casos novos em 2010 e em Porto Alegre, capital do Estado, estimava-se a incidência de 1.040 novos casos do câncer de mama em mulheres.
O câncer de mama é a segunda causa de mortalidade entre as mulheres no Brasil, em decorrência do diagnóstico tardio da doença, fato observado com maior frequência nos países em desenvolvimento e subdesenvolvidos. Nos países desenvolvidos, observa-se aumento da incidência do câncer de mama, mas redução da mortalidade, resultado da detecção precoce da doença1.
O câncer de mama é considerado uma doença multifatorial, pois fatores genéticos e ambientais estão relacionados a seu aparecimento. O processo é complexo, sendo dividido em iniciação, promoção e progressão. A iniciação é uma etapa do processo da carcinogênese mamária, em que os eventos genéticos são desencadeados por fatores carcinogênicos e os oncogenes ativados promovem estímulo e proliferação anormal das células. Os genes supressores tumorais inibem a divisão celular, reparando os defeitos do ácido desoxirribonucleico (DNA). Os genes BRCA1 e 2 produzem proteínas necessárias à reparação do DNA defeituoso. Caso haja alterações nesses genes, ocorre instabilidade cromossômica e incapacidade de reparação dos erros celulares no tecido mamário. A promoção é um evento iniciador genético, estimulado por hormônios esteroides, reações inflamatórias e fatores de crescimento. Na fase de progressão, o tumor já está estabelecido e há influência em sua capacidade de invasão tecidual e de metastização3.
As pacientes em estádio inicial do câncer de mama têm como opção de tratamento a quadrantectomia ou mastectomia radical modificada, podendo ser acompanhada da técnica de remoção do linfonodo sentinela, quando o tumor tiver < 3 cm de diâmetro. Para a retirada do linfonodo sentinela, não pode haver comprometimento clínico nodular, para que, no transoperatório e na identificação e retirada do linfonodo sentinela, a partir de exame de congelação transoperatório, se possa definir a necessidade ou não de retirada de todas as cadeias dos linfonodos axilares, procedimento denominado de esvaziamento axilar1.
O tratamento de escolha para o câncer de mama é a cirurgia. A mastectomia radical clássica foi introduzida por William Halsted, em 1894, tornando-se um marco no tratamento do câncer de mama3. Na atualidade, para os estádios iniciais do câncer de mama, as cirurgias conservadoras, como as quadrantectomias com pesquisa de linfonodo sentinela, são procedimentos de eleição; nos casos mais avançados, mastectomia radical modificada, com preservação dos músculos peitorais e pesquisa do linfonodo sentinela, com ou sem necessidade de esvaziamento axilar ganglionar, é o procedimento mais indicado para o tratamento.
Após a quadrantectomia e a mastectomia, a mulher tem a opção de reconstruir sua mama amputada por meio de cirurgia plástica reparadora, com inserção de implante de silicone ou de solução salina, expansores de tecidos temporários ou definitivos, por meio de um retalho de músculo reto abdominal ou grande dorsal ou retalhos musculares microcirúrgicos5.
Com o aumento da incidência de câncer de mama, mais casos de mastectomia serão realizados, e maior número de pacientes buscará o tratamento de reconstrução da mama pelo especialista. O cirurgião plástico deverá estar preparado para enfrentar essa enfermidade e, com seus conhecimentos e habilidades técnicas, contribuir sobremaneira com o tratamento dessas pacientes. Importante ressaltar que as pacientes submetidas a reconstrução de mama apresentam melhor recuperação do ponto de vista oncológico, resgatando sua autoestima e enfrentando o tratamento adjuvante de sua doença, como quimioterapia e radioterapia, mais estimuladas e confiantes.
A reconstrução mamária pode ser realizada de forma imediata ou tardia, de acordo com a preferência do profissional ou serviço que realiza o procedimento, bem como por escolha da paciente. A opção pela reconstrução primária ou imediata justifica-se pelo auxílio do mastologista no ato operatório, verificando-se melhor planejamento dos tecidos disponíveis para a reconstrução, pela observância da vitalidade desses tecidos e pela preservação de maior quantidade de pele e músculos. Além disso, a reconstrução é mais rápida, pois os tecidos já estão disponíveis no transoperatório da mastectomia, não sendo necessária a espera de seis meses a um ano para que se possa reconstruir a deformidade da mama6.
Os que advogam a reconstrução tardia justificam sua posição por se tratar de procedimento que será efetuado em momento posterior, evitando-se hematomas, infecção, sangramentos e perdas de retalhos musculares que estão incluídos no procedimento da mastectomia. Defendem, também, que há possibilidade de realização de radioterapia pós-operatória, não indicada inicialmente pelo mastologista, mas que após resultado do exame anatomopatológico pode ter sua indicação revista, aumentando o risco de complicações nos retalhos empregados na reconstrução mamária. A cirurgia tardia é tecnicamente mais fácil, com menor dissecção de tecidos, com retalhos cutâneos mais confiáveis e menor área de espaço "morto". Na reconstrução tardia, a mastectomia e a vitalidade dos retalhos cutâneos locais já estão determinadas e, em casos de realização de radioterapia, os tecidos alterados por esse procedimento são removidos, podendo ser substituídos por tecidos autólogos, ao invés de se procurar reparar uma reconstrução protética irradiada imediata6.
As reconstruções de mama imediatas ou tardias com uso de expansores podem ocorrer em um ou mais de um tempo cirúrgico. No nosso Serviço, optou-se por reconstruções em mais de um tempo, pela possibilidade de adaptação mais adequada entre a mama reconstruída e a mama contralateral. Nos casos em que há necessidade de reconstrução do complexo areolomamilar, esse tempo é usado para adequar volume, tamanho e formato das mamas, aumentando ou não o expansor mamário da mama reconstruída, reposicionando o sulco submamário, caso seja necessário, e permitindo, também, que a mama contralateral sofra refinamentos.
Em nossa prática, utilizamos o expansor definitivo ajustável nas reconstruções mamárias, pela possibilidade de se operar as pacientes juntamente com o mastologista, possibilitando avaliação pré-operatória adequada e discussão com as pacientes sobre a melhor forma de reconstrução e sobre a necessidade de radioterapia posteriormente ao procedimento cirúrgico, por se tratar de uma técnica de execução dinâmica, sem a necessidade da utilização de tecidos de outras regiões, como é o caso dos retalhos dos músculos grande dorsal e reto abdominal.
Os fenômenos tromboembólicos aumentam sobremaneira em procedimentos anestésico-cirúrgicos de longa duração; além disso, os riscos de infecção aumentam após quatro horas de cirurgia, colocando em xeque os implantes mamários utilizados para as reconstruções mamárias6. Entrosamento da equipe médica, adequado planejamento pré-operatório e sequência cirúrgica obedecendo à programação tornam a cirurgia de mastectomia e reconstrução mamária imediata rápida, evitando-se surpresas transoperatórias, que poderiam prolongar a cirurgia e, assim, aumentar os riscos inerentes ao procedimento.
A reconstrução mamária imediata traz benefícios, uma vez que as pacientes não se sentem mutiladas, têm a unidade glandular mamária reconstruída, retornam ao convívio social rapidamente e retomam a identidade corporal prévia à cirurgia.
Os implantes mamários surgiram na década de 1960, com diversidade de tamanhos e formas, sendo redondos, anatômicos, de polo inferior e perfis alto, baixo, médio ou superalto. Os implantes mamários disponíveis no mercado brasileiro para reconstrução são: próteses de silicone, que apresentam superfície externa lisa, texturizada ou com espuma de poliuretano e preenchimento interno com gel de silicone; expansores de tecidos, que podem ter superfície lisa ou texturizada, com interior vazio para ser preenchido com solução salina, através de válvula remota ou externa; e expansores definitivos de Becker, de duplo lúmen, que têm superfície externa texturizada, contendo gel de silicone na proporção de 35% a 50% do volume do expansor na camada anterior e loja posterior vazia, a ser preenchida na proporção de 50% a 65% com solução salina por meio de válvula externa7.
Os materiais aloplásticos usados para reconstrução mamária, como os expansores de tecidos e os implantes mamários de silicone, apresentam complicações inerentes a sua utilização, dentre elas: infecção, cujo índice, em nosso meio, varia de 1% a 10%; e contratura capsular, com incidência entre 2% e 5%, reportada por estudos, com graus 3 a 4 de Baker, sendo a complicação mais comum associada aos implantes mamários a longo prazo6. As contraturas capsulares dividem-se em graus: Baker grau 1, mama com consistência macia e o implante mamário não é palpável; Baker grau 2, cápsula levemente palpável; Baker grau 3, implante não visível e com endurecimento palpável; e Baker grau 4, mesmas características do grau 3 associadas a dor. Outra complicação possível com o emprego de materiais aloplásticos usados para reconstrução mamária é o esvaziamento do expansor definitivo, por problemas relacionados às válvulas de retenção do volume expandido de solução salina, levando à diminuição da projeção de tecido mamário reconstruído.
O endurecimento mamário em implantes de reconstrução ocorre em 30% a 35% das pacientes, no período de dois anos de pós-operatório. Os fatores que podem contribuir para o aparecimento de contratura capsular são infecções subclínicas, hematomas não drenados, seromas e contaminação da área operada6.
A técnica de reconstrução mamária com a utilização de expansores foi introduzida, em 1980, por Radovan, e aperfeiçoada por Argenta. A cobertura dos expansores dependia de retalhos musculares ou miocutâneos, pois as cirurgias eram agressivas, com ressecções cutâneas extensas, culminando com a falta de pele para o fechamento dos tecidos. Os expansores utilizados à época eram lisos, sendo indicados em todas as pacientes que possuíam boa extensão de pele e tecidos moles. O método de escolha é a loja submuscular, com dissecção e divisão do músculo peitoral maior paralelo à orientação de suas fibras musculares, na altura da quarta ou da quinta costelas. A dissecção superior é facilitada, enquanto a dissecção inferior e lateral do retalho é dificultada, uma vez que as bases anatômicas são imprecisas. A dissecção inferior deve ser realizada 2 cm abaixo do sulco submamário original, haja vista que, durante a expansão, o expansor tende a se elevar. As fibras musculares próximas ao esterno devem ser preservadas, evitando-se que o expansor possa migrar para a porção medial. Após a confecção da loja muscular, coloca-se o expansor, que é total ou parcialmente coberto. Os expansores com superfície texturizada permitem melhor aderência aos tecidos circunjacentes, evitando sua migração ou rotação. O volume do expansor é determinado como base na mama contralateral. O expansor é colocado vazio no plano submuscular e, após fechamento muscular, é inflado com 100 ml a 200 ml de solução salina, respeitando-se a expansibilidade dos tecidos8. A abordagem com incisão oblíqua do músculo peitoral maior de acordo com a orientação de suas fibras musculares, seguida da confecção da bolsa muscular, é defendida por Guimarães et al.9, com resultados satisfatórios e complicações comparáveis à experiência reportada na literatura mundial.
As opções de instalação do expansor incluem o posicionamento apenas abaixo do músculo peitoral maior, menor e serrátil anterior, e a cobertura muscular total, incluindo esses músculos e a bainha do músculo reto abdominal. Essa técnica apresenta, como efeito indesejável, achatamento do polo inferior da mama reconstruída8. Quando os retalhos musculares não estão disponíveis, a cobertura da porção inferior do expansor pode ser realizada com material bioprotético no subcutâneo, como AlloDerm10. Trata-se de uma matriz dérmica acelular de pele de cadáveres esterilizada, em que houve remoção dos componentes antigênicos, mantendo-se colágeno, elastina, ácido hialurônico, fibronectina, proteoglicanos e canais vasculares. Essa matriz integra-se ao tecido receptor, protegendo a parte inferior do expansor11.
No Brasil, a Agência Nacional de Vigilância Sanitária (Anvisa) não permite a comercialização do produto, inviabilizando sua utilização em nosso meio. Dessa forma, a reconstrução mamária é feita com a utilização de expansor definitivo tipo Becker, com cobertura muscular completa, utilizando os músculos peitoral maior, menor, serrátil anterior e a aponeurose anterior do músculo reto abdominal.
Nesse contexto, este trabalho teve por objetivo demonstrar a experiência de nosso Serviço com a técnica de reconstrução mamária com expansor definitivo tipo Becker, discutindo detalhes técnicos e potenciais complicações inerentes ao procedimento.
MÉTODO
Foi realizado um estudo retrospectivo, por meio de análise de prontuário, das reconstruções mamárias pós-mastectomia, realizadas em nosso Serviço, no período de janeiro de 2008 a junho de 2010. Foram estudadas 21 pacientes submetidas a reconstrução mamária com expansor permanente. As pacientes candidatas a reconstrução mamária foram encaminhadas pelo Serviço de Mastologia do hospital, apresentando diagnóstico anatomopatológico da doença e planejamento do tipo de tratamento para o tumor mamário ou para cirurgia redutora de risco em pacientes com indicação (BRCA1 ou 2 positivos).
Na consulta pré-operatória, as pacientes foram orientadas quanto a procedimento de reconstrução, material a ser utilizado, necessidade dos tempos cirúrgicos, cicatrizes, dor e possíveis complicações, bem como limitação dos resultados. Foram realizados exames pré-operatórios, de acordo com a faixa etária e a presença de comorbidades, além de definição dos volumes do expansor e, quando necessária, simetrização da mama contralateral, e consulta pré-anestésica, seguidas de preenchimento e assinatura, pela paciente, do Termo de Consentimento Cirúrgico Pós-Informado.
Em nosso Serviço, para a reconstrução mamária, foram utilizados expansores de duplo lúmen, do tipo Siltex® Contour Profile Becker 50, redondos, Mentor®. Esses expansores possuem cobertura de gel de silicone em sua porção anterior de 50%, e câmara interna posterior para ser preenchida com solução salina através de válvula remota. Os volumes totais de solução salina a serem infundidos foram determinados com base no volume total do expansor, no tamanho proposto a ser atingido, e no volume da mama contralateral, com possibilidade de expansão de até 20% a mais do volume predeterminado pela fábrica. Na mama contralateral, foram utilizadas próteses mamárias e realizadas mamoplastias redutoras com implantes mamários ou mamopexias, de acordo com a necessidade.
Os critérios de inclusão para a realização da reconstrução de mama com expansor definitivo foram: pacientes submetidas ou com indicação de realização de mastectomia radical modificada por carcinoma de mama, e pacientes com risco elevado para o desenvolvimento de câncer de mama, com indicação de adenomastectomia profilática.
Os critérios de exclusão considerados neste estudo foram: discordância da paciente com a realização da reconstrução mamária, presença de comorbidades com contraindicação clínica ou cardiológica para realização do procedimento, e demonstração pelas pacientes de expectativa de resultado inatingível com o procedimento, durante a avaliação pré-operatória.
Técnica Operatória
Foi realizada mastectomia radical modificada ou adenomastectomia profilática em um tempo cirúrgico, optando-se pela incisão em T invertido ou vertical de acordo com a cicatriz que seria usada na simetrização contralateral.
A anestesia aplicada às pacientes foi geral, em todos os casos. O mastologista, juntamente com o cirurgião plástico, protegeu os retalhos resultantes da mastectomia, evitando-se possíveis sofrimentos cutâneos. Não foram usados afastadores de mama, sendo respeitadas as espessuras de 0,5 cm a 1 cm dos retalhos cutâneos, preservando-se a vascularização dérmica da pele. Os retalhos empregados foram dos músculos peitoral maior, menor, serrátil anterior e da aponeurose anterior do músculo reto abdominal. Esta última foi dissecada aproximadamente 6 cm a 8 cm abaixo do sulco submamário, tornando o retalho mais longo e possibilitando sutura inferior sem tensão no sulco submamário do retalho. Essa manobra evita que a dissecção da região retromuscular do peitoral maior seja realizada muito superiormente, garantindo a disponibilidade de tecido inferior suficiente para cobertura do material aloplástico (Figura 1).
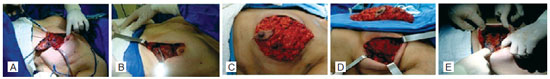
Figura 1 - Em A, ressecção da mama com o complexo areolomamilar. Em B, preservação do músculo integro. Em C, demarcação dos músculos peitoral maior, menor, serrátil anterior e bainha do reto abdominal. Em D, retalho muscular dissecado e rebatido amplamente. Em E, expansor totalmente coberto e saída da mangueira de expansão.
O expansor foi colocado totalmente no plano submuscular, procedendo-se à sutura da aponeurose anterior do músculo reto abdominal ao local do sulco submamário predeterminado, obtendo-se adequado contorno do polo inferior da mama reconstruída e proteção do expansor mamário. Em seguida, a válvula remota foi conectada à mangueira do expansor, fixando-se a união com os conectores que acompanham o produto, colocando-se a válvula lateral e inferiormente ao expansor, evitando-se, assim, que o expansor pudesse ser atingido nas sessões de expansão, por punção externa do dômus (Figura 2).
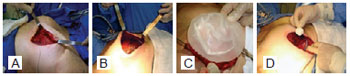
Figura 2 - Em A, colocação do expansor vazio na loja muscular. Em B, expansor coberto pelo retalho muscular íntegro. Em C, expansor coberto pelo retalho muscular e drenagem por dreno tubular. Em D, conexão da válvula remota lateral e inferiormente ao sulco submamário.
O expansor definitivo não foi expandido inicialmente, evitando-se tensões teciduais. Foi realizado teste do conjunto da válvula externa ligada ao expansor com o intuito de avaliar se o sistema estava funcionando adequadamente, sendo injetada solução salina com azul de metileno, resultando em tom azul claro. Essa tática auxiliou nas punções posteriores para a expansão, pois quando a válvula foi puncionada houve refluxo de solução salina com azul de metileno, confirmando o local correto para a infusão dos líquidos. O retalho muscular, em sua porção lateral, foi suturado, unindo-se o músculo peitoral maior ao menor, com fio absorvível de monocryl 2-0. A porção inferior do retalho, correspondendo ao músculo serrátil anterior e a aponeurose do reto abdominal, foi suturada ao periósteo dos arcos costais, com o propósito de definição do sulco submamário, com fio de monocryl 2-0. A pele dos retalhos cutâneos foi fechada em dois planos de monocryl 2-0 e 3-0.
A loja do expansor mamário foi drenada com dreno de sucção em sistema fechado tipo Porto Vac. O dreno foi mantido até que a saída de líquidos fosse inferior a 15 ml. Os curativos foram realizados com micropores sobre as incisões e no dreno tubular, colocando-se gazes e sutiã na cobertura das mamas (Figura 3).
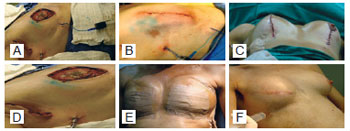
Figura 3 - Em A, punção da válvula e injeção de azul de metileno com solução salina. Em B, aspecto da incisão cutânea suturada, do linfonodo sentinela e do dreno tubular. Em C, aspecto final das incisões cutâneas e sulco submamário com dreno tubular. Em D, colocação do dreno tubular na linha axilar anterior lateralmente. Em E, aplicação de micropore nas mamas e no dreno tubular. Em F, expansão tecidual.
Foi realizada profilaxia para tromboembolismo pulmonar, com colocação de meias elásticas Kendall Ted®, compressores pneumáticos intermitentes nos membros inferiores, deambulação precoce no mesmo dia do ato operatório e administração de heparina de baixo peso molecular, iniciada seis horas após o término do procedimento cirúrgico.
As sessões de expansão foram iniciadas na segunda semana de pós-operatório, até obtenção do volume total programado, de acordo com a mama contralateral e os anseios da paciente.
Casos Selecionados
Foram selecionados alguns casos clínicos para ilustrar os resultados obtidos com a técnica, descritos a seguir.
Paciente 3 - Mulher com 35 anos de idade, portadora de câncer de mama direita, foi submetida a mastectomia radical modificada, com reconstrução mamária e simetrização contralateral imediata em outro Serviço. Teve perda do expansor na mama direita e ptose na mama contralateral. Um ano após a primeira cirurgia, procurou nosso Serviço para reparação. Realizada reconstrução em mama direita com expansor de Becker e, no segundo tempo, adenomastectomia esquerda e reconstrução mamária com expansor de Becker. A cirurgia de adenomastectomia foi indicada pelo médico oncologista, visto que a paciente apresentava fatores prognósticos para câncer triplo-negativo. No terceiro tempo, as válvulas dos expansores foram retiradas e foi feita a reconstrução do complexo areolomamilar direito (Figuras 4 a 6).
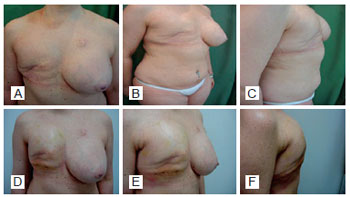
Figura 4 - Paciente 3. Primeira consulta no Serviço e primeiro tempo cirúrgico com expansor definitivo em mama direita: expansão parcial.
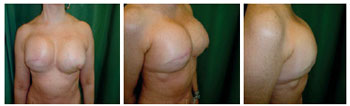
Figura 5 - Paciente 3. Segundo tempo cirúrgico: expansor definitivo totalmente expandido na mama direita e adenomastectomia profilática esquerda com expansor definitivo totalmente expandido.
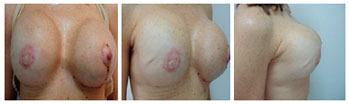
Figura 6 - Paciente 3. Terceiro tempo cirúrgico: retirada das válvulas de expansão e reconstrução do complexo areolomamilar esquerdo e direito.
Paciente 9 - Mulher com 38 anos de idade, portadora de câncer de mama bilateral, foi submetida a mastectomia radical modificada bilateral e reconstrução imediata com expansor definitivo (Figuras 7 e 8).
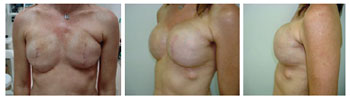
Figura 7 - Paciente 9. Expansor bilateral em fase de expansão.
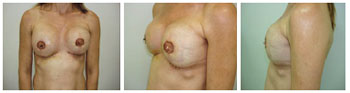
Figura 8 - Paciente 9. Reconstrução do complexo areolomamilar esquerdo e direito.
Paciente 12 - Mulher de 29 anos de idade, portadora de carcinoma lobular de mama direita, foi submetida a reconstrução mamária tardia e simetrização da mama esquerda (Figuras 9 a 12).
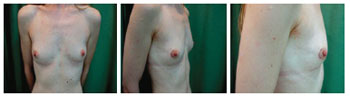
Figura 9 - Paciente 12. Pré-operatório: aspecto da mama sem cirurgia.
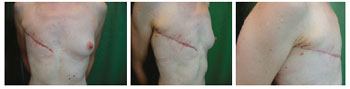
Figura 10 - Paciente 12. Aspecto da mastectomia realizada em outro Serviço.
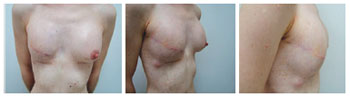
Figura 11 - Paciente 12. Primeiro tempo de reconstrução mamária: expansor definitivo na mama direita expandido e simetrização mamária contralateral com prótese de silicone.
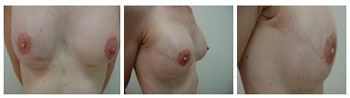
Figura 12 - Paciente 12. Segundo tempo de reconstrução mamária: reconstrução do complexo areolomamilar direito, retirada da válvula do expansor e reposicionamento do complexo areolomamilar esquerdo.
Paciente 19 - Mulher de 42 anos de idade, sem diagnóstico de câncer de mama, com biopsia revelando células atípicas, com histórico de mãe que faleceu por metástases de câncer de mama. Realizada adenomastectomia profilática bilateral, com reconstrução mamária imediata com expansores definitivos (Figuras 13 a 16).
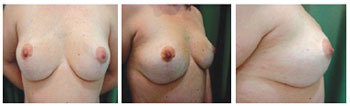
Figura 13 - Paciente 13. Aspecto pré-operatório de adenomastectomia profilática.
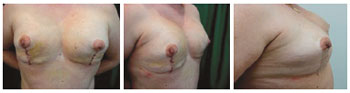
Figura 14 - Paciente 13. Primeiro tempo cirúrgico de adenomastectomia bilateral com reconstrução imediata com expansores definitivos bilaterais: expansão parcial.
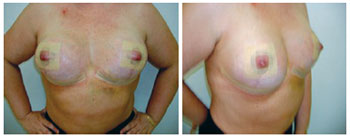
Figura 15 - Paciente 13. Segundo tempo cirúrgico com expansão total e retirada das válvulas dos expansores. Pós-operatório de um mês.
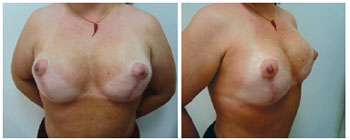
Figura 16 - Paciente 13. Pós-operatório de seis meses.
RESULTADOS
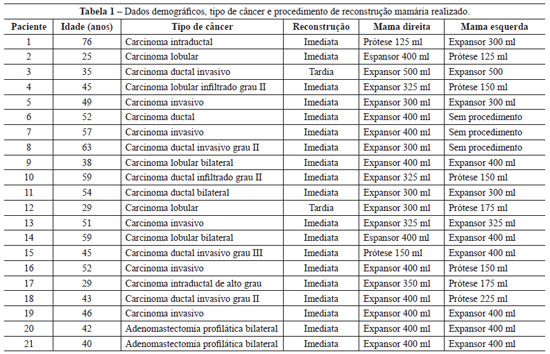
A Tabela 1 sintetiza os dados demográficos e relativos ao tipo de câncer e ao procedimento de reconstrução mamária empregado no estudo.
As 21 pacientes operadas apresentavam idade entre 25 e 76 anos, 7 delas entre 50 e 59 anos, 7 entre 40 e 49 anos, 5 com idade inferior a 40 anos, e apenas 2 com idade superior a 60 anos.
Em relação ao tipo de câncer que essas mulheres desenvolveram, 7 delas apresentavam carcinoma ductal invasivo; 5, carcinoma lobular; outras 5, carcinoma invasivo; 2, carcinoma intraductal; e 2 pacientes não tiveram diagnóstico de câncer, mas realizaram adenomastectomia profilática por apresentarem alto risco para desenvolvimento de câncer de mama, por história familiar e pesquisa genética.
Reconstrução mamária com utilização de expansor definitivo foi realizada imediatamente após a mastectomia em 19 pacientes, e de forma tardia em apenas 2. Simetrização da mama contralateral não foi realizada em 3 casos, por opção das pacientes; em 3 pacientes submetidas a mastectomia bilateral; e em 2 pacientes submetidas a adenomastectomia profilática.
Os expansores foram utilizados para reconstrução da mama submetida a mastectomia e também para a simetrização mamária contralateral, conforme indicação do cirurgião. O volume dos expansores variou de 300 ml a 400 ml e das próteses utilizadas para a simetrização, de 150 ml a 225 ml.
Nas pacientes incluídas neste estudo, foram observados dois casos de infecção, sendo um deles na primeira semana de pós-operatório e o outro, no terceiro mês de pós-operatório, coincidindo com a segunda sessão de quimioterapia. A paciente que apresentou infecção local tardia estava assintomática e a infecção foi atribuída a queda da imunidade humoral secundária à quimioterapia. Em ambos os casos, os expansores foram retirados e as pacientes foram tratadas com antibioticoterapia endovenosa, com cura do processo infeccioso. Uma paciente, de 59 anos de idade, portadora de câncer de mama bilateral, apresentou deiscência da cobertura cutânea na cicatriz vertical, com exposição do expansor. A paciente foi tratada com retalho torácico de rotação, que possibilitou cobertura da área exposta e boa evolução, sem sinais de infecção e sem prejuízo à reconstrução (Figuras 17 a 19). Duas pacientes apresentaram seromas com culturas negativas, tratados com aspiração local e infiltração de corticosteroides após a evacuação do seroma localmente.
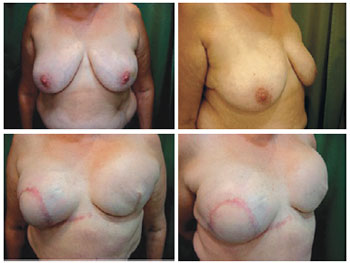
Figura 17 - Paciente 14. Aspecto pré-operatório. Retalho cutâneo torácico de rotação para cobertura da área de exposição cutânea.
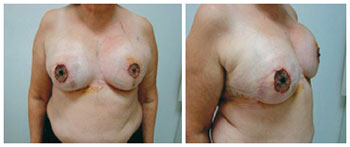
Figura 18 - Paciente 14. Reconstrução do complexo areolomamilar esquerdo e direito, adequação dos volumes mamários e retirada das válvulas.
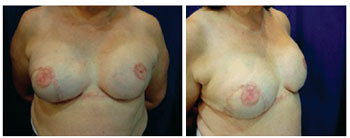
Figura 19 - Paciente 14. Aspecto final da reconstrução.
DISCUSSÃO
Na confecção do retalho muscular, é necessária a dissecção abaixo do sulco submamário definido no pré-operatório, com o propósito da cobertura total do material aloplástico usado na reconstrução, englobando a aponeurose do músculo reto abdominal, 6 cm a 8 cm abaixo do sulco submamário, evitando-se lesão de sua continuidade com o músculo peitoral maior.
Em nosso meio não dispomos de materiais bioprotéticos, como o AlloDerm®, para cobertura do expansor em sua porção inferior, como reportado por alguns autores8,12,13. Além de ser um produto sem autorização da Anvisa para comercialização e emprego no País, é um produto caro e não composto de tecidos autólogos, como a bainha aponeurótica do músculo reto abdominal, que apresenta menor índice de complicações e custos operacionais diminuídos.
Observou-se que a cobertura total proporciona maior segurança à proteção do expansor, pois em caso de eventual deiscência da sutura dos retalhos ou mesmo de necrose cutânea não ocorrerá exposição do expansor, que estará em um compartimento fechado com a bolsa muscular, evitando infecção, contaminação e perda.
O descolamento menor da região superior do músculo peitoral maior justifica-se pela grande quantidade de tecidos inferiores, que cobrem o expansor adequadamente e por completo. Dessa forma, no momento da expansão que se realiza no pós-operatório, não ocorre migração lateral, medial ou superior do expansor, que é expandindo no local colocado, sem necessidade de curativos com faixas na região torácica alta para forçar o expansor a migrar para a porção torácica inferior.
Nas dissecções ao longo do músculo peitoral maior, ao se cortar o músculo suas fibras musculares se enfraquecem e se desvascularizam, proporcionando maior possibilidade de deiscência de sutura. Com a abordagem transmuscular, descolamento da região inferior torácica e posicionamento do sulco mamário inferior são dificultados, diferentemente das situações em que se aborda, no sulco submamário, a dissecção dos retalhos, englobando maior quantidade de tecidos, sutura inferior na demarcação prévia do sulco submamário e visualização direta do sulco.
Com o presente estudo, evidencia-se que a reconstrução de mama com expansores definitivos14 é uma boa opção no arsenal das técnicas existentes, de fácil aprendizado, execução simples, baixos índices de morbidade e complicações, com bons resultados alcançados, além de evitar as mutilações resultantes das cirurgias de mastectomia. Em nossa prática, nas 21 mulheres atendidas a técnica mostrou-se adequada e com bons resultados, e as complicações observadas são inerentes a qualquer reconstrução mamária pós-mastectomia.
Outros estudos devem ser realizados com a intenção de aperfeiçoar cada vez mais as técnicas de reconstrução mamária pós-mastectomia por câncer de mama.
CONCLUSÃO
A utilização do retalho dos músculos peitoral maior, menor, serrátil anterior e bainha do músculo reto abdominal é uma boa opção nas reconstruções mamárias com a utilização de expansor definitivo de tecidos. A técnica promove adequada proteção ao expansor e aos retalhos cutâneos que se posicionam sobre ele, permitindo que os expansores sejam expandidos sem que fiquem encarcerados e presos à loja muscular. Com essa técnica, o sulco submamário é refeito, com sutura do retalho ao periósteo costal, o que garante uma forma natural à mama reconstruída. No período de expansão, não ocorre migração do expansor para as regiões lateral ou superior, o que prejudicaria o resultado final da reconstrução. Essa é uma técnica de fácil execução, que não necessita de materiais aloplásticos ou especiais, além de permitir a visualização direta no momento do teste do funcionamento da válvula remota na expansão, identificando eventuais escapes de líquidos ou obstruções no sistema da válvula ligada ao expansor.
REFERÊNCIAS
1. Instituto Nacional do Câncer. Controle do câncer de mama: documento de consenso. Rio de Janeiro: Instituto Nacional do Câncer; 2004. Disponível em: http://www.inca.gov.br/publicacoes/Consensointegra.pdf Acesso em: 10/10/2006.
2. Sant'Ana DBA. Mulher e o câncer na história. In: Gimenes MGG, Fávero MH, eds. A mulher e o câncer. Campinas: Livro Pleno; 2000. p.43-70.
3. Menke CH, Biazús JV, Xavier NL, Cavalheiro JA, Rabin EG, Bittelbrunn A, et al. Rotinas em mastologia. 2ª ed. Porto Alegre: Artmed; 2007.
4. Brasil. Ministério da Saúde. Instituto Nacional de Câncer. Estimativa 2010: incidência de câncer no Brasil. Rio de Janeiro: Instituto Nacional de Câncer; 2009.
5. Caponero R, Donato EMOD, Malzyner A. A metamorfose de uma angústia: o tratamento do câncer de mama de Halsted ao BRCA-1. In: Gimenes MGG, Fávero MH, eds. A mulher e o câncer. Campinas: Livro Pleno; 2000. p.71-107.
6. Gabka CJ, Bohmert H. Cirurgia plástica e reconstrutiva da mama. 2a ed. Porto Alegre: Artmed; 2010.
7. Pelay MJ, Oroz J, Colas C. Reconstrução da mama com expansor de próteses. Anales Sis San Navarra. 2005;28 Suppl 2.
8. Spear SL, Mesbahi AN. Reconstrução com implantes. In: Neligan PC, Lipa JE, eds. Reconstrução mamária pós-mastectomia: cirurgia plástica. Rio de Janeiro: Dilivros; 2008. p.81-96.
9. Guimarães GS, Daher JC, Cammarota MC. Reconstrução mamária com expansor permanente: uma outra alternativa. Rev Bras Cir Plást. 2008;23(2):75-81.
10. Spear SL, Pelletiere CV, Lockwood M. Immediate breast reconstructions with tissue expanders and AlloDerm. In: Spear SL, ed. Surgery of the breast: principles and art. 2nd ed. Philadelphia: Lippincott Williams & Wilkins; 2006. p. 484-8.
11. Lifecell Corporation package insert. Branchburg: Lifecell Corp; 2004.
12. Becker H. One stage immediate breast reconstruction with adjustable implants. In: Spear SL, ed. Surgery of the breast: principles and art. 2nd ed. Philadelphia: Lippincott Williams & Wilkins; 2006. p.438-50.
13. Becker H. The expandable mammary implant. Plast Reconstr Surg. 1987;79(4):631-7.
14. Avelar LET, Tostes ROG, Andrade Junior JCCG, Ribeiro GVC, Tavares MV. Reconstrução imediata do volume mamário com expansores permanentes. Rev Soc Bras Cir Plást. 2007;22(3):162-9.
Cirurgião plástico, membro titular da Sociedade Brasileira de Cirurgia Plástica, Erechim, RS, Brasil.
Correspondência para:
Rinede Luis Manfredini
Rua São Paulo, 466 - sala 1.206 - Centro
Erechim, RS, Brasil - CEP 99700-000
E-mail: cirurgiaplastica@awo.com.br
Artigo submetido pelo SGP (Sistema de Gestão de Publicações) da RBCP.
Artigo recebido: 11/3/2011
Artigo aceito: 13/8/2011
Trabalho realizado no Hospital de Caridade de Erechim e na Uniclínica/UNIMED Erechim, Erechim, RS, Brasil.
Trabalho apresentado para ascensão a membro titular da SBCP.


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter