

Original Article - Year 2011 - Volume 26 -
Hemicelulose em reconstrução da parede abdominal em ratos
Reconstruction of the abdominal wall in rats with hemicellulose
RESUMO
Introdução: As perdas de substância da parede abdominal (PSPA) revestem-se de importância clínica e cirúrgica em função da alta frequência com que ocorrem, do sofrimento que produzem e do alto custo dos tratamentos atualmente ministrados. Nos últimos anos, tem-se observado o desenvolvimento de novas técnicas para a resolução das perdas de substância da PSPA, entre as quais se incluem a realização de retalhos e o uso de materiais biocompatíveis e sintéticos. Método: Esse estudo experimental aleatório e não controlado avaliou o uso da hemicelulose para a reparação das PSPA em 40 ratos Wistar EPM III, femêos. Os animais foram divididos em quatro grupos experimentais de estudo: I (n=10), II (n=10), III = (n=10) e IV (n=10). Todos os animais foram submetidos a anestesia geral utilizando-se o tiopental sódico, via intraperitonial. Foi provocada uma lesão de 2,0 x 3,0cm no tecido músculo-aponeurótico e peritônio da região anterior do abdome. A aposição da película de hemicelulose sobre a lesão foi realizada superpondo-se 15 películas de 2,0 x 3,0cm, umedecidas em soro fisiológico a 0,9%. A película foi fixada à parede muscular adjacente e, em seguida, foi realizada a síntese da pele e panículo carnoso por meio de sutura contínua com fio de náilon de número cinco zeros. A eutanásia dos animais dos grupos I (n=10), II (n=10), III (n=10) e IV (n=10) foi realizada após 3, 28, 35 e 240 dias, respectivamente. Conclusão: Esse estudo concluiu que a hemicelulose foi eficiente em reparar as grandes perdas da parede abdominal em ratos.
Palavras-chave: Parede abdominal/cirurgia. Implantes experimentais. Ratos. Histologia.
ABSTRACT
Introduction: Loss of abdominal wall substance (LAWS) is clinically and surgically important because of its high incidence, the distress it causes, and the high cost of its current treatments. Recently, new techniques have been developed to treat LAWS, including the creation of flaps and use of biocompatible synthetic materials. The aim of this randomized uncontrolled experimental study was to assess the suitability of hemicellulose film for LAWS repair in rats. Methods: Forty female Wistar EPM III rats were divided into 4 groups (I-IV) of 10 animals each. All the animals received general anesthesia with 40 mg/kg intraperitoneal thiopental sodium. A 2.0 × 3.0 cm area of muscle-aponeurotic tissue and peritoneal damage was created in the anterior abdomen of every rat. Fifteen 2.0 × 3.0 cm hemicellulose films soaked in 0.9% saline were affixed in overlapping layers to the adjacent muscle walls with 8 separate 5-0 nylon sutures, and the skin and panniculus carnosus were synthesized by placing continuous 5-0 nylon sutures. The animals in groups I, II, III, and IV were euthanized after 3, 28, 35, and 240 days, respectively. Conclusion: Hemicellulose film is effective for repairing LAWS in rats.
Keywords: Abdominal wall/surgery. Implants, experimental. Rats. Histology.
As perdas de substância da parede abdominal (PSPA) revestem-se de importância clínica e cirúrgica em função da alta frequência com que ocorrem, do sofrimento que produzem, da proliferação bacteriana verificada em expressivo número de casos e também do alto custo dos tratamentos atualmente ministrados.
Um desafio que envolve os cirurgiões atuais é o de obter a ação de fechar a parede abdominal quando as margens do retalho músculo-aponeurótico encontram-se amplamente separadas1. A extensa perda tecidual após o traumatismo ou tumores, a extrusão de vísceras edemaciadas por meio da lesão e o enfraquecimento da parede abdominal por infecção compõem alguns dos fatores que limitam o sucesso do fechamento primário dessas lesões. Como consequência, podem ocorrer deiscência da ferida, hérnia incisional e evisceração. Para minimizar a ocorrência de tais complicações, muitos cirurgiões não realizam a sutura primária da lesão, aguardando até o restabelecimento homeostático do paciente; outros preferem tentar a sutura primária para evitar sequelas, como perda de fluido e calor, hipermetabolismo e fístula enteral2.
Desta forma, têm-se observado nos últimos anos o desenvolvimento de novas técnicas para a resolução das PSPA, entre as quais se incluem a rotação de retalhos e o uso de materiais biocompatíveis e sintéticos3-6. Atualmente, as próteses sintéticas ou derivadas de materiais biocompatíveis têm sido utilizadas com frequência nas reconstruções das PSPA, em decorrência principalmente da simplicidade do procedimento cirúrgico e da diminuição da necessidade de outras cirurgias, tornando-se o procedimento de escolha em muitos países6,7.
A evolução do uso de materiais para o tratamento das PSPA tem sido motivo de pesquisa desde o fim do século XIX com o trabalho de Witzel8, que usou uma prótese de prata para a reconstrução das PSPA. Burke9 introduziu o tântalo em cirurgia, abandonado após a comprovação de sua tendência à fragmentação e frequentes complicações, como fístulas no intestino delgado, ulcerações e extrusão de fragmentos do metal por meio do peritônio e da pele10. A partir da década de cinquenta, uma variedade de polímeros sintéticos ou disponíveis, como o polietileno tereftalato (Dacron ®)11, o polipropileno monofilamentar (Marlex ®) e o polipropileno com filamento duplo (Prolene ®)12, o politetrafluoretileno multifilamentar (Teflon ®) não-poroso, abandonado precocemente, e o polímero de politetrafluoretileno expandido (ePTFE), que apresenta forma porosa, resultando em uma diminuição da reação tecidual tipo corpo estranho13. Posteriormente, o politetrafluoretileno evoluiu para uma forma denominada Gore-tex ®8, que se incorporou ao grupo de materiais usados para as reconstruções da parede abdominal.
A literatura mundial tem apresentado vários outros materiais para a correção das PSPA. Têm sido estudados próteses de poliéster multifilamentar (Mersilene ®)14 e compostos que envolvem ácidos lático e glicólico, como o ácido poliglicólico, a poliglactina e suas variantes (Vicryl ®)13,15, derivados do colágeno16, próteses de poliamida monofilamentar (náilon)17, submucosa de intestino delgado suíno18, pericárdio bovino tratado com gluteraldeído19, uma combinação do polipropileno com poliglactina 910 (SHM)6, enxerto autólogo de pele total20, dura-máter humana desidratada (Tutoplast ®)20,21, uma combinação do polipropileno com o ePTFE (Bard Composix)22, próteses de poliviniledeno fluorado (PDVF)23, poliuretano recoberto com polietileno (PolyesterComposite)24 e próteses de baixo-peso constituídas de polipropileno e poliglactina multifilamentar (Vypro II)7.
Apesar do grande número de materiais sintéticos e biocompatíveis disponíveis, há mais desvantagens específicas do que vantagens entre os diversos materiais usados na Medicina23. Dentre as desvantagens, têm-se as aderências intestinais à prótese e as reações inflamatórias, grau de fibroplasia, reabsorção da película, a formação ou não de cápsula e o surgimento de tumor desenvolvidos no organismo após o implante do material, sendo estas as características que mais influenciam a escolha de uma prótese e motivam a pesquisa de novos materiais, como a película de hemicelulose deste estudo. Registrada e patenteada em 1990 (DIMED/MS 8306340 Brasil) por Lauro Xavier Filho e Marçal de Queiroz Paulo, a película de hemicelulose, elaborada mediante processo que envolve biotecnologia, teve sua aplicação reconhecida com a publicação de Solas et al.25, sendo utilizada atualmente como substituto temporário da pele humana em lesões superficiais após queimaduras e escoriações26.
O objetivo deste estudo é avaliar a hemicelulose na reparação das perdas de substância da parede anterior do abdome em ratos.
MÉTODO
Este foi um estudo experimental aleatório e não-controlado em animais de experimentação, realizado no Biotério Central da Universidade Federal de Alagoas.
A película em estudo, obtida por meio da cultura do Acetobacter xylinum, Saccharomyces cervisiae e Saccharomyces pompe, é composta de glucosamina, n-acetil-galactosamina, aminoácidos e carboidrato; não possui aditivos ou modificações químicas; de coloração creme, com tendência ao branco; com espessura média de 0,05 mm, resistente à tração, com grau médio de maleabilidade e resistente à temperatura de até 150ºC; possui superfície granulada que permite trocas gasosas limitadas (Figura 1).

Figura 1 - Película de hemicelulose.
Foram utilizados quarenta ratos EPM III Wistar, fêmeas, adultos com idade em torno de quatro a seis meses, pesando entre duzentos e trezentos gramas. Os animais eram mantidos em ambiente fechado, devidamente refrigerado, à temperatura de 22ºC, sob luz artificial, recebendo água e ração ad libitum. Os ratos receberam cuidados diários e tiveram suas gaiolas trocadas duas vezes por semana, sendo observados por, pelo menos, quinze dias antes da pesquisa, conforme as regras estabelecidas na Lei Federal 6638.
Os animais foram divididos aleatoriamente por sorteio em quatro grupos distintos com dez animais (grupos I, II, III e IV), de acordo com o Quadro 1.

Foram realizados os seguintes procedimentos experimentais: anestesia, ato cirúrgico e eutanásia.
Anestesia
Antes da realização de qualquer procedimento, os animais foram devidamente pesados em balança eletrônica (Filizola - modelo MF3). Todos os animais foram submetidos à anestesia geral utilizando-se o tiopental sódico (um grama de pó estéril diluído em quarenta mililitros de soro fisiológico a 0,9%), via intraperitonial, na dose de quarenta miligramas por quilograma de peso. A indução era conseguida em aproximadamente dez minutos e a anestesia durava em torno de uma hora; nos casos de necessidade de prolongar o tempo anestésico, era injetado um quarto da dose inicial. Após a anestesia, o animal era fixado em decúbito dorsal por meio de fita adesiva em tábuas de 20x30cm, recobertas por cortiça. O abdome do animal foi epilado manualmente e a antissepsia foi feita com iodopovidona degermante.
Ato cirúrgico
O ato cirúrgico era iniciado por meio de uma incisão mediana longitudinal, desde o processo xifoide do animal à porção inferior do músculo reto do abdome. A pele e o panículo carnoso foram separados dos músculos da parede abdominal e, a 1 cm abaixo do processo xifoide, foi provocada uma lesão previamente delimitada por um molde de papel vegetal de 2,0 x 3,0cm (2 cm de largura látero-lateral e 3 cm de comprimento no sentido crânio-caudal), retirando-se um fragmento de tecido músculo-aponeurótico e peritônio da região anterior do abdome de tamanho equivalente (Figura 2). A aposição da película de hemicelulose sobre a lesão era realizada superpondo-se quinze películas de 2,0x3,0cm, umedecidas em soro fisiológico a 0,9% (Figura 3). A película foi fixada à parede muscular adjacente por meio de oito pontos separados, com fios de náilon de número cinco zeros (Figura 4). Em seguida, foi realizada a síntese da pele e panículo carnoso por meio de sutura contínua com fio de náilon de número cinco zeros.

Figura 2 - Lesão de 2,0 x 3,0cm provocada na região anterior do abdome.

Figura 3 - Fragmento de tecido músculo-aponeurótico e peritônio da região anterior do abdome e aposição da película de hemicelulose medindo 2,0 x 3,0cm.

Figura 4 - Película de hemicelulose umedecida posicionada e fixa à parede muscular adjacente.
Terminados os procedimentos cirúrgicos, todos os animais foram avaliados durante todos os dias do pós-operatório, sendo observados a presença ou não de infecção, hérnia abdominal, deiscências, secreção serosa e hematomas.
Eutanásia
Durante a preparação que antecedia a eutanásia dos animais, recipientes com tampas padronizadas contendo cinquenta mililitros de formol a 10%, onde eram conservados os fragmentos da região anterior do abdome, foram devidamente identificados com etiquetas contendo os seguintes dados: espécie, identificação mediante marcação na orelha, data de nascimento, data da cirurgia, tipo de cirurgia com descrição do ato cirúrgico, peso na cirurgia, data da eutanásia e peso após a eutanásia e identificação da lâmina do exame anatomopatológico.
Posteriormente, os animais eram submetidos à administração de oitenta miligramas de tiopental sódico intraperitoneal e, após detectado o óbito, devidamente pesados em balança eletrônica. Em seguida, foram submetidos à cirurgia para retirada do fragmento abdominal, contendo o objeto de estudo e o tecido íntegro. Após a retirada, os fragmentos abdominais foram imersos em soro fisiológico para limpeza e, logo depois, cada fragmento foi colocado, com a película voltada para cima, em seu recipiente de acordo com a identificação.
A eutanásia dos animais dos grupos I (n=10), II (n=10), III (n=10) e IV (n=10) foi realizada após 3, 28 dias, 35 dias e 240 dias, respectivamente.
Após a realização da eutanásia, todos os animais foram observados e analisados quanto à apresentação de sinais de infecção na ferida operatória, hérnia ou deiscência, à presença de secreções serosas ou de hematomas na região anterior do abdome e aderências intestinais à película. Posteriormente, os fragmentos abdominais foram conservados em formol a 10% e enviados ao Serviço de Anatomia Patológica do Hospital Universitário (HU/UFAL) para serem analisados.
A avaliação macro e microscópica dos fragmentos abdominais contendo a película foi controlada pelo pesquisador e por um único patologista do Hospital Universitário (HU/UFAL) e todos os resultados dos exames anatomopatológicos foram analisados pela mesma equipe e compilados em questionário individual os aspectos macroscópicos e microscópicos dos animais (Quadro 2).

A obtenção dos cortes histológicos era realizada com a infiltração do tecido após fixação em uma solução de parafina. Nesse processo, os tecidos necessitaram ser desidratados em etanol para a remoção dos lipídios. Posteriormente, foram realizados os cortes histológicos através de um micrótomo Jung/Reisterstown numa espessura de três a quatro micra (mm). A coloração dos tecidos era então iniciada com a hematoxilina e eosina, para a leitura das células epiteliais; tricrômico de Gomori, para o tecido conjuntivo e colágeno; coloração de Voerhoff, para as fibras elásticas; e impregnação argêntica (reticulina) para as fibras reticulares.
A avaliação dos resultados obtidos foi centrada na avaliação macroscópica, na análise histológica da intensidade da resposta inflamatória do organismo dos animais em relação à película, sistematizada em leve, moderada e intensa, levando-se em consideração também a presença ou não de tecido de granulação, reabsorção da película, neoformação vascular, grau de fibroplasia, aderência das vísceras à película, formação de cápsula e desenvolvimento de tumor.
Método Estatístico
O Epi-Info 2002, produto do Centers for Disease Control and Prevention de Atlanta, EUA, foi utilizado para a montagem do banco de dados e análise estatística no nível de confiança de 95%.
Foi aplicada pontuação aos resultados categóricos das variáveis (Quadro 3). A hipótese H0 (igualdade), da pontuação resultante de cada variável nos grupos, foi testada por meio do ANOVA quando o teste de Bartlett's indicava homogeneidade de variâncias; caso contrário, usou-se o Teste de Kruskal-Wallis no nível de confiança de 95%. A regressão linear com gráfico de dispersão foi gerada para avaliar a correlação entre as variáveis.

RESULTADOS
Não foram observados casos de infecção, hérnia abdominal, deiscência, secreção serosa ou hematomas nos animais dos grupos I e II. No grupo III, foi verificado um caso de deiscência e dois animais com secreção serosa. Enquanto o grupo IV apresentou um caso de deiscência e outro de secreção serosa (Tabela 1).
Os resultados da avaliação microscópica dos grupos de estudo estão apresentados sob a forma de quadro e gráficos contendo frequência, porcentagem e intervalo de confiança a 95% (Quadro 4, Figuras 5 a 15).
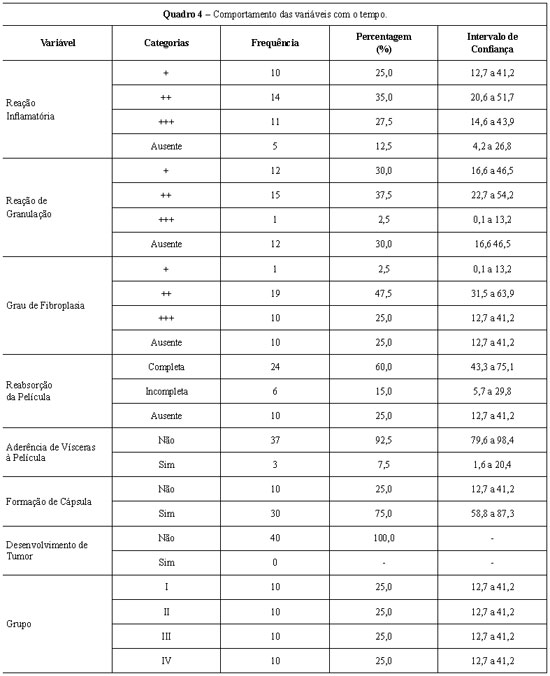
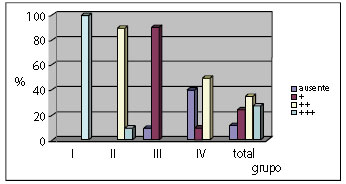
Figura 5 - Distribuição percentual da reação inflamatória por grupo.
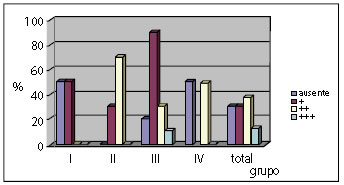
Figura 6 - Distribuição percentual da reação de granulação por grupo.
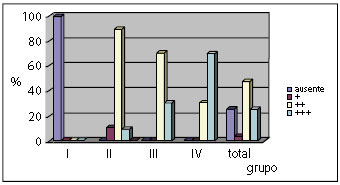
Figura 7 - Distribuição percentual do grau de fibroplasia por grupo.
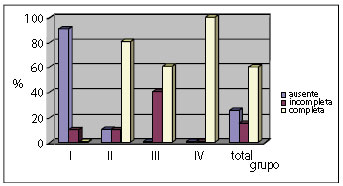
Figura 8 - Distribuição percentual da reabsorção da película por grupo.
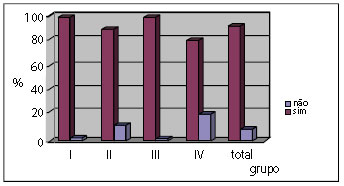
Figura 9 - Distribuição percentual da aderência de vísceras à película por grupo.
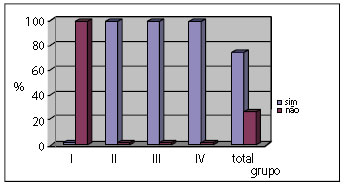
Figura 10 - Distribuição percentual da formação de cápsula por grupo.
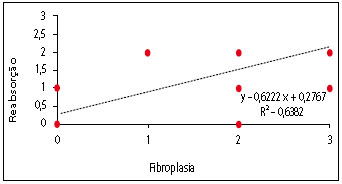
Figura 11 - Dispersão e regressão entre grau de fibroplasia e reabsorção da película.
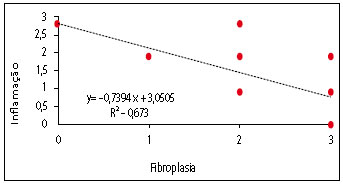
Figura 12 - Dispersão e regressão entre grau de fibroplasia e reação inflamatória.
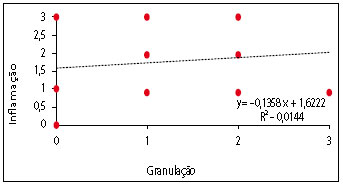
Figura 13 - Dispersão e regressão entre grau de granulação e reação inflamatória.
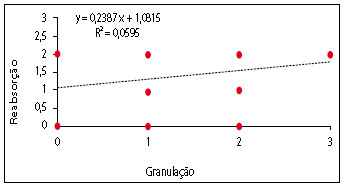
Figura 14 - Dispersão e regressão entre grau de granulação e reabsorção da película.
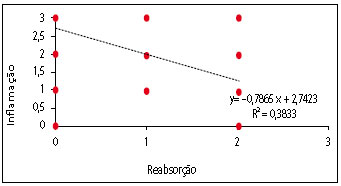
Figura 15 - Dispersão e regressão entre reabsorção da película e reação inflamatória.
Não foram pontuadas as aderências das vísceras à película, formação de cápsula e desenvolvimento de tumor.
DISCUSSÃO
As PSPA constituem-se ainda em grande problema de saúde pública e a procura do material ideal para substituir parte da parede abdominal continua sendo um desafio para a cirurgia moderna. As características de um material ideal foram postuladas por Scales em 1953 e descritas por Roa27. Scales referiu que o substituto ideal do tecido humano deveria não causar reações inflamatórias ou de corpo estranho, não produzir reação de hipersensibilidade, não ser carcinogênico, ser quimicamente inerte e capaz de suportar esforços e tensões, ser esterilizável, não ser modificado pelos tecidos que o envolvem e possuir condições de ser fabricado em série27.
O objetivo deste estudo experimental foi o de analisar a capacidade da película de hemicelulose em substituir parte da parede abdominal de ratos Wistar, convém ressaltar que não foi estudada a força tênsil da película, não houve mensuração da rigidez ou motilidade intestinal. Não foi em nenhuma das fases do estudo experimental utilizado qualquer artifício para a indução de infecção abdominal. A intenção deste estudo se concentrou na avaliação dos questionários individuais de todos os animais (n=40), procurou-se estudar os aspectos macroscópicos e microscópicos da película de hemicelulose posicionada na PSPA em ratos EPM III Wistar fêmeas.
A película de hemicelulose (Bioskin ®) é constituída de glucosamina, n-acetil-galactosamina, aminoácidos, carboidratos polissacarídeos e obtida por meio da cultura do Acetobacter xylinum, do Saccharomyces cervisiae e do Saccharomyces pompe. A celulose consiste em um polímero não-ramificado de resíduos de glicose organizados em uma cadeia linear, onde cada resíduo de glicose é rodado aproximadamente 180°. A glucosamina é encontrada em alta concentração no espaço articular e estimula a fabricação de substâncias necessárias para o tratamento das lesões inflamatórias articulares28. A n-acetil-galactosamina é formada pela galactose contendo um grupo amina juntamente com o acetil obtido por meio da acetilação28. O Acetobacter xylinum é uma bactéria gram-negativa, envolvida com a síntese da celulose, sendo o modelo para estudo das enzimas e genes envolvidos com a biossíntese da celulose29. O Saccharomyces cervisiae e o Saccharomyces pompe são fungos que possuem núcleos dispersos em um micélio, não possuem plastos ou pigmentos fotossintéticos e sua nutrição é obtida por absorção29.
A película usada neste estudo assemelha-se ao Biofill ®, película de celulose que é produzida pela biossíntese de bactérias do gênero Acetobacter, estudada como curativo biológico satisfatório e eficaz no tratamento de queimaduras e escoriações traumáticas ou cirúrgicas, como a dermoabrasão30-32. Esses autores descreveram a película de celulose como substituto temporário da pele humana. Os casos clínicos apresentados expressaram que o Biofill ® sofre um processo de desidratação que evolui para uma crosta espessa, de coloração acastanhada, quando posicionada sobre a área cruenta de uma escoriação ou queimadura. Concluiu-se que a película forneceu uma cobertura temporária satisfatória e eficaz para lesões de pouca profundidade e áreas de pequena mobilidade, que a aderência à superfície cruenta diminui a dor e as perdas eletrolíticas e referiram também que a transparência possibilita uma constante inspeção da ferida e pronto tratamento nos casos em que ocorrem complicações. Os estudos de Silva et al.33, Tucci et al.34 e Legaz et al.26, que envolveram o uso da película de hemicelulose, obtiveram conclusões muito próximas das anteriormente descritas.
O motivo do uso da película de hemicelulose (Bioskin ®) como substituto da parede abdominal de ratos Wistar foi o de encontrar um material que desenvolvesse integração biológica com mínima reação tecidual, induzindo pouca aderência intestinal no pós-operatório imediato e tardio, que não desenvolvesse reação tipo metaplasia e displasia com o surgimento de tumoração maligna, que não necessitasse de remoção em casos de infecção local e que apresentasse baixo custo.
Foi evidenciado que o uso de ratos Wistar não reproduz exatamente a situação de uma investigação em seres humanos, e que um modelo como o rato Wistar se contrapõe a sua disponibilidade, facilidade no manuseio, custo e considerações éticas e bioéticas distintas do ser humano35-37.
Todos os animais foram operados com idade entre quatro e seis meses e peso entre duzentos e trezentos gramas, com a intenção de minimizar os efeitos provocados pela idade e pelo peso no processo de cicatrização e na resposta metabólica do animal35.
O pentobarbital sódico por via intraperitonial foi escolhido como anestésico, por minimizar a insuficiência respiratória provocada pelo éter etílico e por se tratar de uma medicação tão segura quanto o hidrocloreto de ketamina20,38,39, além de sua larga utilização em estudos semelhantes40-42.
Em todos os animais, a lesão realizada media 2,0x3,0cm, sendo retirado um fragmento de tecido músculo-aponeurótico da parede abdominal. O tamanho dessa lesão obedeceu aos preceitos dos trabalhos vinculados à cicatrização de Milton43 e estão muito próximos das medidas propostas por Walter et al.16, Birbilis et al.44 e Hooker et al.45, que foram de 3,0x4,0cm e de Baptista et al.46, que media 2,5x2,5cm.
O peso dos animais, aferidos individualmente no início e no fim do experimento, apresentou uma normalidade nos dados. Quando comparados os grupos, foi observado que: os animais do grupo I (n=10) com eutanásia realizada três dias após a cirurgia perderam peso; os do grupo II (n=10) com eutanásia após quatro semanas não apresentaram diferenças significativas entre o início e o fim do experimento; nos animais dos grupos III (n=10) e IV (n=10) houve ganho ponderal significativo. Esses eventos acima sugerem que não foram observadas variáveis que determinassem modificação no pós-operatório dos animais operados.
Em todos os animais, a fixação da película ao tecido músculo aponeurótico foi realizada com o fio cirúrgico monofilamentar cinco zeros não-absorvível (náilon), considerado o mais apropriado, com base no estudo específico de Bucknall47. No entanto, Toosie et al.39 demonstraram que o uso tópico da cola de fibrina em substituição aos fios de sutura reduz a aderência intestinal após a reconstrução das hérnias com prótese em ratos, mas neste estudo não foi usada a cola de fibrina.
O método histológico ideal seria aquele que resultasse em um desvio mínimo da condição do estado vivo, e ainda permitisse uma resolução máxima dos diversos componentes teciduais. O requisito para o exame anatomopatológico foi o de usar os fixadores que desenvolvessem menor quantidade de precipitados, sendo os preparados fixados com formol os melhores para o estudo com microscópio óptico.
Nenhum dos animais submetidos à reconstrução da PSPA com aposição da película apresentou herniações na parede abdominal e a análise macroscópica dos segmentos contendo a película revelou aderências viscerais no rato número nove do grupo II e nos ratos sete e nove do grupo IV; esse mesmo resultado foi encontrado no exame anatomopatológico. Esse achado é compatível com o verificado na literatura por Cnota et al.2 e Jenkins et al.15. A análise microscópica dos grupos de estudo observou que a película de hemicelulose desempenhou em ratos Wistar EPM III fêmeas, o papel de um implante que, cirurgicamente inserido nos animais, foi eficiente para conter a formação de hérnia abdominal, desencadeou equilíbrio com os tecidos circunvizinhos e confirmou as características de um implante tolerável descritas por Roa27.
Os testes estatísticos foram aplicados para avaliar a evolução da cicatrização nos grupos, não comparando a película de hemicelulose com outro implante.
No conjunto de gráficos de Dispersão e Regressão Linear (Figuras 11 a 15), pode ser observado que a correlação foi fraca para aquelas que envolveram a Reação de Granulação. Esse fenômeno é justificado porque a Granulação obteve maior pontuação no Grupo de estudo II, não aumentando ou diminuindo de forma regular com o tempo. A correlação das outras variáveis que não envolveram a granulação foi muito boa, exceto a correlação entre reabsorção e inflamação, que foi boa. A tendência decrescente das curvas entre Fibroplasia versus Inflamação e Reabsorção versus Inflamação é um fenômeno esperado. O conjunto de resultados da Regressão fala a respeito de um processo de cicatrização que se encontra nos limites da normalidade.
O conjunto de Gráficos da distribuição percentual das variáveis (Figuras 5 a 10) demonstra que a Inflamação reduziu com o tempo, a Granulação é mais presente nos grupos de estudo II e III, a Fibroplasia aumentou com o tempo, a Reabsorção foi completa no grupo de estudo IV, o grau de aderência intestinal não foi encontrado nos grupos de estudo I e III e foi pouco presente nos grupos de estudo II e IV, por fim a formação de Cápsula foi evidenciada a partir do grupo de estudo II.
No quadro da análise de variância pode ser confirmado que as diferenças entre os grupos para cada pontuação, dadas as variáveis, foram significativas. A reação inflamatória é mais forte no grupo de estudo I; a Granulação, no grupo de estudo II; a Fibroplasia, no grupo de estudo IV; e a Reabsorção, no grupo de estudo IV. Esses resultados confirmam estatisticamente um processo de cicatrização, envolvendo o implante de hemicelulose, que evoluiu sem anormalidades e beneficiando os animais dos grupos de estudo (I, II, III, e IV).
CONCLUSÃO
A hemicelulose foi eficiente para reparar as perdas de substância da parede anterior do abdome em ratos.
Nenhum dos animais apresentou herniações na parede abdominal.
Análise macroscópica revelou aderências viscerais no rato número nove do grupo de estudo II e nos ratos sete, oito, nove e dez do grupo de estudo IV, esse mesmo resultado foi encontrado no exame anatomopatológico.
A análise microscópica dos grupos de estudo observou que a película de hemicelulose foi eficiente para conter as vísceras intestinais dos animais e evitar a formação de hérnia.
REFERÊNCIAS
1. Kapan S, Kapan M, Goksoy E, Karabicak I, Oktar H. Comparison of PTFE, pericardium bovine and fascia lata for repair of incisional hernia in rat model, experimental study. Hernia. 2003;7(1):39-43.
2. Cnota MA, Aliabadi-Wahle S, Choe EU, Jacob JT, Flint LM, Ferrara JJ. Development of a novel synthetic material to close abdominal wall defects. Am Surg. 1998;64(5):415-8.
3. Chung S, Hazen A, Levine JP, Baux G, Olivier WA, Yee HT, et al. Vascularized acellular dermal matrix island flaps for the repair of abdominal muscle defects. Plast Reconstr Surg. 2003;111(1):225-32.
4. de Vries Reilingh TS, van Goor H, Rosman C, Bemelmans MH, de Jong D, van Nieuwenhoven EJ, et al. "Components separation technique" for the repair of large abdominal wall hernias. J Am Coll Surg. 2003;196(1): 32-7.
5. Dumanian GA, Denham W. Comparison of repair techniques for major incisional hernias. Am J Surg. 2003;185(1):61-5.
6. Klinge U, Klosterhalfen B, Conze J, Limberg W, Obolenski B, Ottinger AP, et al. Modified mesh for hernia repair that is adapted to the physiology of the abdominal wall. Eur J Surg. 1998;164(12):951-60.
7. Junge K, Klinge U, Rosch R, Klosterhalfen B, Schumpelick V. Functional and morphologic properties of a modified mesh for inguinal hernia repair. World J Surg. 2002;26(12):1472-80.
8. Bauer JJ, Salky BA, Gelernt IM, Kreel I. Repair of large abdominal wall defects with expanded polytetrafluoroethylene (PTFE). Ann Surg. 1987;206(6):765-9.
9. Burke GL. The corrosion of metals in the tissues; and an introduction to tantalum. Can Med Assoc J. 1940;43(2):125-8.
10. Adler RH. An evaluation of surgical mesh in the repair of hernias and tissue defects. Arch Surg. 1962;85:836-44.
11. Wolstenholme JT. Use of commercial dacron fabric in the repair of inguinal hernias and abdominal wall defects. AMA Arch Surg. 1956;73(6):1004-8.
12. Usher FC. A New technique for reparing large abdominal wall defects. Arch Surg. 1961;82:870-7.
13. Lamb JP, Vitale T, Kaminski DL. Comparative evaluation of synthetic meshes used for abdominal wall replacement. Surgery 1983;93(5):643-8.
14. Cerise EJ, Busuttil RW, Craighead CC, Ogden WW 2nd. The use of Mersilene mesh is repair of abdominal wall hernias: a clinical and experimental study. Ann Surg. 1975;181(5):728-34.
15. Jenkins SD, Klamer TW, Parteka JJ, Condon RE. A comparison of prosthetic materials used to repair abdominal wall defects. Surgery. 1983;94(2):392-8.
16. Walter M, Brenner U, Holzmuller W, Muller JM. Experiments with a biological material for the closure of incisional hernias. Lab Anim. 1987;21(3):195-200.
17. Nyhus LM, Condom RE. Hernia. 3ª ed. Philadelphia:Lippincott;1989.
18. Prevel CD, Eppley BL, Summerlin DJ, Jackson JR, McCarty M, Badylak SF. Small intestinal submucosa: utilization for repair of rodent abdominal wall defects. Ann Plast Surg. 1995;35(4):374-80.
19. Olmos Zúñiga JR, Jasso Victoria R, Sotres Vega A, Arreola Ramírez JL, Gaxiola Gaxiola M, Vanda Cantón B, et al. Utilización de bioprótesis liofilizadas en la reparacíon de defectos abdominales en ratas. Rev Inst Nal Enf Resp Méx. 1996;9(3):183-6.
20. Kama NA, Coskun T, Yavuz H, Doganay M, Reis E, Akat AZ. Autologous skin graft, human dura mater and polypropylene mesh for the repair of ventral abdominal hernias: an experimental study. Eur J Surg. 1999;165(11):1080-5.
21. Baykal A, Yorganci K, Sokmensuer C, Hamaloglu E, Renda N, Sayek I. An experimental study of the adhesive potential of different meshes. Eur J Surg. 2000;166(6):490-4.
22. Ferrando JM, Vidal J, Armengol M, Gil J, Manero JM, Huguet P, et al. Experimental evaluation of a new layered prosthesis exhibiting a low tensile modulus of elasticity: long-term integration response within the rat abdominal wall. World J Surg. 2002;26(4):409-15.
23. Klinge U, Klosterhalfen B, Ottinger AP, Junge K, Schumpelick V. PVDF as a new polymer for the construction of surgical meshes. Biomaterials. 2002;23(16):3487-93.
24. Zieren J, Paul M, Osei-Agyemang T, Maecker F, Muller JM. Polyurethane-covered dacron mesh versus polytetrafluoroethylene DualMesh for intraperitoneal hernia repair in rats. Surg Today 2002;32(10):884-6.
25. Solas MT, Vicente C, Xavier L, Legaz ME. Ionic adsorption of catalase on bioskin: kinetic and ultrastructural studies. J Biotechnol. 1994;33(1):63-70.
26. Legaz ME et al. Quaternary structure of catalase using a bioskin-immobilized enzyme. Biotechnology Techniques. 1998;12(6):481-4.
27. Roa TT. Materiales inertes. In: Coiffman F, ed. Texto de cirurgia plastica, reconstructiva y estetica. Barcelona: Salvat;1986. p.182-5.
28. Baici A, Hörler D, Moser B, Hofer HO, Fehr K, Wagenhäuser FJ. Analisis of glycosaminoglycans in human serum after oral administration of chondroitin sulfate. Rheumatol Int. 1992;12(3):81-8.
29. Fontana JD, Franco VC, de Souza SJ, Lyra IN, de Souza AM. Nature of plant stimulators in the production of Acetobacter xylinum ("tea fungus") biofilm used in skin therapy. Appl Biochem Biotechnol. 1991;28-29:341-51.
30. Cabral LM. Curativo biológico no tratamento do grande queimado: apresentação de caso. Rev Bras Cir. 1987;77(6):383-9.
31. Pitanguy I, Salgado F, Maracajá PF. Utilização de película de celulose (Biofillâ) como curativo biológico. Rev Bras Cir. 1988;78(5):317-26.
32. Rebello C, Almeida DA, Lima Júnior EM, Dornelas MP. Bio-fill: um novo substituto de pele: nossa experiência. Rev Bras Cir. 1987;77(6):407-14.
33. Silva SC, Sperança PA, Gusmão ES. Avaliação clínica da membrana biológica Bioskin ®(Hemicelulose) na técnica de regeneração tecidual guiada. Periodontia. 1995;5(2):233-42.
34. Tucci MG et al. Valutazione dell'efficacia clinica e della tollerabilità di un nuovo biomateriale per il trattamento delle perdite di sostanza della cute. Chron. Derm. 1996;6(4):499-507.
35. Donovan WE. Modelos experimentales en la investigación de los colgajos cutáneos. In: Grabb WC, Myers MB, eds. Colgajos cutáneos. Barcelona: Salvat, 1982. p. 11-20. Versão espanhola.
36. Lawrence WT, Murphy RC, Robson MC, Heggers JP. The detrimental effect of cigarette smoking on flap survival: an experimental study in the rat. Br J Plast Surg. 1984;37(2):216-9.
37. van Adrichem LN, Hoegen R, Hovius SE, Kort WJ, van Strik R, Vuzevski VD. The effect of cigarette smoking on the survival of free vascularized and pedicled epigastric flaps in the rat. Plast Reconstr Surg. 1996;97(1):86-96.
38. Raman J, Montano SR, Lord RS. Assisted local anaesthesia in rabbits. Microsurgery. 1989;10(1):75-6.
39. Toosie K, Gallego K, Stabile BE, Schaber B, French S, de Virgilio C. Fibrin glue reduces intra-abdominal adhesions to synthetic mesh in a rat ventral hernia model. Am Surg. 2000;66(1):41-5.
40. Klinge U, Klosterhalfen B, Muller M, Schumpelick V. Foreign body reaction to meshes used for the repair of abdominal wall hernias. Eur J Surg. 1999;165(7):665-73.
41. Klosterhalfen B, Klinge U, Schumpelick V. Functional and morphological evaluation of different polypropylene-mesh modifications for abdominal wall repair. Biomaterials. 1998;19(24):2235-46.
42. Simmermacher RK, Schakenraad JM, Bleichrodt RP. Reherniation after repair of the abdominal wall with expanded polytetrafluoroethylene. J Am Coll Surg. 1994;178(6):613-6.
43. Milton SH. The tubed pedicle flap. Br J Plast Surg. 1969;22(1):53-9.
44. Birbilis T, Theodoropoulou E, Birbili A, Dimas S, Leutsakos V. A preliminary report on the use of relon mesh in the repair of eventrations with large parietal defects. An experimental study in rats. J Int Med Res. 1997;25(3):135-40.
45. Hooker GD, Taylor BM, Driman DK. Prevention of adhesion formation with use of sodium hyaluronate-based bioresorbable membrane in a rat model of ventral hernia repair with polypropylene mesh: a randomized, controlled study. Surgery. 1999;125(2):211-6.
46. Baptista ML, Bonsack ME, Delaney JP. Seprafilm reduces adhesions to polypropylene mesh. Surgery. 2000;128(1):86-92.
47. Bucknall TE. Factors influencing wound complications: a clinical and experimental study. Ann R Coll Surg Engl. 1983;65(2):71-7.
1. Chefe do Serviço de Cirurgia Plástica e Reconstrutora do Hospital Universitário da Universidade Federal de Alagoas (UFAL) e Coordenador da Disciplina de Cirurgia Plástica da Faculdade de Medicina da UFAL, Maceió, AL, Brasil.
2. Cirurgião de cabeça e pescoço do Serviço de Cirurgia Plástica e Reconstrutora do Hospital Universitário da UFAL, Setor de Tumores, Maceió, AL, Brasil.
3. Médica graduada na UFAL, Disciplina de Cirurgia Plástica da Faculdade de Medicina da Universidade Federal de Alagoas, Maceió, AL, Brasil.
4. Acadêmica da Faculdade de Medicina da UFAL, Maceió, AL, Brasil.
5. Chefe da Disciplina e do Serviço de Cirurgia Plástica da Universidade Federal de São Paulo, São Paulo, SP, Brasil.
Correspondência para:
Fernando Gomes de Andrade
Rua José Freire Moura, 191/104 - Ponta Verde
Maceió, AL, Brasil - CEP 57000-000
E-mail: fernandogomes1911@hotmail.com
Artigo submetido pelo SGP (Sistema de Gestão de Publicações) da RBCP
Artigo recebido: 27/1/2011
Artigo aceito: 10/3/2011
Trabalho realizado na Universidade Federal de Alagoas, Maceió, AL, Brasil.



 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter