

Original Article - Year 2010 - Volume 25 -
Enxerto ósseo em crânio: princípios básicos para a integração óssea
Bone graft in skull: basic principles for osteointegration
RESUMO
Introdução: A reparação das perdas ósseas evoluiu de maneira significativa a partir do século 20, principalmente na segunda metade, quando a Medicina teve uma evolução importante para resolver os casos de reconstrução de perdas de tecidos. Inicialmente os materiais de inclusão, citando os metais maleáveis, silicone, acrílico de rápida polimerização, apareceram juntamente com o uso de enxerto ósseo autólogo. Os enxertos ósseos autólogos avançaram com muita propriedade, para se tornarem o material de eleição na reparação destas perdas ósseas. Os locais mais importantes para obtenção do enxerto são: crânio, osso ilíaco, costela e tíbia. Nos últimos 30 anos, com o refinamento das técnicas e o uso de material cirúrgico preciso, tanto para retirada do osso para o enxerto, como a colocação do mesmo na área receptora, estes procedimentos se firmaram definitivamente no estudo da reconstrução. Aliado aos recursos citados, salientamos o conhecimento da origem embriológica do osso que é subdividido em ossos cartilaginosos (tíbia, osso ilíaco e costela) e ossos membranosos, portanto, os "ossos parietais" são priorizados para a reparação de ossos cranianos e faciais. Além da origem embriológica, devemos citar também o conhecimento histológico do osso compacto e do osso esponjoso. Citamos, ainda, as células precursoras do tecido ósseo, osteoblastos, osteócitos e osteoclastos.
Palavras-chave: Osso e ossos. Transplante ósseo. Anormalidades craniofaciais/cirurgia.
ABSTRACT
Background: The repair of bone loss had a great improvement starting in the middle of the last century, when the Medicine had a big evolution in solving the problems of tissue loss using initially soft metals, silicone, acrylic of rapid polymerization, came up at the same time of the use of bone graft autologous. The bone graft autologous developed in the way that became the first choice for reconstruction of bone loss. The common area to obtain the bones grafts are: cranial, iliac bones, ribs and tibia. In the last 30 years, with the improvement of techniques and the use of precisely surgical materials, for extraction of the bones for grafts and also for insertion of the bone at the receptor area, these processes established the way to do reconstruction surgeries. Besides the processes listed above we also take in consideration that we had about embryologic origin of the bones with are divided in: cartilaginous bones (tibia, iliac bones and ribs) and membranous bones, therefore the "parietals bones", are prioritized for the repair of cranial and facial bones. Besides the embryologic origin of the bones we should also emphasize the knowledge of the compact bone and spongy bone history. We would like also to mention the precursor cells of the bone tissues, osteoblasts, osteocytes and osteoclasts.
Keywords: Bone and bones. Bone transplantation. Craniofacial abnormalities.
A reconstrução das perdas ósseas do crânio depende fundamentalmente do mecanismo da integração dos enxertos ósseos autólogos e do conhecimento histológico e citológico dos tecidos ósseos, para entender como estes mecanismos funcionam.
Na história da humanidade, há 2000 anos a.C. há relatos de perdas ósseas do crânio em ossadas encontradas em povos do Egito e do México (Civilização dos Maias), só para citar alguns exemplos. A partir de 1678, há descrições na literatura médica de tentativas de abordagens com materiais de inclusão para reparação destas perdas.
A partir da metade do século XX, iniciou-se simultaneamente o uso de materiais de inclusão (metais maleáveis, silicone, acrílico, etc.) e enxertos ósseos autólogos. Estes últimos começaram com os ossos ilíacos e as costelas e, a partir da década de 80, com Paul Tessier et al.1, na França, John Marquis Longacre & Converse2, nos Estados Unidos, e Jorge Psillakis e Vera Cardim3, no Brasil, que acrescentaram técnicas mais precisas para obtenção dos enxertos ósseos do crânio (osso parietal).
No estudo da origem embriológica do tecido ósseo em diferentes partes do corpo, concluiu-se que os ossos da tíbia, ilíaca e costela têm origem embriológica de osso cartilaginoso; por outro lado, o enxerto proveniente do osso parietal tem origem embriológica de osso membranoso. O osso parietal é formado por uma díploe óssea, separado por osso esponjoso, facilitando a obtenção deste enxerto, e quando retirado corretamente, se conseguirá reparar a área doadora com a díploe externa e usando a díploe interna como osso autólogo membranoso, que é obviamente a escolha de eleição para as perdas ósseas do crânio. Citamos, também, no osso parietal as propriedades imunológicas, resistência à reabsorção, facilidade de fixação na área receptora, além do que esse osso cumpre as duas propostas primordiais, que são proteção precisa da massa encefálica devido à mesma forma, e objetivo estético, o que para o paciente do ponto de vista psicológico é de fundamental importância.
Outro aspecto fundamental para obtenção de bons resultados tem sido o refinamento das técnicas cirúrgicas e o uso de material cirúrgico preciso, tanto para a retirada do osso, como para a colocação do mesmo na área receptora. Neste parágrafo é importante salientar que, para o enxerto ser integrado, necessita de três itens fundamentais: 1) Recobrimento de partes moles; 2) Preparação do leito receptor com uso de Drill (broca de videa) para estimular a neoformação de vasos e assim nutrir o enxerto; 3) Fixação rígida do enxerto com fio de aço ou miniplacas metálicas ou reabsorvíveis.
Nesse trabalho, que consiste nos princípios básicos para a integração óssea, exemplificamos quatro casos de enxertos ósseos em crânio, devido à importância fundamental da proteção da massa encefálica como item prioritário e, em segundo plano, a preocupação do ponto de vista estético, principalmente nas perdas ósseas da região frontal.
Na sequência do nosso estudo, é fundamental tecer considerações sobre a histologia e a citologia do tecido ósseo para melhor entender o mecanismo de integração óssea. Iniciando pela citologia, é importante citar: 1) as células precursoras ósseas, que se diferenciam em osteoblastos; 2) os osteoblastos, que são células ativas na deposição óssea e precursoras dos osteócitos; 3) Os osteócitos são células maduras derivadas dos osteoblastos. Nelas se encontra o osso mineralizado, dando sustentação a todo esqueleto; 4) os osteoclastos são células multinucleadas, com origem similar aos macrófagos, sendo ativas na reabsorção e na remodelação do osso. Através dos osteoblastos surgem as fibras colágenas e o fosfato de cálcio que mineraliza o osso, assim como os osteócitos mantêm a matriz óssea mineralizada.
Relativo à histologia, citaremos o osso compacto ou cortical (formado por lamelas) e o osso esponjoso (formado por trabéculas). No osso compacto, na maior extensão encontra-se o sistema de Harvers ou Osteon. Estes sistemas são formados por canais de Harvers, onde se encontram estruturas neurovasculares. Estes canais se intercomunicam com canais perpendiculares chamados canais de Volkman, que trazem a nutrição da superfície para parte interna do osso. Portanto, a estrutura óssea é composta por camadas lamelares externas que abraçam todo o osso e lamelares internas que formam cada sistema de Harvers. Os osteócitos se posicionam dentro do osso em espaços chamados lacunas e os osteoclastos se situam nos canais de reabsorção, onde se concentram em maior proporção os capilares. No osso esponjoso, a função vascular dos canais de Harvers é substituída por vasos sinusoides. Na prática cirúrgica, o conhecimento de todas as estruturas citadas no estudo histológico nos faz entender como os vasos do leito receptor migram pelos canais de Volkmann e canais de Harvers, nutrindo o enxerto e processando o depósito e reabsorção de minerais.
Concluímos que, para integração do enxerto ósseo é importante a técnica cirúrgica precisa e o conhecimento do processo de integração do enxerto por meio da histologia.
MÉTODO
No período de 1986 a 2009, foram realizadas 21 cirurgias envolvendo enxerto ósseo de crânio. Destes casos, 17 (81%) eram de indivíduos do sexo masculino e 4 (19%) do sexo feminino. A idade dos pacientes variou de 22 a 47 anos.
Na nossa casuística, dos 17 pacientes, 16 foram perdas ósseas relacionadas às fraturas frontobasais, e 1 caso de displasia fibrosa óssea da região fronto-orbitária.
Nos 2/3 restantes do crânio, apenas 4 (19%) pacientes apresentaram tumor na região parietal, displasia fibrosa óssea e sequestro ósseo por queimadura.
A fim de desenvolver o tema proposto neste trabalho, tivemos como base quatro casos, nos quais analisamos o pré e pós-operatórios, demonstrando nossos conceitos técnicos cirúrgicos sobre a integração óssea em crânio.
Dentre esses quatro casos, três foram relacionados a traumas por acidentes e um, sobre displasia fibrosa óssea.
Todos os pacientes foram submetidos à avaliação clínica cardiológica e laboratorial, estudo radiológico e alguns à tomografia, sendo estes últimos limitados pela condição econômica do paciente.
O procedimento cirúrgico foi realizado sob anestesia geral, com antibioticoterapia profilática (keflex / cefalexina - 500 mg de 6/6 horas) e com a presença do neurocirurgião no caso de perdas ósseas de maiores proporções. Os casos de grandes perdas ósseas foram encaminhados para a unidade de choque, onde permaneceram por 72 horas, em média.
A via coronal foi utilizada em todos os casos, para colocação do enxerto, com exceção do paciente com queimadura de região posterior do crânio. Realizada antissepsia do couro cabeludo com povidine degermante e fixação dos campos cirúrgicos com nylon 3-0 em pontos separados (Figura 1).
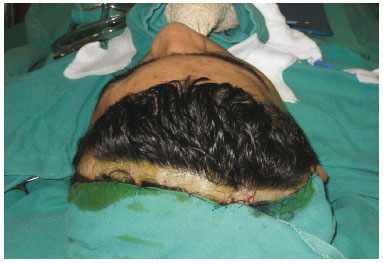
Figura 1 - Preparo do cabelo, colocação de campo cirúrgico e incisão coronal.
Foi infiltrado anestésico local com vasoconstrictor (lidocaína a 0,7% em adrenalina 1: 200,000).
Com relação à área doadora, obtivemos o enxerto do crânio com abordagem coronal, descolando o periósseo nas regiões parietais e frontal (Figura 2).
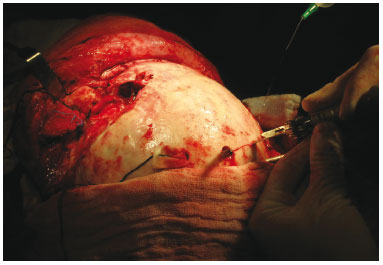
Figura 2 - Descolamento do periósteo.
A área a ser retirada foi demarcada, usando o trépano nos quatro ângulos (Figura 3) do quadrado demarcado no osso parietal, seguido do descolamento da dura-máter (Figura 4). Realizada osteotomia com serra pneumática (Figura 5), retirado o bloco ósseo (Figura 6), separada a díploe com serra pneumática e escopro (Figura 7) e, finalmente, feita a bipartição do osso (Figura 8).
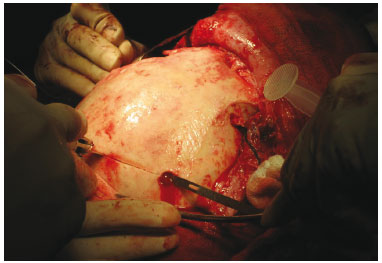
Figura 3 - Demarcação da área doadora.
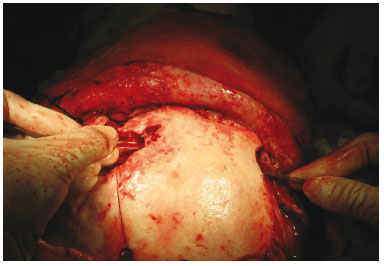
Figura 4 - Descolamento da dura-máter.
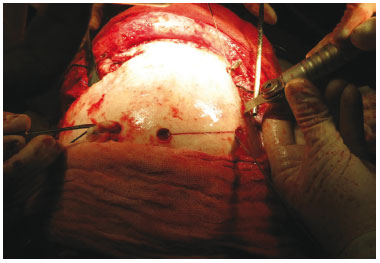
Figura 5 - Osteotomia com serra de Zimmer (pneumática).
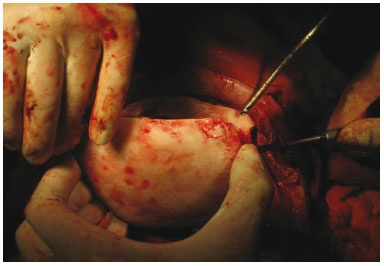
Figura 6 - Retirada do bloco ósseo.
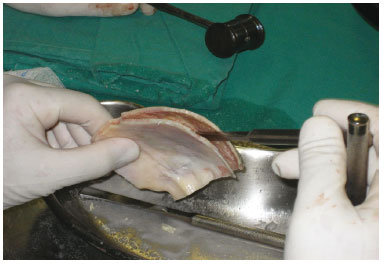
Figura 7 - Bipartição da diploe com serra e escopro.
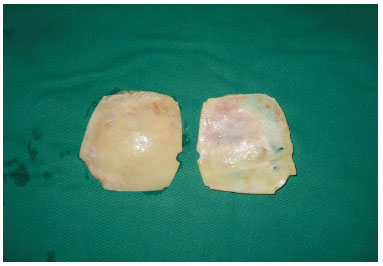
Figura 8 - Osso bipartido.
Para retirada da costela, incisamos ao nível do 7º ou 8º espaço intercostal (Figura 9), descolamos a costela (Figura 10) e ressecamos a mesma numa extensão de aproximadamente 10 cm.
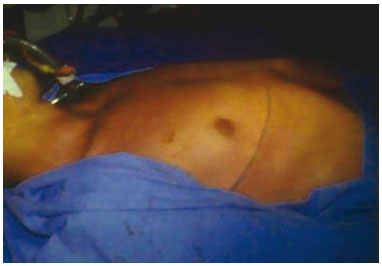
Figura 9 - Incisão ao nível do 7º e 8º espaço intercostal.
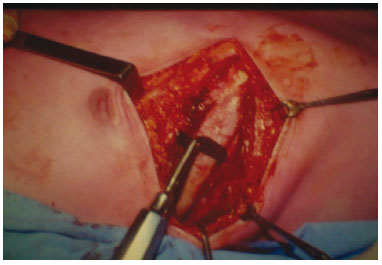
Figura 10 - Descolamento da costela.
Na retirada do osso ilíaco, incisamos a pele um pouco abaixo da crista ilíaca, numa extensão aproximada de 7 cm, com ressecção óssea na parte interna ou externa do osso ilíaco (Figuras 11 e 12).
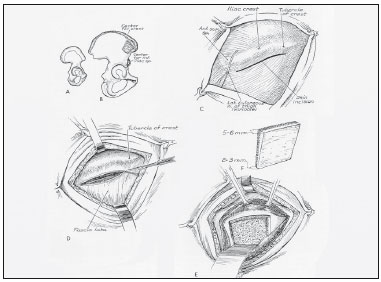
Figura 11 - Retirada do enxerto ósseo do ilíaco.
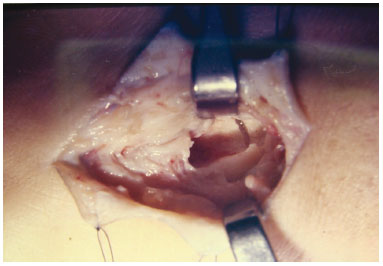
Figura 12 - Retirada do enxerto.
Após a obtenção do enxerto, o mesmo foi colocado na área receptora, obedecendo aos critérios já comentados anteriormente, onde se evidencia primeiramente: 1) preparo do leito receptor com escarificação das bordas para estimular a neoformação de vasos que migrarão para o enxerto; 2) moldagem do enxerto de tal forma que as bordas fiquem bem coaptadas, em todos os lados do leito receptor; 3) fixação rígida com fios de aço ou miniplacas de titânio (Figura 13); 4) cobertura completa de partes ósseas com o próprio couro cabeludo, retalho de vizinhança (Figura 14) ou retalho a distância (free flap). Concluindo, colocamos dreno tubular tipo porto-vac nas áreas doadoras do ilíaco, costela e região parietal (quando retiramos a díploe).
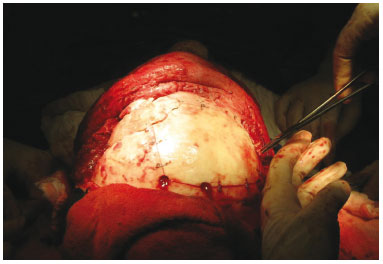
Figura 13 - Fixação rígida com fio de aço.
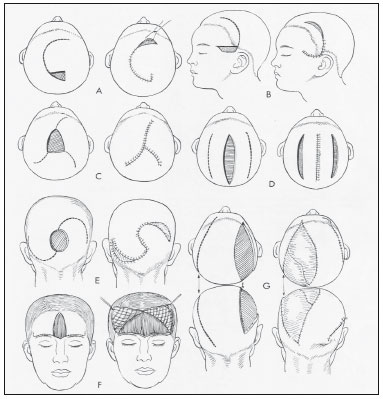
Figura 14 - Tipos de retalhos.
Após todo procedimento de retirada do osso da área doadora e colocado na área receptora, reposicionamos o escalpo e suturamos a derme com Vicryl 4-0 e a pele com Nylon 4-0. O mesmo fazemos na aproximação das partes moles nas áreas doadoras.
Nos casos operados, não tivemos infecção tanto na área doadora, como na área receptora.
Em todos os casos, realizamos antibioticoterapia (keflex/cefalexina 500 mg, de 6/6h, por 8 dias). Orientamos o paciente e os familiares para controle rigoroso de assepsia, alimentação, uso de líquidos para hidratação e suspensão de uso de cigarro.
O resultado estético e funcional foi bem aceito por todos os pacientes, inclusive a não reabsorção óssea.
O acompanhamento ambulatorial variou de 5 a 14 meses, com média de 9,5 meses.
RESULTADOS
Na nossa casuística predominou o sexo masculino (81%).
Dezesseis (75%) pacientes apresentavam traumatismo cranioencefálico, todos decorrentes de acidente automobilístico; 2 (10%) pacientes eram portadores de tumor ósseo, correspondente a displasia fibrosa óssea; 2 (10%) pacientes apresentavam sequela de queimaduras; e 1 (5%) doente era portador de carcinoma espinocelular.
Quanto ao local da lesão, os pacientes apresentavam a seguinte distribuição:
perda óssea de região glabelar anterior - 1 (5%) paciente; perda óssea de região glabelar interna - 1 (5%) paciente; região frontal - 15 (70%) pacientes; região parieto-occipital - 2 (10%) pacientes; região parietal - 2 (10%) pacientes.
Na nossa casuística, não havia nenhum paciente submetido à cirurgia previamente.
Quanto ao local de retirada dos enxertos, observamos:
crânio - 2 (10%) pacientes; costela - 6 (29%) pacientes; ilíaco - 13 (61%) pacientes.
Quanto às vias de acesso para colocação do enxerto, a via coronal foi utilizada em 20 (95%) pacientes e a via parieto-occipital em 1 (5%). No paciente que apresentou osso parieto-occipital à esquerda exposto em mais ou menos 5 x 4 cm, apenas programamos um retalho bipediculado com avanço do mesmo para cobrir o enxerto. A área doadora foi enxertada com pele de espessura parcial sobre o periósteo (usamos o dermátomo de Padgett).
É importante destacar que a via de acesso para a colocação do enxerto no crânio segue a mesma orientação quando da retirada do enxerto de osso parietal.
Para fixação dos enxertos, utilizamos fio de aço (fixação semirígida) em 17 (81%) pacientes e miniplacas e parafusos (fixação rígida) nos demais, ou combinadas em alguns casos.
Neste estudo não houve nenhum caso de absorção óssea ou infecção.
Em todos os pacientes, usamos antibioticoterapia.
DISCUSSÃO
A preocupação pela reparação das perdas ósseas do crânio remonta desde o século XVII, quando um neurocirurgião holandês, sediado em Amsterdam (1687), fez em enxerto heterólogo, retirando o osso do crânio de um cachorro e enxertando em um paciente com perda óssea. Após um período mais ou menos de 1 mês, foi obrigado a retirar o enxerto para não ser excomungado pela igreja.
Na nossa proposta de reparação das perdas ósseas de crânio, optamos, como fonte de obtenção, pelos ossos provenientes da tíbia, ilíaco, costela e crânio (osso parietal). Enfatizamos a utilização dos ossos autólogos como material de eleição para as perdas ósseas do crânio.
Avaliamos as diferentes fontes de obtenção óssea e observamos que a morbidade após a retirada do osso da tíbia, ilíaco e costela é significante menor, quando comparada à obtenção do osso parietal. Na abordagem do osso parietal, a equipe médica deverá estar extremamente treinada, incluindo a presença do neurocirurgião, ser realizada em hospital geral com UTI e preparada para receber complicações graves e ter equipamentos precisos e adequados para se obter bons resultados cirúrgicos. No tocante aos equipamentos cirúrgicos, devemos citar o aparelho hall (serra de Zimmer), as miniplacas e parafusos de titânio, as miniplacas absorvíveis (mais usadas em crianças), os escopros com formas adequadas para retirada do osso no crânio, descoladores para dura-máter, tesouras próprias para cortar o osso (sacabocado), onde com isso se obtém a forma adequada do enxerto para se colocar na área receptora.
Em pesquisa realizada em animais na Universidade de Michigan, nos Estados Unidos, independente da origem embriológica, o osso cortical apresenta menor taxa de absorção que o osso esponjoso. No caso do osso parietal, a retirada para enxerto deve ser feita em pacientes acima dos 11 ou 12 anos, em média. A área mais segura para retirada do enxerto é na região central do osso, onde existe maior espessura (em torno de 0,9 cm). Deve-se afastar da linha sagital superior no mínimo de 2 cm, para evitar lesão do seio sagital superior. Como a maioria dos pacientes é destra, deve-se optar por retirar o enxerto do parietal direito. Quanto à incisão, optamos sempre por incisão coronal, onde podemos abordar a região frontal e parietal simultaneamente. Na área receptora, o enxerto deve estar bem adaptado na forma, para facilitar a fixação, a área receptora deve ser desgastada para haver neovascularização e, assim, nutrir o enxerto.
No nosso estudo, percebemos que a partir da década de 1980, cirurgiões de pontos diferentes do planeta iniciaram simultaneamente a retirada do enxerto do osso parietal, destacando-se, entre outros: Joseph MacCarthy4,5, Sherrel Astone e Charles Thorn6,7, Henry Kawamoto e Anthony Wolfe8,9, nos Estados Unidos, Jorge Psillakis10, Vera Cardim, Zanini e Mélega3, no Brasil, Daniel Marchac e Paul Tessier1, ambos na França, Ortiz Monastério, no México.
Paralelamente ao advento de técnicas cirúrgicas cada vez mais precisas, suporte de anestesia por profissionais preparados e o uso de medicamentos mais eficazes, principalmente os antibióticos, devemos reiterar a aplicação do conhecimento histológico do tecido ósseo, onde o sistema de Havers é citado enfaticamente. Assim, juntando todo este armamentário científico, caminhamos obviamente para obtermos sempre melhores resultados funcionais e estéticos, com menor incidência de complicações possível.
Na nossa casuística e nos demais serviços onde fizemos um estudo comparativo, a grande maioria dos relatos de perda óssea de crânio é decorrente de acidente automobilístico e, no geral, em pessoas jovens, do sexo masculino, na faixa etária mais produtiva, que está entre os 25 e 40 anos. Sabemos ainda que, nos grandes centros, com o aumento populacional significante e também o aumento de números de veículos automotores, as estatísticas devem aumentar exponencialmente.
Finalizando, é gratificante e tranquilizador para a sociedade como um todo ter ciência que o avanço cada vez maior nesta área de cirurgia reparadora caminhará para reduzir as futuras sequelas nestes tipos de traumas e reintegrar os pacientes a sua vida profissional e social, com mínima limitação tanto do ponto de vista funcional como estético.
CONCLUSÃO
Nas reparações das perdas ósseas de crânio, entendemos que a importância do conhecimento da técnica cirúrgica e o uso de material especializado, aliado ao conhecimento do processo de integração do enxerto na área receptora, através do entendimento claro como este procedimento do ponto de vista histológico se concretiza, nos leva a ter um controle quase total desta indicação cirúrgica, evitando desta forma os sequestros ósseos.
Nossas fontes de enxerto através do ilíaco, costela e crânio (osso parietal) nos levaram a uma flexibilidade de opções. Consideramos que o osso proveniente do crânio tem melhor integração, facilidade de manuseio e mais estabilidade na fixação rígida, obviamente por causa da mesma origem embriológica, apesar de que, em nossa casuística, usamos em maior proporção o osso ilíaco e a costela como enxertos.
Nos nossos pacientes, chegamos aos dois principais objetivos: proteção da massa encefálica e bons contornos estéticos.
REFERÊNCIAS
1. Tessier P, Kawamoto H, Posnick J, Raulo Y, Tulasne JF, Wolfe SA. Complications of harvesting autogenous bone grafts: a group experience of 20,000 cases. Plast Reconstr Surg. 2005;116(5 Suppl):72S-3.
2. Longacre JJ, Converse JM, Knize DM. Transplantation of bone. In: Converse JM, ed. Reconstructive plastic surgery. 2nd ed. Philadelphia:WB Saunders;1977. p.313-39.
3. Zanini SA, Psillakis JM. A face e a calota craniana como área doadora de enxertos ósseos. In: Psillakis JM, Zanini AS, Mélega JM, Costa EA, Cruz RL, eds. Cirurgia craniomaxilofacial: osteotomias estéticas da face. Rio de Janeiro:Medsi;1987. p.89-91.
4. McCarthy JG, Thorne CHM, Wood-Smith D. Principles of craniofacial surgery: orbital hypertelorism. In: McCarthy J, ed. Plastic surgery. vol. 4. Philadelphia:WB Saunders;1990. p.2974-3011.
5. McCarthy JG, Zide BM. The spectrum of calvarial bone grafting: introduction of the vascularized calvarial bone flap. Plast Reconstr Surg. 1984;74(1):10-8.
6. Lee WP, Butler PE. Transplant biology and applications to plastic surgery. In: Aston SJ, Beasley RW, Thorne CHM, eds. Grabb and Smith's plastic surgery. Philadelphia: Lippincott-Raven;1997. p.27-37.
7. Freund RM. Scalp, calvarium and forehead reconstruction. In: Aston SJ, Beasley RW, Thorne CHM, eds. Grabb and Smith's plastic surgery. Philadelphia: Lippincott-Raven;1997. p.473-82.
8. Tessier P, Kawamoto H, Matthews D, Posnick J, Raulo Y, Tulasne JF, et al. Autogenous bone grafts and bone substitutes: tools and techniques: I. A 20,000-case experience in maxillofacial and craniofacial surgery. Plast Reconstr Surg. 2005;116(5 Suppl):6S-24S.
9. Tessier P, Kawamoto H, Matthews D, Posnick J, Raulo Y, Tulasne JF, et al. Taking bone grafts from the anterior and posterior ilium: tools and techniques: II. A 6800-case experience in maxillofacial and craniofacial surgery. Plast Reconstr Surg. 2005;116(5 Suppl):25S-37S.
10. Psillakis JM, Nocchi VL, Zanini SA. Repair of large defect of frontal bone with free graft of outer table of parietal bones. Plast Reconstr Surg. 1979;64(6):827-30.
1. Cirurgião plástico, Coordenador de equipe da Beneficência Portuguesa de São Paulo, São Paulo, SP, Brasil. Membro da Sociedade Brasileira de Cirurgia Plástica (SBCP).
2. Cirurgião plástico da Beneficência Portuguesa de São Paulo, São Paulo, SP, Brasil. Membro da Sociedade Brasileira de Cirurgia SBCP.
3. Médico estagiário da Clínica de Cirurgia Plástica Dr Antonio Macedo, São Paulo, SP, Brasil.
Correspondência para:
Antonio Macedo Filho
Av. Agami, 323 - Moema
São Paulo, SP, Brasil - CEP 04522-001
E-mail: docmacedo@uol.com.br
Artigo submetido pelo SGP (Sistema de Gestão de Publicações) da RBCP.
Artigo recebido: 7/7/2010
Artigo aceito: 25/11/2010
Trabalho realizado no Hospital Beneficência Portuguesa de São Paulo, São Paulo, SP, Brasil.
Trabalho Vencedor do Prêmio Nemer Chidid 2010.


 Read in Portuguese
Read in Portuguese
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter