

Case Reports - Year 2008 - Volume 23 -
Injeção Ilícita de Silicone Líquido: Revisão de Literatura a Propósito de Dois Casos de Necrose de Mamas
Illicit Injection of Liquid Silicon: Literature Review Concerning Two Cases of Breast Necrosis
RESUMO
O silicone líquido foi introduzido no início do século XX com finalidade estética e reparadora, teve seu apogeu no Japão, na década de 1950, e logo após apareceram as primeiras publicações das reações adversas e suas complicações, principalmente com a prática de injeção ilícita dessa substância por pessoas não qualificadas. Este trabalho tem finalidade de realizar uma revisão bibliográfica sobre os efeitos da injeção de silicone líquido a propósito de casos de necrose de mamas.
Palavras-chave: Doenças mamárias/induzido quimicamente. Silicones/efeitos adversos. Injeções subcutâneas/adverse effects. Óleos de silicone/adverse effects.
ABSTRACT
The liquid silicon was introduced begin in the XX's century with aesthetic and reparative purpose, had its acme in Japan, in the decade of 1950, and soon after they appeared the first publications of the adverse reactions and their complications, mainly with the practice of illicit injection of that nourishes for unqualified people. This work has purpose of accomplishing a bibliographical revision on the effects of the injection of liquid silicon concerning cases of necrosis of breast.
Keywords: Breast diseases/chemically induced. Silicones/adverse effects. Injections, subcutaneous/adverse effects. Silicone oils/adverse effects.
Ao longo dos anos tem-se utilizado múltiplos elementos e técnicas tanto para a reconstrução como para o delineamento e correção do contorno corporal. Em 1900, Gersuny introduziu o uso de injeções de parafina para aumento de volume mamário, no entanto, esta técnica foi abandonada devido às diversas complicações1,2.
Em 1930, iniciou-se a indústria do silicone na sede da Corning Glass Works e no Instituto Mellon3. Dezoito anos mais tarde, Rowe, Spencer e Bass estudaram a toxicologia dos silicones, e Barondes, em 1950, revisou seu emprego na medicina e, em 1953, Brown utiliza estes fluidos pela primeira vez em Cirurgia Plástica4,5.
A partir da década de setenta, quando Andrews et al.6 publicaram um trabalho mostrando pela primeira vez as reações adversas em seres humanos, incluindo desde complicações locais até acometimento de órgãos à distância, esse tipo de material teve o seu uso suspenso pelo FDA americano e pela DIMED no Brasil2,3,7.
A gravidade das complicações e a dificuldade de resposta terapêutica motivaram os autores a elaborar o presente estudo, que objetiva relatar os danos causados pela aplicação de silicone líquido de forma clandestina, a abordagem terapêutica utilizada e a evolução clínica apresentada pelos pacientes.
RELATO DOS CASOS
No Serviço de Cirurgia Plástica do Hospital de Base de São José do Rio Preto, no ano de 2004, foram atendidos dois casos de pacientes do sexo masculino com idade de 16 anos e 18 anos, profissionais do sexo, apresentando as primeiras complicações decorrentes da aplicação de silicone líquido em região mamária, realizada de forma clandestina, por pessoa não habilitada.
Paciente 1 M.H.M., 16 anos, admitido no serviço de emergência com história de injeção de silicone líquido em mamas, há 5 dias, com febre, taquicardia, sinais flogísticos localizados e área de epidermólise mamária (Figura 1A). Apresentava leucocitose, hemocultura com Stafilococcos coagulase negativo, e bioquímica normal. Administrado Clindamicina associado Amicacina, curativos e foi transferido para UTI. Cultura evidenciou Pseudomonas aeruginosa, e aos antibióticos associou-se Oxacilina e Flagyl®. O laudo anatomopatológico do desbridamento foi: "processo inflamatório agudo exsudativo e necrosante com abscessos focais periféricos e extensa esteatonecrose do tecido mamário" (Figura 1B). Indicada Câmara Hiperbárica que foi recusada pelo paciente. Foi transfundido com concentrado de Hemáceas. Evoluiu com elevação do Clearence de creatinina e Urina I ácida (pH= 5,5), proteínuria, sem bacteriúria e com leucocitúria. Apresentou, ainda, elevação da TGO, da Fosfatase alcalina, e Gama GT. A radiografia de tórax apontou: "Redução da transparência pulmonar por processo intersticial bilateralmente. Opacidade periférica com base pleural em campo médio hemitórax direito", sem alterações no exame do escarro (Figura 1C). Realizaram-se curativos seqüenciais inicialmente utilizando papaína gel a 3% e, posteriormente, com Ácido Graxo Essencial (AGE), evoluindo com melhora clínica e laboratorial, finalizando com diminuição da área cruenta das mamas, o que resultou na alta hospitalar após 45 dias de internação. Aproximadamente 7 dias após a alta e já com área granulada, recebeu enxertia de pele total (Figura 1D). Este paciente perdeu o seguimento após a retirada do curativo do enxerto.
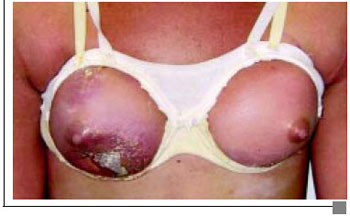
Figura 1A - Admissão do paciente com o aparato nas mamas.
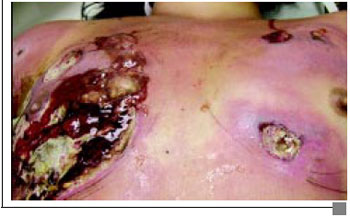
Figura 1B - Aspecto da necrose das mamas.
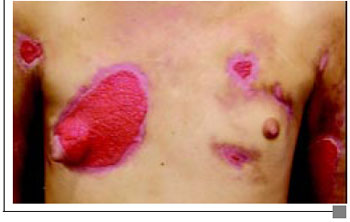
Figura 1C - Linfoadenomegalia cervical e feridas granuladas.

Figura 1D - Pós-enxertia de pele com curativo de Brown.
Paciente 2 E.R.C., 18 anos, admitido com sinais flogísticos localizados nas áreas das mamas predominantemente à direita, com epidermólise evidente, febril e toxemiado (Figura 2A). Apresentava leucocitose, Hemocultura negativa e Bioquímica normal. Iniciado Clindamicina associada Amicacina, curativos e transferido para UTI. Evolui com extensa necrose das áreas injetadas que necessitaram de quatro desbridamentos, sendo o primeiro imediatamente após o equilíbrio do estado geral. Todas as culturas solicitadas foram negativas. O laudo Anatomopatológico foi semelhante ao caso do paciente 1. Submetido a Câmara Hiperbárica: 20 sessões, 1 vez ao dia, 5 dias por semana, durante o período de internação. Foi submetido à drenagem de abscessos cervical e torácico (Figura 2B). Sem alterações renais, radiografia de tórax normal e escarro sem alterações. Paciente recebeu transfusão de 3 UI de Concentrado globular. Observou-se uma melhora clínica e das características das feridas mais precocemente que o paciente do caso 1 (Figura 2C). Realizados enxertia de pele total para cobrir área cruenta de região mamária direita e reposicionamento do CAM (Figura 2D).
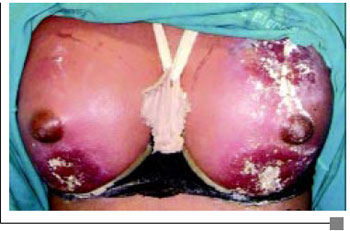
Figura 2A - Presença de epidermólise e sinais flogísticos.
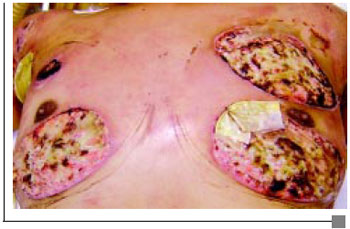
Figura 2B - Necrose e abscessos em tórax.
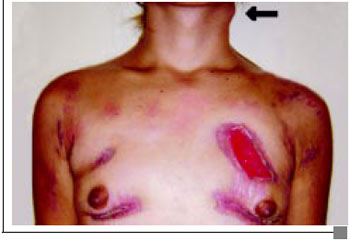
Figura 2C - Aspecto pré-enxertia.
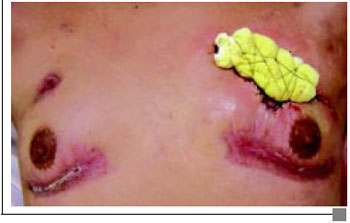
Figura 2D - Aspecto pós-enxertia de pele e reposicionamento do CAP.
DISCUSSÃO
No início do século XX, a injeção de óleos e outros líquidos para modelagem corporal com fins estéticos era feita por esteticistas, com conseqüências desastrosas, tanto que Heidingsfeld, em 1906, concluiu que essas complicações resultavam da ausência de técnicas adequadas e de impurezas no material injetado1,2. Da mesma forma, os pacientes descritos relataram o uso de silicone líquido, acondicionado em vidros sem condições de higiene, provavelmente adicionado de outros óleos, e injetado no tecido mamário por pessoa não preparada e sem assepsia.
Dentre as complicações apresentadas pela injeção do silicone líquido está uma série de reações inflamatórias, resultando em processos fibróticos que, na realidade, seriam necessários para conter o líquido, evitando a migração2,3, e por esse motivo nossos pacientes foram admitidos com um acessório no formato de um sutiã, o qual deveria permanecer por certo período, moldando o processo fibrótico e retendo o silicone nas mamas.
A evolução rápida para ulceração das áreas acometidas nos dois casos foi atípica e, provavelmente, potencializada pela infecção. Na literatura, o estudo encontrado com maior casuística é o de Milojevic5, na Iugoslávia, que relatou complicações, como migração, fibroses e granulomas, e não mencionou ulceração, diferente de Kubota et al7., que encontraram 2% de ulcerações. Estas, além de incomuns, têm um período de latência grande que, na sua maioria, corresponde a processo inflamatório de corpo estranho recidivante5,6,8. O aparecimento do quadro agudo necrotizante no local injetado, como o apresentado no presente estudo, não é o usual, pois a maioria dos trabalhos refere período mínimo de 4 semanas para o início da sintomatologia4,5.
A reação tecidual ao material injetado, assinalada pelo exame anatomopatológico das peças cirúrgicas obtidas, mostrou processo inflamatório agudo, o que também é incomum, de acordo com os autores estudados4,5,6, que encontraram processo inflamatório crônico.
Observamos a impregnação dos tecidos perimamários com deslocamento gravitacional do material para o dorso, braços e região cervical, e abscesso cervical e braquial por migração do material, o que seria uma das complicações já relatada8. Os pacientes apresentaram também acometimento de Iinfonodos cervicais, ambos os casos, concordando com a literatura, que relata linfadenopatia axilar após injeção de silicone líquido8,9.
Elevações das transaminases decorrentes de um provável acometimento hepático sem repercussões clínicas foram observadas no paciente 1, que melhorou e não foram necessárias biópsias e demais investigações, mesmo porque complicações hepáticas do silicone não são comuns5,10. Ellenbogen et al.9 descreveram complicações sistêmicas em paciente submetido a tal prática, com aumento das enzimas hepáticas, biópsia hepática mostrando células gigantes multinucleadas, contendo vacúolos formados por silicone em seu interior, a qual denominou de hepatite granulomatosa.
Quanto às alterações das provas de função renal, observadas no primeiro paciente, estas vão de encontro com os achados de Andrews et al.6, que relataram embolia por silicone em glomérulos renais, sugerindo transporte por via sangüínea.
Ainda referente às complicações, há relatos de dispnéia após o uso de silicones e de pneumonite aguda e crônica12, sendo que os pacientes dessas amostras evoluíram com taquipnéia, dispnéia, febre, infiltrado pulmonar à radiografia, e presença de silicone em espécimes de lavado broncoalveolar. O que ocorreu com apenas um dos pacientes desse relato, porém sem alterações no escarro.
A conduta cirúrgica adotada de repetidos desbridamentos, tentando preservar os tecidos adjacentes, foi necessária, pois se tratava de um processo necrotizante e infeccioso. A antibioticoterapia e a corticoterapia foram iniciadas, já que sofreram uma rápida deterioração tecidual, inclusive com repercussões inflamatórias e hemodinâmicas10,11. Há controvérsias quanto à conduta nos quadros crônicos, observando-se até mesmo casos de mastectomias subcutâneas para tratamento das complicações dessas injeções13. No entanto, existem opções mais conservadoras, como a correção por aspiração ultra-sônica do silicone associada à reconstrução das mamas com prótese de silicone, como realizado por Zadhi14 em paciente do sexo feminino e sem infecção aguda. Nossos pacientes foram submetidos à enxertia de pele e reposionamento do CAM, que fora preservado durante os consecutivos desbridamentos cirúrgicos.
Foi realizada oxigenoterapia hiperbárica no paciente 2, que evoluiu melhor. Não encontramos relatos na literatura da associação de câmara hiperbárica nesses casos, porém a sua utilização em cicatrização de lesões crônicas e agudas já foi relatada com bons resultados15.
CONCLUSÃO
O silicone líquido deve ser contra-indicado para aumento de volumes, quanto mais realizado por leigos sem cuidados de técnicas clássicas de antissepsia ou, ainda, em associação com outros produtos.
As conseqüências são locais, com infecção, fibrose e reações tipo corpo estranho, podendo ainda ser regionais, por difusão aos tecidos periféricos ou migração linfática até os gânglios, drenagem venosa e, finalmente, migração pelo efeito gravitacional, sendo que na vigência de uma infecção aguda são necessários drenagem e desbridamento imediatos, minimizando os outros efeitos posteriores.
Como houve uma evolução discretamente mais favorável das áreas cruentas no paciente submetido à oxigenoterapia hiperbárica, sugere-se mais estudos que comprovem este efeito.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Gutierrez CL, Montes AA. Siliconomas: caso clínico. Rev Med Chile. 2002,130(7):793-7.
2. Matton G, Anseeuw A, De Keyser F. The history of injectable biomaterials and the biology of collagen. Aesthetic Plast Surg. 1985;9(2):133-40.
3. Pereira WJB. Biomateriais em cirurgia plástica. In: Mélega JM, ed. Cirurgia plástica reparadora e estética. Rio de Janeiro: Medsi; 2002. p.167-75.
4. Gemperli R, Alonso N, Lodovici O, Pigossi N. Estudo clínico das reações sistêmicas e locais ao uso indevido do silicone líquido e/ou óleo mineral. Rev Hosp Fac Med S Paulo. 1984;39(4):158-62.
5. Milojevic B. Complications after silicone injection therapy in aesthetic plastic surgery. Aesthetic Plast Surg. 1982;6(4):203-6.
6. Andrews JM, Haddad CM, Ramos RR, Martins DMFS, Ferreira LM. Morbidade e mortalidade após injeção de silicone líquido em seres humanos. A Folha Médica. 1989;99(2), agosto.
7. Kubota J, Fujino T, Abe T. Long term complications caused by injected silicone gel and paraffin oil. Keio J Med. 1984;33(3):127-36.
8. Delage C, Shane JJ, Johnson FB. Mammary silicone granuloma. Migration of silicone fluid to abdominal wall and inguinal region. Arch Dermatol. 1973;108(1):105-7.
9. Ellenbogen R, Rubin L. Injectable fluid silicone therapy. Human morbidity and mortality. JAMA. 1975;234(3):308-9.
10. Hage JJ, Kanhai RC, Oen AL, van Diest PJ, Karim RB. The devastating outcome of massive subcutaneous injection of highly viscous fluids in male-to-female transsexuals. Plast Reconstr Surg. 2001;107(3):734-41.
11. Ben-Hur N, Rees TD, Ballantyne DL Jr. Behavior of liquid silicones (dimethylpolysiloxane silicone liquid of 350 centistoke viscosity) injected into animals. Ann Chir Plast. 1967;12(3):243-6.
12. Chastre J, Brun P, Soler P, Basset F, Trouillet JL, Fagon JY, Gibert C, et al. Acute and latent pneumonitis after subcutaneous injections of silicone in transsexual men. Am Rev Respir Dis. 1987;135(1):236-40.
13. Ortiz-Monasterio F, Trigos I. Management of patients with complications from injections of foreign materials into the breasts. Plast Reconstr Surg. 1972;50(1):42-7.
14. Zandi I. Failure to remove soft tissue injected with liquid silicone with use of suction and honesty in scientific medical reports. Plast Reconstr Surg. 2000;105(4):1555-8.
15. D'Agostinho OM. Aplicações clínicas do oxigênio hiperbárico. Diag Trat. 2001;6(1):7-10.
I. Membros Especialistas da S.B.C.P., Ex-residentes do Serviço de Cirurgia Plástica do Hospital de Base da Faculdade de Medicina de São José do Rio Preto, SP.
II. Residente do Serviço de Cirurgia Plástica do Hospital de Base da Faculdade de Medicina de São José do Rio Preto, SP.
III. Professor Doutor em Cirurgia Plástica pela UNIFESP, Membro Titular da S.B.C.P. e Chefe do Serviço de Cirurgia Plástica do Hospital de Base da Faculdade de
Medicina de São José do Rio Preto, SP.
Correspondência para:
Clínica Imagem de Cirurgia Plástica
Av. José Munia, 7075 CEP: 15085-350
São José do Rio Preto/SP
Telefax: (xx)17 3355-9200
Trabalho realizado no Serviço de Cirurgia Plástica do Hospital de Base da Faculdade de Medicina de São José do Rio Preto, SP.
Apoio: CEPlástica - Centro de Estudos em Cirurgia Plástica do Hospital de Base da Faculdade de Medicina de São José do Rio Preto, SP.
Artigo recebido: 24/09/2007
Artigo aprovado: 22/01/2008


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter