

Review Article - Year 2024 - Volume 39 -
Os riscos do polimetilmetacrilato: Revisão integrativa de 587 casos de complicações
The Risks of Polymethyl Methacrylate: An Integrative Review of 587 Complication Reports
RESUMO
Introdução A demanda por procedimentos estéticos minimamente invasivos impulsionou o uso do polimetilmetacrilato (PMMA) como preenchimento dérmico, que a princípio foi aprovado para lipodistrofias relacionadas ao vírus da imunodeficiência humana (HIV - human immunodeficiency virus, em inglês). Seu uso inadequado causa graves complicações, como inflamações, migração do material, infecções e repercussões sistêmicas. Nesta revisão, objetivamos realizar uma investigação sobre esses riscos e complicações relatadas na literatura nos últimos 20 anos.
Materiais e Métodos Realizamos uma revisão integrativa de estudos descritivos sobre complicações do PMMA publicados entre 2004 e 2024, utilizando as bases de dados PubMed, Scientific Electronic Library Online (SciELO) e Scopus. Foram analisados 38 estudos, totalizando 587 casos, e foram excluídos artigos publicados fora do período analisado ou que não atendiam aos critérios de inclusão.
Resultados Encontramos 587 casos de complicações associadas ao PMMA, sendo que 64% deles ocorreram no Brasil. O sítio mais frequente foi a região malar, seguido do sulco nasogeniano, da região glútea, e dos lábios. As complicações variaram entre imediatas e tardias, e de repercussões simples a mais severas. As mais frequentes foram: eritema (26%), prurido (16%), edema (11%), granulomas (21%), nodulações (14%) e alterações cutâneas (8%), incluindo casos graves de insuficiência renal, hipercalcemia, choque séptico, infecções e necrose de tecido. A quantidade injetada de material variou de 1,9 a 900 mL, e, no que tange ao tratamento, houve predominância de esteroides, antibióticos e necessidade de abordagem cirúrgica, com realização de excisões, drenagem de abscesso e desbridamento.
Conclusão Preenchimentos com PMMA estão associados a complicações graves, e seu uso muitas vezes não está relacionado à correção de lipodistrofias por HIV. O material tem riscos significativos, incluindo complicações sistêmicas, com a necessidade de remoção cirúrgica.
Palavras-chave: polimetilmetacrilato; preenchedores dérmicos; relatos de casos; revisão; risco
ABSTRACT
Introduction The demand for minimally-invasive esthetic procedures has boosted the use of polymethyl methacrylate (PMMA) as a dermal filler, which was initially approved for human immunodeficiency virus (HIV)-related lipodystrophies. Improper PMMA use can lead to severe complications, including inflammation, material migration, infections, and systemic repercussions. The present review investigated PMMA-related risks and complications reported in the literature over the past 20 years.
Materials and Methods We conducted an integrative review of descriptive studies on PMMA complications published from 2004 to 2024 and retrieved from PubMed, Scientific Electronic Library Online (SciELO), and Scopus. We analyzed 38 studies, encompassing 587 cases, and excluded articles published outside the specified period and those not meeting the inclusion criteria.
Results We identified 587 cases of PMMA-related complications, 64% of them occurring in Brazil. The most common complication site was the malar region followed by the nasolabial fold, the gluteal area, and the lips. The complications ranged from immediate to delayed, and from mild to severe. The most frequent complications included erythema (26%), pruritus (16%), edema (11%), granulomas (21%), nodules (14%), and skin changes (8%). Severe cases included renal failure, hypercalcemia, septic shock, infections, and tissue necrosis. The volume injected ranged from 1.9 to 900mL. The treatment predominantly involved steroids, antibiotics, and surgical interventions, including excisions, abscess drainage, and debridement.
Conclusion The use of PMMA fillers may lead to severe complications, often unrelated to the correction of HIV-related lipodystrophies; PMMA presents significant risks, including systemic complications, requiring surgical removal.
Keywords: case reports; dermal fillers; polymethyl methacrylate; review; risk
Introdução
A demanda por procedimentos estéticos minimamente invasivos que prometem resultados eficientes, satisfatórios e com curto tempo de recuperação tem aumentado nos últimos anos.1 Procedimentos cosméticos como os preenchimentos dérmicos e volumizadores faciais e corporais emergiram como alternativas populares à cirurgia plástica convencional, com a promessa de rápida recuperação e a falsa sensação de menores riscos associados, o que vai ao encontro das expectativas dos pacientes.2
Nesse contexto , um tipo de preenchedor muito utilizado é o polimetilmetacrilato (PMMA), um componente plástico, inabsorvível, cujas esferas são inseridas em um veículo para permitir a aplicação por meio de injeções.3 O PMMA foi inicialmente liberado para uso em nível ambulatorial no Brasil em 2009 pelo Ministério da Saúde, para o tratamento das lipodistrofias secundárias aos efeitos adversos dos antirretrovirais utilizados no tratamento do HIV.4,5 No entanto, com o passar dos anos, o uso indiscriminado e inadequado desse material resultou em inúmeras complicações, tanto imediatas quanto tardias.3
As complicações imediatas do PMMA incluem reações inflamatórias, dor e infecções que ocorrem logo após a aplicação. Tais alterações podem variar de reações adversas menores, como eritema e edema, até efeitos adversos mais graves, como necroses teciduais, acometimentos oculares, infecções severas e, até mesmo, insuficiência renal por hipercalcemia.5-7 As complicações agudas podem persistir e evoluir para formações granulomatosas, infecções recorrentes, doenças autoimunes e insuficiência renal crônica. Além disso, a migração do material para áreas indesejadas pode resultar em assimetrias e deformidades locais muitos anos após a sua aplicação.8
Por ser inabsorvível, a interação do PMMA com o tecido adjacente não permite que o material possa ser removido isoladamente. O caráter irreversível da aplicação do produto é um dos seus maiores limitantes.3,5,8 A irreversibilidade do PMMA pode resultar no aparecimento de complicações tardias de tratamento complexo e que, em muitos casos, evoluem com deformidades permanentes. Diante de complicações como a presença de granulomas, reação inflamatória crônica, fibrose e infecções com formação de biofilme bacteriano, a única alternativa terapêutica é a remoção cirúrgica do produto, juntamente com o tecido saudável adjacente, resultando em sequelas permanentes.5,8
Essas reações podem ser intensificadas por técnicas inapropriadas de aplicação, indicações questionáveis, volumes inadequados de produto para a área alvo de tratamento ou por uma má seleção na qualidade dos materiais utilizados. Estudos6 mostram que o procedimento deve ser realizado por cirurgiões plásticos ou dermatologistas qualificados que compreendam a anatomia da área a ser tratada, dominem a técnica correta e saibam tratar as eventuais complicações; porém, essas recomendações muitas vezes não são levadas em consideração.
Em vista desse cenário, faz-se necessária uma ampla investigação na literatura médica, a fim de compilar as evidências científicas disponíveis sobre o PMMA, para determinar quais são as possíveis complicações imediatas e tardias decorrentes do seu uso, a fim de aumentar a compreensão sobre a segurança desse material para fins estéticos e até mesmo questionar a liberação do uso dessa substância pelos órgãos competentes.
Objetivo
O objetivo deste trabalho é realizar uma revisão integrativa dos casos de complicações imediatas e tardias decorrentes do uso de PPMA relatados na literatura nos últimos 20 anos.
Materiais e Métodos
Trata-se de uma revisão integrativa da literatura contemplando relatos de caso e séries de casos sobre complicações imediatas e tardias do PMMA. Foi realizada uma pesquisa por artigos publicados 2004 e 2024 nas bases de dados PubMed, Scientific Electronic Library Online (SciELO) e Scopus, utilizando os descritores polimetilmetacrilato, preenchedores dérmicos e complicações.
Foram excluídos estudos publicados fora do período estipulado, estudos experimentais e aqueles não realizados com humanos. Os estudos que preencheram os critérios de inclusão foram lidos integralmente por dois revisores independentes, e, em caso de conflito, um terceiro pesquisador resolveu a discrepância.
Na leitura dos artigos, os seguintes dados foram coletados: nome da revista, autor, ano, país de origem, tipo de estudo (relato de caso ou série de casos), casuística, idade, profissional que realizou o procedimento (médico ou não médico), volume injetado, sítio anatômico tratado, sinais e sintomas apresentados após a injeção do PMMA, complicações imediatas, complicações tardias, tratamento das complicações, e se o preenchimento foi realizado no contexto do tratamento da lipodistrofia secundária à infecção por HIV ou com fins estéticos.
Resultados
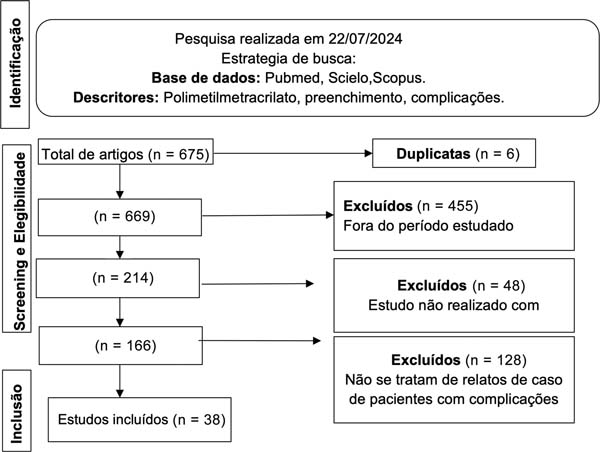
Ao todo, 38 estudos preencheram os critérios de inclusão dessa revisão, totalizando 587 casos (►Fig. 1): 17 artigos eram séries de casos e 21, relatos de casos individuais (►Tabela 1);9-43 39% dos artigos (15/38) relatavam casos que ocorreram no Brasil, sendo o relato mais antigo5 publicado em 2008, e o mais recente,9 em 2024 (►Tabela 2).
| Revista | Autores | Ano | Casuística | Referência |
|---|---|---|---|---|
| Revista Brasileira de Cirurgia Plástica | Goldman et al. | 2024 | 209 | 9 |
| Annals of Plastic Surgery | Durkin et al. | 2023 | 3 | 10 |
| Journal of the American Academy of Dermatology | Vengalil et al. | 2023 | 1 | 11 |
| Cytopathology | Saoud et al. | 2023 | 1 | 12 |
| Ophthalmic Plastic and Reconstructive Surgery | Parikh et al. | 2023 | 1 | 13 |
| Journal of Cutaneous and Aesthetic Surgery | Sivam et al. | 2023 | 1 | 14 |
| Journal of Drugs in Dermatology | Goldman et al. | 2021 | 27 | 15 |
| SKIN The Journal of Cutaneous Medicine | Dhaliwal et al. | 2021 | 1 | 16 |
| European Review for Medical and Pharmacological Sciences | Freire de Carvalho et al. | 2021 | 1 | 17 |
| Annals of Medicine and Surgery | Alimoradi et al. | 2021 | 1 | 18 |
| Jornal Brasileiro de Nefrologia | Manfro et al. | 2021 | 2 | 7 |
| Revista Brasileira de Cirurgia Plástica | Kurimori et al. | 2019 | 1 | 3 |
| Dermatologic Therapy | Goldman e Wollina | 2019 | 2 | 19 |
| Dermatologic Surgery | Ibrahim e Dover | 2018 | 1 | 20 |
| Georgian Medical News | Goldman et al. | 2018 | 2 | 21 |
| Open Access Macedonian Journal of Medical Sciences | Goldman e Wollina | 2018 | 81 | 22 |
| Contact Dermatitis | Shah et al. | 2017 | 1 | 23 |
| Revista Brasileira de Cirurgia Plástica | Souza et al. | 2016 | 1 | 24 |
| Diagnostic Pathology | Cannata-Ortiz et al. | 2016 | 1 | 25 |
| Aesthetic Surgery Journal | Limongi et al. | 2016 | 11 | 26 |
| Plastic Reconstructive Surgery - Global Open | Purnell et al | 2016 | 1 | 27 |
| Journal of Cosmetic and Laser Therapy | Friedmann et al. | 2016 | 4 | 28 |
| Medicina Intensiva | Boattini et al. | 2015 | 1 | 29 |
| Calcified Tissue International | Hindi et al. | 2015 | 1 | 30 |
| Skin Research and Technology | Cinotti et al. | 2015 | 1 | 31 |
| Archives of Endocrinology and Metabolism | Rados e Furlanetto | 2015 | 1 | 32 |
| Clinical Cases in Mineral and Bone Metabolism | Negri et al. | 2014 | 4 | 33 |
| Journal of the American Geriatrics Society | Costa et al. | 2014 | 1 | 34 |
| Aesthetic Plastic Surgery | Park et al. | 2012 | 13 | 35 |
| Journal of Plastic, Reconstructive & Aesthetic Surgery | Park et al. | 2012 | 15 | 36 |
| The Canadian Journal of Plastic Surgery | Solomon et al. | 2012 | 153 | 37 |
| Journal of Hand Surgery | Al-Qattan | 2011 | 3 | 38 |
| Journal of Plastic, Reconstructive & Aesthetic Surgery | Santana et al. | 2010 | 1 | 39 |
| Aesthetic Plastic Surgery | de Figueiredo et al. | 2010 | 1 | 40 |
| Kosmetische Medizin | Wollina | 2009 | 1 | 41 |
| Plastic and Reconstructive Surgery | Salles et al. | 2008 | 32 | 5 |
| Dermatology | Wolfram et al. | 2006 | 4 | 42 |
| Clinical and Experimental Dermatology | Sidwell et al. | 2006 | 1 | 43 |
| Total | 587 | |||
| Autor | Ano | Número de casos | Referência |
|---|---|---|---|
| Goldman et al. | 2024 | 209 | 9 |
| Goldman et al. | 2021 | 27 | 15 |
| Freire de Carvalho | 2021 | 1 | 17 |
| Manfro et al. | 2021 | 2 | 7 |
| Kurimori et al. | 2019 | 1 | 3 |
| Goldman e Wollina | 2019 | 2 | 19 |
| Goldman A et al. | 2018 | 2 | 21 |
| Goldman e Wollina | 2018 | 81 | 22 |
| Souza et al. | 2016 | 1 | 24 |
| Limongi et al. | 2016 | 11 | 26 |
| Rados e Furlanetto | 2015 | 1 | 32 |
| Costa et al. | 2014 | 1 | 34 |
| Santana et al. | 2010 | 1 | 39 |
| de Figueiredo J et al. | 2010 | 1 | 40 |
| Salles et al. | 2008 | 32 | 5 |
| Total | 373 | ||
Regiões Anatômicas e Volume Injetado
O sítio de preenchimento mais frequente foi o malar, seguido do sulco nasogeniano, da região glútea, dos lábios, da região nasal, da região frontal, da face, da região palpebral, da região zigomática, dos membros superiores, do mento, da mandíbula, do tórax, do tronco, dos membros inferiores e das regiões temporal, auricular e peniana (►Tabela 3). Somente 2 (5%) estudos relatavam casos de preenchimento com finalidade reconstrutora para o tratamento da lipodistrofia decorrente do uso de antirretroviral.30,33 A maioria dos estudos (89,4%) não informou o volume injetado durante o procedimento; contudo, foram registradas quantidades como 1,9 mL em região palpebral em 1 paciente,10 4 mL para tratamento facial,17 e 2 casos de injeção de 400mL e 900mL de PMMA para preenchimento glúteo.3,27
| Região anatômica | Número de estudos (porcentagem) | Referência |
|---|---|---|
| Malar | 12 (0.13) | 5,9,11,13,14,19,20,28,35,39,42,43 |
| Sulco nasogeniano | 11 (0.12) | 9,20,24,28,31,35,37,39-42 |
| Glúteo | 10 (0.11) | 3,5,7,18,21,27,29,30,32,33 |
| Nariz | 8 (0.09) | 5,9,15,19,23,28,37,40 |
| Frontal | 8 (0.09) | 5,9,11,12,28,35,37,42 |
| Lábio | 7 (0.08) | 9,13,19,28,35,37,42 |
| Face (local específico não determinado) | 7 (0.08) | 16,19,22,26,35,39,43 |
| Ocular | 4 (0.04) | 9,10,35,42 |
| Zigomático | 4 (0.04) | 9,17,42,43 |
| Membros superiores | 4 (0.04) | 7,19,21,38 |
| Mento | 4 (0.04) | 9,13,28,42 |
| Mandibular | 2 (0.02) | 9,19 |
| Tronco | 2 (0.02) | 5,22 |
| Membros inferiores | 2 (0.02) | 25,33 |
| Tórax | 1 (0.01) | 21 |
| Temporal | 1 (0.01) | 9 |
| Auricular | 1 (0.01) | 9 |
| Pênis | 1 (0.01) | 5 |
Profissional que Realizou o Procedimento
Ao todo, 6 de 38 estudos relatavam o profissional responsável pela realização do procedimento. Em 27 casos, o procedimento foi realizado por médicos, sendo 16 cirurgiões plásticos certificados, 9 dermatologistas e 2 urologistas. Seis preenchimentos foram realizados por profissionais não médicos, incluindo enfermeiros, esteticistas e dentistas.3,5,11,13,28,31
Complicações
As complicações relatadas foram divididas em imediatas (até 30 dias após a injeção de PMMA) e tardias (após 30 dias). Foram relatadas 10 diferentes complicações imediatas, sendo o eritema a mais frequente (26%), seguida do aparecimento de prurido (16%), edema (11%), insuficiência renal aguda (11%), nodulações (11%), e outras menos frequentes (►Tabela 4).
| Imediatas | ||
|---|---|---|
| Tipo | Número de estudos (porcentagem) | Referência |
| Eritema | 5 (0.26) | 13,23,37,38,42 |
| Prurido | 3 (0.16) | 23,37,40 |
| Edema | 2 (0.11) | 23,38 |
| Insuficiência renal aguda | 2 (0.11) | 3,29 |
| Nodulação | 2 (0.11) | 35,42 |
| Choque séptico | 1 (0.05) | 29 |
| Disfunção hepática | 1 (0.05) | 29 |
| Equimose | 1 (0.05) | 37 |
| Insuficiência respiratória | 1 (0.05) | 29 |
| Secreção seropurulenta | 1 (0.05) | 40 |
| Tardias | ||
| Tipo | Número de estudos (porcentagem) | Referência |
| Granuloma | 17 (0.21) | 5,9,10,12-14,16,18 21 22,26,30,33,38,39,41,42 |
| Nodulação | 11 (0.14) | 9,11,19,24,26,28,31,34,35,37,43 |
| Alterações cutâneas | 6 (0.08) | 25-28,38,42 |
| Sinais inflamatórios | 5 (0.06) | 5,9,32,36,38 |
| Edema | 5 (0.06) | 9,13,20,25,26 |
| Infecção | 4 (0.05) | 9,17,28,42 |
| Necrose | 3 (0.04) | 5,9,40 |
| Irregularidade facial | 3 (0.04) | 26,36,42 |
| Hipercalcemia | 2 (0.03) | 18,33 |
| Acometimento ocular | 2 (0.03) | 13,17 |
| Insuficiência renal crônica | 2 (0.03) | 7,21 |
| Redução de função renal | 1 (0.01) | 33 |
| Neovascularização | 1 (0.01) | 9 |
| Pigmentação | 1 (0.01) | 9 |
| Lacrimejamento | 1 (0.01) | 9 |
| Fístula | 1 (0.01) | 9 |
| Reação alérgica | 1 (0.01) | 13 |
| Psoríase | 1 (0.01) | 17 |
| Nefrocalcinose | 1 (0.01) | 18 |
| Linfadenite granulomatosa pulmonar | 1 (0.01) | 18 |
| Pericardite | 1 (0.01) | 21 |
| Síndrome sarcoidose-like | 1 (0.01) | 21 |
| Eritema | 1 (0.01) | 26 |
| Taquicardia | 1 (0.01) | 27 |
| Hipercalemia | 1 (0.01) | 32 |
| Nefrite | 1 (0.01) | 33 |
| Prurido | 1 (0.01) | 33 |
| Hipertensão | 1 (0.01) | 33 |
| Rigidez | 1 (0.01) | 36 |
| Seroma | 1 (0.01) | 38 |
| Sarcoidose pulmonar | 1 (0.01) | 43 |
Em relação às complicações tardias, 30 diferentes tipos foram relatados. O aparecimento de granuloma foi a mais comum (21%), seguida de nodulações inespecíficas (14%), alterações cutâneas (8%), reações inflamatórias (6%), edema (6%), infecção (5%), necrose (4%), irregularidades na face (4%), hipercalcemia (3%), acometimento ocular (3%), insuficiência renal crônica (3%), entre outras (►Tabela 4).
Tratamento
O uso de esteroides,3,7,9-11,13,14,17,18,21,24,26-28,30,32,33,35,36,38,39,41-43 antibióticos3,11,20,25,29,40,42,43 e abordagem cirúrgica,3,7,9,10,12,13,17,23,24,26-28,35,36,38-40,42 incluindo 75 casos de excisão, foram as 3 formas de tratamento mais frequentes. Outras abordagens terapêuticas relatadas incluem o uso de: laser,9,15,19,21,22 fluoruracila,9,14,28 ozônio,9 xylitol,9 alopurinol,9 metotrexato,17 vitamina D,17 hidroxicloroquina,17 colchicina,21 hemodiálise,7,29 suporte vasopressor,29 intubação orotraqueal com suporte ventilatório,29 calcitonina,32,33 infusão salina,32 bifosfonatos,30,32,33 ciclofosfamida,33 cetoconazol33 e ácido hialurônico,36,41 conforme a especificidade de cada caso.
Discussão
Há revisões da literatura5 que destacam o grande número de complicações resultantes de preenchimentos com PMMA. Neste estudo, atualizamos as evidências quanto ao número de relatos de complicações decorrentes do uso de PMMA nos últimos 20 anos, e identificamos uma prevalência significativa de casos ocorridos no Brasil, que representaram mais do que 50% do total de artigos desta revisão. Fatores regulatórios relacionados à história da política de saúde pública brasileira no tratamento dos pacientes com HIV/AIDS podem ser uma explicação para esses achados.
Em 1996, com o surgimento do tratamento antirretroviral de alta potência,a melhora da condição da saúde de pacientes com HIV/AIDS era frequentemente acompanhada de alterações anatômicas estigmatizantes.44 Em vista disso, a Agência Nacional de Vigilância Sanitária (ANVISA) liberou o uso de preenchimentos com PMMA para fins reparadores nessa população.45
A evolução dos fármacos antirretrovirais resultou na diminuição do número de pacientes com lipodistrofias estigmatizantes. Entretanto, é intrigante observar que o número de complicações relacionadas ao uso estético do PMMA aumentou, sendo que, nesta revisão, somente em dois casos as complicações relatadas foram decorrentes do uso do PMMA com finalidade reparadora para o tratamento de pacientes com HIV/AIDS.30,33
Os resultados desta revisão evidenciam que a utilização atual do PMMA extrapola os limites seguros estabelecidos e as indicações formais para o seu uso, conforme determinado pelas agências reguladoras. Um exemplo disso são os relatos de casos de preenchimentos glúteos com volumes de até 900 mL de PMMA,3 sendo que a recomendação do consenso brasileiro publicado por Blanco Souza et al.46 em 2017 é a de que não se exceda o volume máximo de 100 mL nessa região.
Em vista disso, é evidente a importância de destacar alguns pontos quanto à liberação do uso do PMMA com finalidades estéticas. A ausência de fiscalização apropriada resulta em práticas inadequadas, como a realização desses procedimentos por profissionais não médicos, assim como por médicos não capacitados, inclusive fora de ambientes com infraestrutura adequada.3,5,11,13,28,31 A maior parte dos artigos não identificou o prescritor dos preenchimentos realizados, porém, dos 6 estudos que o fizeram, de um total de 34 casos, apenas 16 foram realizados por profissionais certificados para a aplicação do material, o que pode ter contribuído para o aumento do risco relacionado ao procedimento.5
De 2004 a 2024, o número de complicações relacionadas ao uso do PMMA no Brasil foi significativamente maior do que no restante do mundo, totalizando 373 casos. Ainda que a utilização do PMMA com fins estéticos tenha sido questionada pela Sociedade Brasileira de Cirurgia Plástica (SBCP),47 ele ainda é muito utilizado como preenchedor no Brasil, ao passo que, em outros países, outros tipos de preenchedores reversíveis e absorvíveis são mais utilizados, como o ácido hialurônico, enxerto de gordura autóloga, ácido poli-L-lático e bioestimuladores de colágeno.48
Foram relatados mais casos de complicações tardias do que imediatas, sendo que as mais frequentes foram as formações granulomatosas (21%). Cabe ressaltar a potencial gravidade das complicações decorrentes de preenchimentos com PMMA, como choque séptico e insuficiência renal crônica,7,21,29 além da incerteza quanto à segurança em longo prazo, tendo em vista os relatos12 de granulomas de corpo estranho em locais distantes da aplicação do PMMA. Em vista disso, uma fiscalização mais rígida da distribuição, venda, prescrição e dos locais onde são realizados esses procedimentos, assim como a conscientização da população sobre os riscos relacionados ao PMMA podem contribuir para a diminuição da incidência de efeitos adversos.6
A ANVISA autoriza a aplicação de PMMA em duas situações: correção da lipodistrofia decorrente do uso de antiretrovirais e para correção volumétrica facial e corporal. Não há contraindicação de uso do PMMA nos glúteos, mas não deve ser utilizado com o objetivo de aumento do volume. A aplicação deve ser realizada somente por médicos qualificados para essa finalidade, os quais devem decidir, a partir de uma avaliação detalhada, a dosagem e o número de injeções apropriadas para cada paciente, levando em conta as particularidades e necessidades do indivíduo.49
É importante salientar que a ANVISA classifica o PMMA como um produto médico implantável de classe de risco IV. Essa classificação pressupõe um alto nível de controle regulatório devido aos potenciais riscos de complicação, como reações inflamatórias, infecções, migração do material e necrose tecidual, sobretudo por se tratar de material permanente e não reabsorvível pelo organismo, o que destaca a irreversibilidade desse método de preenchimento.49
No que diz respeito à segurança, alternativas mais seguras ao PMMA incluemo ácido hialurônico e agordura autóloga. O ácido hialurônico apresenta maior biocompatibilidade, menor risco de complicações e a possibilidade de reversão com a aplicação da enzima hialuronidase. A gordura autóloga também é uma opção viável e segura, com menor risco complicações.50
Com relação às limitações desta revisão, destacamos uma incerteza: a maior incidência de complicações relatadas no Brasil é decorrente da maior frequência de procedimentos com PMMA ou realmente existe uma maior incidência de complicações? Essa é uma limitação significativa, uma vez que não dispomos de dados absolutos sobre o número total de procedimentos realizados no Brasil e no mundo. Outra limitação é o fato de a revisão se basear apenas nos casos de complicações documentadas na literatura, o que pode não refletir a realidade. É provável que o número de complicações seja muito maior do que o relatado, visto que complicações não publicadas em artigos científicos não foram contabilizadas.
Conclusão
O uso de preenchimentos de PMMA está relacionado ao aparecimento de complicações imediatas e tardias graves. A maioria dos casos de complicações não está relacionada ao uso para a correção de lipodistrofias em pacientes com HIV/AIDS, e 64% dos casos de complicação descritos na literatura médica dos último 20 anos ocorreram no Brasil. O PMMA é inabsorvível, e múltiplos procedimentos cirúrgicos invasivos podem ser necessários para tratar as sequelas decorrentes da sua utilização como preenchedor permanente. Existem alternativas ao PMMA que são reversíveis e apresentam menores riscos à saúde dos pacientes.
Referências
1. Richards BG, Schleicher WF, D’Souza GF, Isakov R, Zins JE. The Role of Injectables in Aesthetic Surgery: Financial Implications. Aesthet Surg J 2017;37(09):1039-1043. Doi: 10.1093/asj/sjx136
2. de Maio M. The minimal approach: an innovation in facial cosmetic procedures. Aesthetic Plast Surg 2004;28(05): 295-300. Doi: 10.1007/s00266-004-0037-1
3. Kurimori KT, Mendes M, Milcheski DA, Monteiro AA Junior, Gemperli R. Severe complication due to inappropriate use of polymethylmethacrylate: a case report and current status in Brazil. Rev Bras Cir Plást 2019;34(01):156-162
4. Martins WH, Pessôa KVO, Martins MA, Silva MH, Pereira Filho GV, Abreu LC. Facial filling with polymethylmethacrylate in patients with acquired immunodeficiency syndrome. Rev Bras Cir Plást 2016;31(02):216-228
5. Salles AG, Lotierzo PH, Gemperli R, et al. Complications after polymethylmethacrylate injections: report of 32 cases. Plast Reconstr Surg 2008;121(05):1811-1820. Doi: 10.1097/PRS.0b013e31816b1385
6. Martins EL, Kock PA, Fedatto PF. Polimetilmetacrilato (PMMA) na prática clínica: Revisão integrativa sobre abordagens estéticas, complicações e aspectos regulatórios. Research. Soc Dev 2024;13 (06):e9013646046 Available from https://rsdjournal.org/index.-php/rsd/article/view/46046[Internet]
7. Manfro AG, Lutzky M, Dora JM, Kalil MAS, Manfro RC. Case reports of hypercalcemia and chronic renal disease due to cosmetic injections of polymethylmethacrylate (PMMA). J Bras Nefrol 2021; 43(02): 288-292https://www.scielo.br/pdf/jbn/2020nahead/2175-8239-jbn-2020-0044.pdf
8. Cordeiro G, Salotti Ldos RAmbrósio LHC, De Oliveira Júnior MR, Maciel LTR, Coêlho MDG. Reações do PMMA nos procedimentos estéticos faciais. BrazilianJournal of Health Review. 2023;6(06): 27030-27042
9. Goldman A, Marinowic DR, Luz PM. Complicações relacionadas ao uso de polimetilmetacrilato na face: Análise de 209 casos. Rev Bras Cir Plást 2024;39(02):e0900
10. Durkin AJ, Catena D, Woltjen N, et al. Surgical Management of Polymethylmethacrylate-Collagen Gel Complications in the Lower Eyelid: A Case Series. Ann Plast Surg 2023;90(01):12-18. Doi: 10.1097/SAP.0000000000003364
11. Vengalil N, Council LM, Michalski BM. Foreign body granulomas to polymethylmethacrylate soft tissue filler following COVID-19 infection. JAAD Case Rep 2023;41:1-3. Doi: 10.1016/j.jdcr.2023.08.037
12. Saoud C, Lossos C, Ali SZ. Polymethylmethacrylate-induced foreign body reaction presenting as bilateral parotid lesions: A case report of dermal filler adverse reaction diagnosed on fine needle aspiration. Cytopathology 2023;34(04):385-387. Doi: 10.1111/cyt.13233
13. Parikh AO, Conger JR, Sibug Saber ME, Samimi D, Burnstine MA. Multiple cases of facial disfigurement from filler use and one injector. Ophthalmic Plast Reconstr Surg 2023;39(04):366-369. Doi: 10.1097/IOP.0000000000002323
14. Sivam S, Mackay C, Humphrey C, Kriet JD. Giant PMMA foreign body granulomas with imaging. J Cutan Aesthet Surg 2023;16 (03):256-258. Doi: 10.4103/JCAS.JCAS_194_20
15. Goldman A, Wollina U, Machado D, Marionwic D. Laser in the Treatment of Granulomas on the Nose Produced by Polymethylmethacrylate: A Case Series. J Drugs Dermatol 2021;20(11): 1161-1166. Doi: 10.36849/jdd.6550
16. Dhaliwal P, Ibad S, Losak D, Cockerell C. A Case of Granulomatous Hypersensitivity Reactions to a Dermal Filler Precipitated by PD-1 Checkpoint Inhibitor Therapy. Skin (Milwood, NY) 2021;5(01): 41-45. Doi: 10.25251/skin.5.1.10
17. Freire de Carvalho J. Polyautoimmunity (Psoriasis, Sjogren’s syndrome, and autoimmune uveitis) following polymethylmethacrylate injection. Eur Rev Med Pharmacol Sci 2021;25(06): 2478-2480. Doi: 10.26355/eurrev_202103_25410
18. Alimoradi M, Chahal A, El-Rassi E, Daher K, Sakr G. Synthol systemic complications: Hypercalcemia and pulmonary granulomatosis. A case report. Ann Med Surg (Lond) 2021; 69:102771. Doi: 10.1016/j.amsu.2021.102771
19. Goldman A, Wollina U. Polymethylmethacrylate-induced nodules of the lips: Clinical presentation and management by intralesional neodymium:YAG laser therapy. Dermatol Ther 2019;32(01): e12755. Doi: 10.1111/dth.12755
20. Ibrahim O, Dover JS. Delayed-onset nodules after polymethyl methacrylate injections. Dermatol Surg 2018;44(09):1236-1238. Doi: 10.1097/DSS.0000000000001405
21. Goldman A, Staub H, Wollina U. HYPERCALCEMIA DUE TO POLY- METHYLMETHACRYLATE INJECTIONS? (LITERATURE REVIEW AND CASE REPORTS). Georgian Med News 2018;9(282):17-20
22. Goldman A, Wollina U. Intralesional Neodymium YAG laser to Treat Complications of Polymethylmethacrylate. Open Access Maced J Med Sci 2018;6(09):1636-1641. Doi: 10.3889/oamjms.2018.348
23. Shah V, Chaubal TV, Bapat RA, Shetty D. Allergic contact dermatitis caused by polymethylmethacrylate following intradermal filler injection. Contact Dermatitis 2017;77(06):407-408. Doi: 10.1111/cod.12779
24. Souza RN, Mendoça SG, Alencar EC, França ALA, Araújo ÊG, Leite LAS. Complicação tardia de preenchimento cutâneo após facelift: relato de caso. Rev Bras Cir Plást 2016;31(02):269-272
25. Cannata-Ortiz P, Gracia C, Aouad Y, et al. Small vessel microembolization and acute glomerulonephritis following infection of aesthetic filler implants. Diagn Pathol 2016;11:2. Doi: 10.1186/s13000-016-0453-y
26. Limongi RM, Tao J, Borba A, et al. Complications and Management of Polymethylmethacrylate (PMMA) Injections to the Midface. Aesthet Surg J 2016;36(02):132-135. Doi: 10.1093/asj/sjv195
27. Purnell CA, Klosowiak JL, Cheesborough JE, Park E, Bandy A, Dumanian GA. Resolution of Cosmetic Buttock Injection-induced Inflammatory Reaction and Heart Failure after Excision of Filler Material. Plast Reconstr Surg Glob Open 2016;4(10):e1079. Doi: 10.1097/GOX.0000000000001079
28. Friedmann DP, Kurian A, Fitzpatrick RE. Delayed granulomatous reactions to facial cosmetic injections of polymethylmethacrylate microspheres and liquid injectable silicone: A case series. J Cosmet Laser Ther 2016;18(03):170-173. Doi: 10.3109/14764172.2015.1114642
29. Boattini M, Francisco AR, Cavaco R, Rodrigues J, Bento L. Shock following subcutaneous injections of polymethylmethacrylate. Med Intensiva 2015;39(04):256-257. Doi: 10.1016/j.medin.2014.06.011
30. Hindi SM, Wang Y, Jones KD, et al. A Case of Hypercalcemia and Overexpression of CYP27B1 in Skeletal Muscle Lesions in a Patient with HIV Infection After Cosmetic Injections with Polymethylmethacrylate (PMMA) for Wasting. Calcif Tissue Int 2015;97(06): 634-639. Doi: 10.1007/s00223-015-0048-8
31. Cinotti E, Perrot JL, Labeille B, et al. Identification of a soft tissue filler by ex vivo confocal microscopy and Raman spectroscopy in a case of adverse reaction to the filler. Skin Res Technol 2015;21 (01):114-118. Doi: 10.1111/srt.12166
32. Rados DV, Furlanetto TW. An unexpected cause of severe and refractory PTH-independent hypercalcemia: case report and literature review. Arch Endocrinol Metab 2015;59(03):277-280. Doi: 10.1590/2359-3997000000051
33. Negri AL, Rosa Diez G, Del Valle E, et al. Hypercalcemia secondary to granulomatous disease caused by the injection of methacrylate: a case series. Clin Cases Miner Bone Metab 2014;11(01):44-48
34. Costa FW, Teixeira LH, Carvalho FS, et al. Bilateral oral nodules after the use of a dermal filler containing polymethylmethacrylate microspheres in an older woman. J Am Geriatr Soc 2014;62 (03):587-588. Doi: 10.1111/jgs.12717
35. Park TH, Seo SW, Kim JK, Chang CH. Clinical experience with polymethylmethacrylate microsphere filler complications. Aesthetic Plast Surg 2012;36(02):421-426. Doi: 10.1007/s00266-011-9803-z
36. Park TH, Yeo KK, Seo SW, et al. Clinical experience with complications of hand rejuvenation. J Plast Reconstr Aesthet Surg 2012;65(12):1627-1631. Doi: 10.1016/j.bjps.2012.06.008
37. Solomon P, Sklar M, Zener R. Facial soft tissue augmentation with Artecoll(®): A review of eight years of clinical experience in 153 patients. Can J Plast Surg 2012;20(01):28-32. Doi: 10.1177/229255031202000110
38. Al-Qattan MM. Complications related to Artecoll injections for soft tissue augmentation of the hand: 3 case reports. J Hand Surg Am 2011;36(06):994-997. Doi: 10.1016/j.jhsa.2011.03.016
39. Santana KP, Pereira LH, Sabatovich O, Sterodimas A. Foreign-body granulomas caused by polymethylmethacrylate (PMMA) microspheres: successful correction by autologous fat transplantation. J Plast Reconstr Aesthet Surg 2010;63(02):e139-e141. Doi: 10.1016/j.bjps.2009.01.088
40. de Figueiredo JCA, Naufal RR, Zampar AG, Mélega JM. Expanded median forehead flap and abbé flap for nasal and upper lip reconstruction after complications of polymethylmethacrylate. Aesthetic Plast Surg 2010;34(03):385-387. Doi: 10.1007/s00266-008-9294-8
41. Wollina U. Facial recontouring for late dermal filler complications. Kosmetische Medizin. 2009;6:219-221
42. Wolfram D, Tzankov A, Piza-Katzer H. Surgery for foreign body reactions due to injectable fillers. Dermatology 2006;213(04): 300-304. Doi: 10.1159/000096193
43. Sidwell RU, McL Johnson N, Francis N, Bunker CB. Cutaneous sarcoidal granulomas developing after Artecoll facial cosmetic filler in a patient with newly diagnosed systemic sarcoidosis. Clin Exp Dermatol 2006;31(02):208-211. Doi: 10.1111/j.1365-2230.2005.01993.x
44. Kates LC, Fitzgerald R. Poly-L-lactic acid injection for HIV-associated facial lipoatrophy: treatment principles, case studies, and literature review. Aesthet Surg J 2008;28(04):397-403. Doi: 10.1016/j.asj.2008.06.005
45. Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Departamento de DST, Aids e Hepatites Virais. Manual de tratamento da lipoatrofia facial : recomendações para o preenchimento facial com polimetilmetacrilato em portadores de HIV/aids / Ministério da Saúde, Secretaria de Vigilância em Saúde, Departamento de DST, Aids e Hepatites Virais. Brasília: Ministério da Saúde; 2009
46. Blanco Souza TA, Colomé LM, Bender EA, Lemperle G. Brazilian Consensus Recommendation on the Use of Polymethylmethacrylate Filler in Facial and Corporal Aesthetics. Aesthetic Plast Surg 2018;42(05):1244-1251. Doi: 10.1007/s00266-018-1167-1
47. Cappella A, Galvão L, Nazar L, Alves D (2023). Polimetilmetacrilato na Harmonização Orofacial-Vantagens e desvantagens, Revisão de literatura. Revista Científica da UNIFENAS-ISSN: 2596-3481, 5(1).
48. Li K, Meng F, Li YR, et al. Application of Nonsurgical Modalities in Improving Facial Aging. Int J Dent 2022;2022:8332631. Doi: 10.1155/2022/8332631
49. Anvisa. Anvisa esclarece sobre indicações do PMMA. Ministério da Saúde, publicado em 04/07/2022, atualizado 03/11/2022. Disponível em: https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2018/anvisa-esclarece-sobre-indicacoes-dopmma
50. Papazian MF, Silva LM, Crepaldi AA, Crepaldi MLS, Aguiar AP. Principais aspectos dos preenchedores faciais. Rev FAIPE 2018;8 (01):101-116
1. Clínica privada, São Paulo, SP, Brasil
2. Curso de Medicina, Escola Bahiana de Medicina e Saúde Pública, Salvador, BA, Brasil
3. Curso de Medicina, Universidade Salvador, Salvador, BA, Brasil
4. Faculdade de Medicina, Universidade de São Paulo, São Paulo, SP, Brasil
Endereço para correspondência Alessandra Lima Costa, Curso de Medicina, Escola Bahiana de Medicina e Saúde Pública, Salvador, BA, Brasil (e-mail: alessandracosta21.1@bahiana.edu.br alessandracosta21.1@bahiana.edu.br).
Artigo submetido: 14/08/2024.
Artigo aceito: 29/09/2024.
Conflito de Interesses
Os autores não têm conflito de interesses a declarar.








 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter