

Original Article - Year 2021 - Volume 36 -
Revisão de 5 anos (2015-2019) da reconstrução aloplástica imediata no Centro Hospitalar e Universitário de Coimbra, Portugal
5-year revision (2015-2019) of immediate alloplastic reconstruction in Hospital and University Center of Coimbra, Portugal
RESUMO
Introdução: Como o câncer de mama é a doença maligna mais prevalente em todo o mundo, o tratamento conservador é de extrema importância. No entanto, em muitos casos, a mastectomia continua sendo o procedimento cirúrgico indicado e, como qualquer outra amputação, leva um fardo significativo para essas pacientes. No caso da mastectomia, a reconstrução imediata da mama é o tratamento padrão. A reconstrução aloplástica continua sendo o tipo mais amplamente realizado de reconstrução mamária imediata.
Métodos: Neste artigo, os autores apresentam uma série de 105 casos de reconstrução aloplástica imediata em 5 anos de 2015 a 2019 no Centro Hospitalar e Universitário de Coimbra, Portugal. Inclui mastectomias curativas e redutoras de risco realizadas por ginecologistas oncológicos. As opções de reconstrução oferecidas pela equipe de reconstrução plástica incluíram tanto a reconstrução direta no implante quanto a reconstrução em dois estágios com o uso de expansores de tecido.
Resultados: Dados sobre a doença oncológica, tipo de mastectomia, critérios de seleção das pacientes e resultados pós-operatórios imediato e tardio com diferentes técnicas de reconstrução imediata foram coletados, analisados e comparados com a literatura. Em nosso estudo, o índice de massa corporal foi o único preditor mais significativo de complicações e seu impacto foi estatisticamente significativo.
Conclusão: Os resultados obtidos representam uma etapa essencial para a melhoria da qualidade da assistência à mulher em reconstrução mamária.
Palavras-chave: Neoplasias mamárias; Neoplasias mamárias experimentais; Mastectomia segmentar; Mamografia; Implantes mamários.
ABSTRACT
Introduction: With breast cancer being the most prevalent malignancy worldwide, conservative treatment is of tremendous importance. Nevertheless, in many cases, mastectomy remains the indicated surgical procedure, and like any other amputation, it carries a significant burden on those patients. In the case of mastectomy, immediate breast reconstruction is the standard of care. Alloplastic reconstruction remains the most widely performed type of immediate breast reconstruction.
Methods: In this article, the authors present a series of 105 cases of immediate alloplastic reconstruction in 5 years from 2015 to 2019 in Centro Hospitalar e Universitário de Coimbra, Portugal. It includes curative and risk-reducing mastectomies performed by oncologic gynecologists. The reconstruction options offered by the plastic reconstructive team included both direct-to-implant reconstruction and two-stage reconstruction with the use of tissue expanders.
Results: Data regarding the oncologic disease, type of mastectomy, patient selection criteria and immediate and late postoperative outcomes with different techniques of immediate reconstruction were collected, analyzed, and compared to literature. In our study, body mass index was the single most significant predictor of complications and, its impact was statistically significant.
Conclusion: The results obtained represent an essential step to improving care quality for women undergoing breast reconstruction.
Keywords: Breast neoplasms; Experimental breast neoplasms; Segmental mastectomy; Mammography; Breast implants.
INTRODUÇÃO
A reconstrução mamária imediata após a mastectomia traz benefícios inegáveis, tanto estéticos quanto psicológicos, evitando um procedimento estigmatizante com nítidas repercussões na qualidade de vida de pacientes com câncer ou mulheres com alto risco de desenvolver câncer de mama1.
Aproximadamente uma em cada oito mulheres nos Estados Unidos desenvolve câncer de mama, com 200.000 novos casos diagnosticados por ano2. Seguindo a tendência de cirurgias conservadoras mais frequentes, há também uma tendência crescente para reconstrução mamária imediata após mastectomia. As taxas de reconstrução aumentaram de 11,6% para 36,4% para mastectomias unilaterais e 36,0% para 57,2% para mastectomias bilaterais entre 1998 e 2011, respectivamente3. A American Society of Plastic Surgeons estimou que 109.256 mulheres foram submetidas à reconstrução mamária em 2016 apenas nos EUA4. A reconstrução mamária imediata mais frequente é a aloplástica. A reconstrução aloplástica inclui dois estágios com o uso de expansores de tecido e reconstrução direta ao implante (RDI )5.
As complicações maiores que implicam em reoperação e falha na reconstrução são relatadas em até 20% a 35%4. Portanto, a avaliação da qualidade e a avaliação dos resultados cirúrgicos são obrigatórias para melhorar a prática clínica. Fatores de risco do paciente como obesidade, tabagismo, radiação e o uso de matrizes dérmicas acelulares influenciam na taxa de complicações6. A pandemia e o aumento da proporção de obesidade significam que um número significativo desses pacientes terá um risco adicional de complicações pós-operatórias, conforme apontado na literatura, com o compromisso com a viabilidade da reconstrução6.
Avaliar os resultados da reconstrução mamária nessa população é um desafio devido ao tempo necessário para a conclusão do processo de reconstrução e à quantidade de variáveis que podem interferir nos resultados em longo prazo.
As complicações mais frequentes relacionadas à reconstrução mamária baseada em implantes são necrose e infecção da pele, frequentemente levando a cirurgias adicionais e comprometendo o momento ideal de terapias adjuvantes2.
A taxa de sobrevida geral em 5 anos após a mastectomia é de 98,7%. Ainda e, de acordo com a literatura em inglês, a maioria das mulheres submetidas à mastectomia ainda não faz a reconstrução mamária7.
OBJETIVO
O objetivo do estudo é avaliar os resultados pós-operatórios imediato e tardio, comparando diferentes tipos de reconstrução imediata e identificando fatores de risco para complicações da reconstrução aloplástica imediata no Centro Hospitalar e Universitário de Coimbra (CHUC), Portugal.
Esses resultados representam um passo importante para a melhoria da qualidade da assistência à mulher em reconstrução mamária.
MÉTODOS
Este estudo retrospectivo avaliou mulheres que foram submetidas à reconstrução aloplástica imediata após mastectomia em um centro médico terciário durante cinco anos entre 2015 e 2019. Os pacientes foram selecionados se tivessem se submetido à mastectomia com reconstrução baseada em implante (RDI ou dois estágios com expansor de tecido). Pacientes que realizaram reconstrução mamária tardia foram excluídas deste estudo.
Os dados clínicos, incluindo idade, comorbidades, tabagismo, quimioterapia neoadjuvante e índice de massa corporal (IMC) foram coletados de prontuários médicos. As comorbidades incluíram obesidade, hipertensão, doença arterial coronariana e diabetes.
As variáveis cirúrgicas coletadas foram o tipo de reconstrução (dois estágios versus RDI), lateralidade (procedimento unilateral ou bilateral) e matriz dérmica acelular. As equipes cirúrgicas eram compostas por oncologistas ginecológicos e cirurgiões plásticos.
Complicações clínicas precoces e tardias relevantes foram analisadas e comparadas de acordo com o tipo de reconstrução. As complicações precoces incluíram infecção, necrose de retalhos de mastectomia/complexo areolopapilar (CAP), hematoma, seroma ou extrusão/deiscência. As complicações tardias foram seroma tardio, mau posicionamento ou rotação do implante, contratura capsular, dor crônica e linfedema. Seroma foi definido como qualquer coleção de fluidos que se desenvolveu após a remoção do dreno ou débito diário acima de 30 cc durante mais de dez dias. Infecção foi definida como qualquer paciente recebendo antibióticos além do curso pós-operatório esperado ou reiniciando os antibióticos por suspeita de infecção ou eritema. A contratura capsular foi definida como a classificação de contratura capsular de Baker de grau III e IV8.
A falha da reconstrução mamária foi definida como uma complicação que resulta na remoção de um implante ou expansor de tecido. A necessidade de remoção do implante foi avaliada com base na causa. Posteriormente, outras opções reconstrutivas foram fornecidas a esses pacientes.
Os dados de tendência do IMC, categorizados como normal, com sobrepeso e obesidade, foram analisados por meio de regressão logística.
A análise estatística foi realizada no SPSS versão 23.0. As variáveis categóricas foram analisadas com o teste do qui-quadrado e as variáveis contínuas com o teste t de Student. O nível de significância adotado foi α = 0,05 (intervalo de confiança de 95%).
Este estudo observacional foi desenvolvido no Centro Hospitalar e Universitário de Coimbra (CHUC), submetido à Comissão de Ética do CHUC com o número de referência 210/CES.
RESULTADOS
Nosso ensaio consiste em um estudo retrospectivo da reconstrução mamária aloplástica imediata no CHUC em 5 anos, de 2015 a 2019. Nesse período, um total de 500 pacientes foram submetidas à reconstrução mamária no setor de cirurgia plástica. Desta amostra, 132 mulheres foram submetidas à reconstrução mamária imediata após a mastectomia por câncer de mama ou de forma preventiva pela equipe de oncologia ginecológica.
A maioria desses pacientes foi submetida a reconstrução aloplástica imediata compreendendo uma amostra de 105 pacientes selecionados para este artigo. Portanto, a reconstrução aloplástica imediata compreendeu cerca de 80% da reconstrução imediata total (com 20% sendo autóloga) e cerca de 21% da reconstrução total da mama em nosso departamento. A idade média dos pacientes era 48,5 ± 8,2 [27-71] anos, 87,6% (n = 92) foram submetidos à mastectomia terapêutica para câncer de mama, carcinoma ductal invasivo predominante (44,8%, n = 47), seguido por carcinoma ductal in situ (24,8%, n = 26) e carcinoma lobular invasivo (13,3 %, n = 14). Além disso, cinco mulheres foram submetidas à mastectomia profilática contralateral no mesmo tempo operatório da mastectomia terapêutica total. 12,4% (n = 13) tiveram mastectomia redutora de risco (profilática).
A maioria das pacientes teve reconstrução mamária unilateral (84,8% [n = 89]). A reconstrução bilateral foi realizada em 16 mulheres (15,2%); 6 eram mastectomias redutoras de risco, 5 tinham câncer de mama bilateral e as 5 restantes foram realizadas em um contexto de mastectomia redutora de risco contralateral.
A mastectomia total foi realizada em 66 pacientes (62,9%), sendo três bilaterais; mastectomia poupadora de pele em 17 casos (16,2%), sendo 2 bilaterais, ambas redutoras de risco; e mastectomia preservadora de mamilo em 16 (15,2%), das quais cinco bilaterais. Além disso, seis mulheres foram submetidas à mastectomia total e mastectomia conservadora do mamilo contralateral.
41,9% (n = 44) das pacientes foram submetidas à reconstrução mamária imediata com técnica direta ao implante, enquanto 58,1% (n = 61) foram submetidas à reconstrução mamária em dois estágios com expansor. A matriz dérmica acelular (MDA) foi utilizada em 26,7% (n = 27) das reconstruções mamárias. A comparação estatística mostrou um aumento significativo na técnica direto para implante vs. expansor ao longo dos anos (de 19,0% em 2015 para 52,4% em 2019).
Procedimentos secundários/complementares
43% (n = 45) dos pacientes foram submetidos a procedimentos secundários na mama reconstruída isoladamente ou em combinação. Houve 26 reconstruções CAP, 24 lipofilling, 2 casos de mastopexia e quatro revisões de cicatriz. 40% (n = 42) de nossas pacientes foram submetidas a simetrização contralateral por mamoplastia redutora ou mastopexia (n = 39) ou por aumento das mamas (n = 3).
As indicações mais comuns para revisões incluíram a melhoria das irregularidades do contorno dos tecidos moles. O lipofilling tornou-se um complemento comum para melhorar os contornos e camuflar a periferia do implante (n = 25).
Complicações
O tempo médio de admissão do paciente foi de 9,5 ± 5,0 dias [2-28]. A taxa geral de complicações foi de 47,6% (n = 50).
Complicações precoces ocorreram em 32,3% (n = 34) e incluíram infecção (n = 10), necrose parcial de retalhos de mastectomia (n = 6) e necrose completa (n = 4), hematoma (n = 8), seroma (n = 12) e extrusão/deiscência (n = 5). Falha total da reconstrução ocorreu em 8 casos.
As complicações tardias foram menos frequentes, afetando 20,0% (n = 21) dos pacientes. Composto por seroma tardio (n = 3), mau posicionamento ou rotação do implante (n = 2), contratura capsular (n = 7), dor crônica (n = 6) e linfedema (n = 2). A substituição do implante foi necessária em 3 casos.
| Complicações precoce | N | % |
|---|---|---|
| Seroma/drenagem prolongada | 12 | 11,4 |
| Hematoma | 8 | 7,6 |
| Necrose de retalhos de mastectomia ou CAP | 10 | 9,5 |
| Extrusão | 5 | 4,7 |
| Infecção | 10 | 9,5 |
| Complicações tardias | N | % |
| Seroma tardio | 3 | 2,8 |
| Má posição, rotação do implante | 2 | 1,8 |
| Contratura capsular | 7 | 6,6 |
| Dor crônica | 6 | 5,7 |
| Linfedema | 2 | 1,8 |
As taxas gerais de complicações, tanto precoces quanto tardias, são apresentadas na Tabela 1.
Complicações menores, como exposição da sutura, cicatrização retardada e epidermólise, geralmente se resolvem por si mesmas com o tratamento conservador.
Dois pacientes foram tratados por revisão do implante e três necessitaram de troca do implante. Vinte pacientes tiveram falha completa da reconstrução aloplástica. Destes, 12 receberam reconstrução autóloga (4 perfurador da artéria epigástrica inferior profunda (DIEP), 5 latissimus dorsi (LD), 2 perfurador da artéria toracodorsal (TDAP) e 1 miocutâneo transverso do reto abdominal (TRAM). Além disso, oito mulheres não queriam reconstrução adicional e 2 tiveram recorrência da doença oncológica.
A comparação estatística mostrou um aumento significativo nas complicações gerais para pacientes na técnica direta ao implante versus reconstrução imediata baseada em expansor de tecido em dois estágios (59,1% [n = 26] versus 39,3% [n = 24], p = 0,046).
O IMC médio foi de 24,8 ± 4,0 [18-37] kg/m2. 59,1% das mulheres tinham peso normal (IMC 18,5-24,9kg/m2), 24,7% estavam com sobrepeso (IMC 25,0-29,9kg/m2) e 16,1% eram obesas (IMC≥30,0kg/m2).
A taxa de complicações foi significativamente maior no grupo de mulheres obesas em comparação às mulheres com peso normal (80,0% vs. 40,0%, p = 0,006) e com sobrepeso (80% vs. 43,5%, p = 0,026), principalmente às custas de complicações iniciais (66,7% vs. 23,6%, p = 0,002; 66,7 vs. 26,1%, p = 0,013). Mulheres com sobrepeso não tiveram mais complicações em comparação com mulheres com peso normal. A incidência de complicações tardias também não foi significativamente diferente entre todos os grupos. O IMC como fator preditivo de complicações não atingiu significância estatística, mas o ponto de corte de 23,5kg/m2 foi associado a melhor sensibilidade (56,8%) e especificidade (53,1%) em conjunto. O ponto de corte para obesidade (IMC> 30kg/m2) foi associado a uma especificidade de 95,9%, apesar de um valor de sensibilidade reduzido (15,9%). A comparação das complicações entre os índices de IMC é indicada na Tabela 2.
DISCUSSÃO
Como afirmado acima, a reconstrução aloplástica imediata pode ser direta ao implante ou em dois estágios com o uso de um expansor e implante.
Direto para implante
Em pacientes ssselecionadas, essa abordagem oferece benefícios em relação à reconstrução mamária em dois estágios, como boa simetria com seios pequenos, menos cirurgias, retorno mais rápido à vida cotidiana e prevenção do período de expansão. Também agrega benefícios psicológicos9 - a sensação de que a paciente nunca perdeu totalmente a mama e economia geral de custos - se faz tudo em um único procedimento10-12. As limitações do RDI são o tamanho da mama, maior risco de necrose da pele ou mamilo é tecnicamente mais exigente para acertar em um procedimento e o risco de radiação pós-operatória afetar negativamente o resultado.
| Comparando o peso com as complicações: |
|---|
| Peso normal vs. excesso de peso -> p = 0,799 |
| Peso normal vs. obesidade -> p = 0,006 ---> estatisticamente significativo |
| Excesso de peso vs. obesidade -> p = 0,026 ---> estatisticamente significativo |
| Comparando o peso com as complicações iniciais: |
| Peso normal vs. excesso de peso -> p = 0,498 |
| Peso normal vs. obesidade -> p = 0,001 ---> estatisticamente significativo |
| Excesso de peso vs. obesidade -> p = 0,02 ---> estatisticamente significativo |
| Comparando o peso com as complicações tardias: |
| Peso normal vs. excesso de peso -> p = 0,966 Peso normal vs. obesidade -> p = 0,791 Excesso de peso vs. obesidade -> p = 0,785 |
IMC: Índice de Massa Corporal
O candidato ideal é uma não fumante saudável com seios pequenos que desejam um tamanho semelhante ou ligeiramente maior, com ptose mínima, para fazer uma mastectomia profilática ou para tratar uma doença em estágio inicial com baixa probabilidade de terapia adjuvante pós-operatória.
A principal limitação da RDI é fornecer cobertura adequada e estável de tecidos moles para um implante em uma nova bolsa de mastectomia.
Mulheres com tamanho maior e seios ptóticos podem ser candidatas à mastectomia de redução de pele (geralmente em padrão T) com reconstrução direta ao implante; este procedimento aumenta o risco de necrose do CAP.
Em nosso centro, as pacientes com histórico de radiação mamária e aquelas que provavelmente necessitarão de radiação pós-mastectomia têm tradicionalmente recebido a reconstrução autóloga.
O plano escolhido em nosso centro foi principalmente a cobertura submuscular parcial usando MDA para cobrir o polo inferior em um plano duplo.
Normalmente, após a criação da bolsa para o implante, o músculo é avançado inferiormente até que o contorno do polo superior desejado seja alcançado. A matriz é então aparada para criar uma bolsa apertada e de suporte e suturada ao polo inferior para funcionar como uma expansão peitoral até o sulco inframamário (SIM) em um plano duplo.
O MDA tem sido usado rotineiramente na reconstrução de RDI. As duas marcas de MDA mais utilizadas em nosso departamento/hospital foram Strattice® e Native®.
Algumas pacientes com retalhos de mastectomia bem vascularizados receberam uma reconstrução subcutânea ou pré-peitoral geralmente combinada com MDA enrolado ao redor do implante. Para esta técnica, o Surgimend® foi escolhido como o MDA de preferência devido a sua maior flexibilidade e suporte em relação ao anterior. No entanto, essa técnica pode causar estresse significativo nos retalhos de mastectomia do polo inferior, levando à necrose dos tecidos moles em curto prazo e afinamento significativo em longo prazo.
A cobertura submuscular total costuma ser desafiadora porque limita o tamanho de um implante que pode ser colocado e não permite o preenchimento natural do polo inferior. Portanto, foi reservado para colocação de expansor e não para RDI.
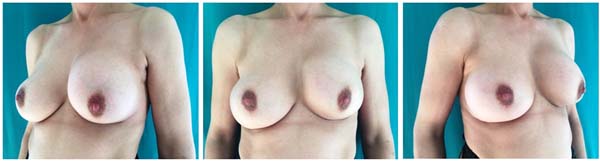
O caso clínico 1 descreve uma paciente de 45 anos com diagnóstico de carcinoma invasivo na mama esquerda. A paciente havia feito aumento mamário anterior há 20 anos e havia contração capsular mamária esquerda (pré-operatório - Figura 1). A paciente foi submetida a mastectomia poupadora de CAP bilateral e linfadenectomia axilar do lado esquerdo. A reconstrução imediata do RDI foi realizada com implantes de 460cc e MDA em um modo de plano duplo. A Figura 2 descreve o resultado 1 ano depois.
Caso clínico 1: reconstrução mamária com DTI imediata
Reconstrução imediata em dois estágios
Por envolver dois procedimentos cirúrgicos, essa técnica aumenta as chances de se obter um melhor resultado. É tecnicamente mais simples e tem indicações mais amplas. Provoca menos tensão nos retalhos de mastectomia devido aos menores volumes de expansão e, portanto, menor risco de necrose cutânea. Em relação ao RDI, tem como desvantagem o atraso no desfecho devido ao período de expansão e a necessidade de mais uma cirurgia.
Os pacientes ideais são não fumantes saudáveis, com pele da parede torácica expansível e tecidos moles de boa qualidade.
Suas contraindicações absolutas são a falta de pele expansível disponível ou suporte ósseo subjacente para resistir às forças do processo de expansão subjacente. Portanto, não oferecemos esta reconstrução rotineiramente para pacientes que se submeteram ou serão submetidos à radioterapia. Em vez disso, esses pacientes receberam reconstrução autóloga.
Marcações
As marcações são feitas com o paciente sentado, com a presença da equipe oncológica e reconstrutiva. Os pontos de referência anatômicos que devem ser traçados no paciente incluem a linha média do tórax, as bordas medial e superior da mama e o sulco mamário lateral (SML) e o SIM.
A incisão escolhida é baseada em vários fatores, incluindo o tamanho e formato pré-operatório da mama, o tamanho e a posição pós-operatória desejada da mama e a localização de cicatrizes pré-existentes.
Apesar de ajudar a alcançar o resultado reconstrutivo desejado, as marcações devem permitir ao cirurgião realizar uma mastectomia oncológica segura.
Avião escolhido
O plano escolhido em nosso centro foi preferencialmente a cobertura submuscular total para cobrir o expansor.
O plano duplo foi ocasionalmente usado. Quando escolhida, a técnica de plano duplo costumava ser combinada com MDA para cobrir o polo inferior.
O pré-peitoral raramente era usado, pois uma expansão do polo inferior pode causar estresse significativo nos retalhos da mastectomia levando à necrose dos tecidos moles em curto prazo e afinamento significativo em longo prazo.
Devido à perda da borda lateral devido à grande bolsa de mastectomia, os retalhos do serrátil anterior são frequentemente usados para controlar a posição lateral do expansor e definir o SML ou linha axilar anterior.
Incisão
A incisão mais usada é uma elipse transversal, que oferece a oportunidade de diminuir o tamanho do envelope de pele com risco mínimo de comprometimento do retalho cutâneo. Também ajuda a esconder a cicatriz sob o sutiã.
Em mastectomias que preservam o mamilo, na maioria das vezes, uma incisão periareolar inferior foi usada. O tipo de mastectomia, a importância do manuseio suave do tecido, a preservação do SIM e da fáscia do serrátil e a minimização da dissecção lateral desnecessária da bolsa mamária são fatores cruciais a serem considerados.
Drenos
Em nosso centro, geralmente colocamos um dreno dentro da bolsa submuscular/MDA. Um segundo dreno é colocado ao longo da prega inframamária no plano subcutâneo e retirado através de uma incisão separada na linha axilar anterior. Os drenos são mantidos até que a produção caia abaixo de 30cc. Os antibióticos são prescritos rotineiramente por uma semana após ou até que os drenos sejam removidos
Período de expansão
A expansão geralmente começa um mês após a cirurgia e os volumes são limitados por desconforto e sinais de estresse na pele (branqueamento). A expansão é geralmente feita em 3 a 5 visitas ao ambulatório. A troca para implante é geralmente realizada de 6 meses a 1 ano após a cirurgia.
Escolha do implante
A seleção do tamanho começa durante a consulta inicial. Primeiro, as dimensões da parede torácica devem ser medidas com precisão, com foco na largura, altura e projeção da mama, permitindo ao cirurgião estimar o volume da mama.
De acordo com a literatura, sugere-se uma pequena sobrecorreção do peso da mastectomia para acomodar a frouxidão criada no envelope de pele devido à mastectomia13. Quase todos os implantes de alto perfil foram usados para a projeção máxima.
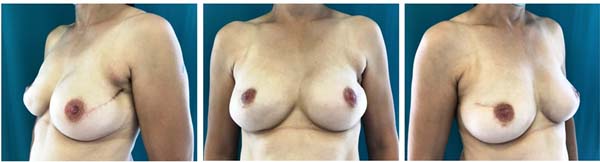
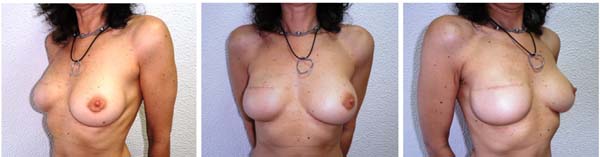
Um exemplo de paciente submetida a reconstrução imediata em dois estágios é retratado no caso clínico 2, paciente de 46 anos com diagnóstico de carcinoma ductal invasivo na mama direita (pré-operatório -Figura 3). A paciente foi submetida a mastectomia total e reconstrução imediata em dois estágios com expansor e posteriormente implante de 270 cc. A mama esquerda foi aumentada com um implante de 180 cc. A Figura 4 descreve o resultado final 2 anos depois. O paciente não desejava reconstruir o CAP.
Caso clínico 2: reconstrução imediata em dois estágios
Comparando complicações com a literatura
Em alguns artigos, complicações maiores foram relatadas com uma incidência geral tão baixa quanto 6% cada13,14.
Em outras séries, as complicações individuais, incluindo perda do implante, necrose da pele com necessidade de reoperação, infecção, hematoma, seroma e contratura capsular foram tão baixas quanto 2%13,14. Em nosso departamento, as taxas de complicações foram um tanto semelhantes a algumas séries da literatura, com porcentagem ligeiramente maior de formação de seroma, infecções (9,5%) e formação de hematoma (7,6%).
Comparando as reconstruções após mastectomia poupadora de NAC
Após mastectomias poupadoras de CAP, outra série de 500 reconstruções consecutivas em um estágio e em dois estágios mostrou taxas gerais de complicações baixas e perda de mamilo inferior a 10%. Além disso, o risco de infecção foi de 3,3%12.
Em nosso serviço, ocorreram dois casos de necrose mamilar total e um caso de infecção, perfazendo uma prevalência de 9,5% e 4,5%, respectivamente, para cada complicação.
O relatório multiinstitucional mais extenso comparando complicações precoces da reconstrução direta ao implante com a reconstrução em dois estágios encontrou uma taxa mais alta de complicações gerais (6,8% em comparação com 5,4%) e falha da prótese (1,4% em comparação com 0,8%) na direta -para a reconstrução do implante. No entanto, nenhuma diferença significativa foi encontrada em relação à infecção, reoperação ou complicações médicas maiores14.
Em nosso centro, apesar da ocorrência de uma maior porcentagem de complicações com a reconstrução em um estágio (56,8%) versus a reconstrução em dois estágios (39,3%), não conseguimos demonstrar qualquer significância estatística entre a reconstrução expansora e implante em termos de complicações: expansor (dois estágios) vs. RDI 39,3% vs. 56,8%, p = 0,077 (ns).
Considerações Especiais
Os pacientes tratados em 2019 ainda não desenvolveram complicações tardias. Algumas complicações como seroma e até complicações tardias como linfedema e dor crônica podem não ter sido registradas em nosso prontuário, levando à subestimação do número de casos.
O linfedema não é uma complicação da reconstrução da mama, mas sim uma complicação da mastectomia. Ainda assim, os autores decidiram que era relevante registrar o número de ocorrências.
CONCLUSÃO
Apesar de suas muitas vantagens, a reconstrução mamária imediata não é um procedimento simples e tem algumas limitações em comparação com a reconstrução tardia.
Fatores como a viabilidade do retalho cutâneo são de extrema importância para o sucesso do procedimento. Além disso, os pacientes devem estar cientes de que a equipe cirúrgica, em última instância, decide se deve realizar a reconstrução imediata na sala de cirurgia.
O consentimento assinado deve sempre ser obtido previamente, explicando que a reconstrução aloplástica imediata pode não ser possível e, consequentemente, adiada para uma configuração tardia.
Ocasionalmente, a equipe de reconstrução pode decidir realizar uma reconstrução imediata em dois estágios em vez de uma reconstrução RDI quando os retalhos de mastectomia são de viabilidade duvidosa. O consentimento deve sempre incluir a possibilidade de necrose parcial ou total do CAP e retalhos de mastectomia e falha na reconstrução.
Apesar de ser amplamente realizado, continua sendo um procedimento de alto risco com grande probabilidade de desenvolver complicações. Em nossa série, 47% dos pacientes desenvolveram alguma complicação, mesmo que pequena.
Nossa maior taxa de revisões em relação à literatura (40,5%) deveu-se em parte ao fato de considerarmos as revisões e os procedimentos secundários em conjunto. Isso inclui reconstrução do CAP, lipofilling, revisões de cicatriz, lipoaspiração e mastopexia, e geralmente foram realizadas na mesma cirurgia.
Gerenciando complicações
As complicações pós-operatórias devem ser tratadas agressivamente e em tempo hábil. Os seromas e hematomas devem ser drenados imediatamente para evitar o excesso de tensão nos retalhos cutâneos sobrejacentes e minimizar o mau posicionamento do implante a longo prazo.
A necrose do retalho cutâneo deve ser acompanhada de perto e, se não cicatrizar rapidamente, deve ser excisada e fechada principalmente para evitar a possibilidade de exposição do implante. A necrose da borda da pele (2 a 5 mm) geralmente pode ser tratada com desbridamento e fechamento sob anestesia local. Áreas maiores geralmente requerem a remoção do implante.
O que melhorar?
Há um valor de p estatisticamente significativo quando se compara a incidência de complicações precoces na população obesa com IMC acima de 30. No entanto, isso não era verdade para pacientes com sobrepeso e IMC entre 25 e 30. Portanto, uma maneira de diminuir a complicação taxas é selecionar pacientes com IMC abaixo de 30.
A seleção adicional de pacientes com IMC normal ou inferior a 30 pode ser uma forma de diminuir o percentual de complicações. Pacientes com sobrepeso e obesos devem ser encorajados a perder peso e podem ser submetidos a reconstrução tardia com mais segurança. Mais investigações ainda precisam ser feitas para descobrir um ponto de corte adequado do IMC.
Outros fatores comportamentais, como tabagismo, hipertensão e diabetes mellitus, causam impacto negativo nas taxas de complicações. Os pacientes devem ser encorajados a parar de fumar, pois a vasoconstrição causa um efeito deletério nos retalhos da mastectomia e na cicatrização de feridas. Os níveis de glicose no sangue também devem ser estritamente controlados. A hipertensão e, especialmente, os pacientes hipertensos mal controlados têm risco aumentado de desenvolver hematoma. Infelizmente, não havia dados suficientes disponíveis para avaliar a significância estatística desses fatores de risco neste ensaio.
A opinião dos autores é que pacientes previamente submetidos à radioterapia ou que provavelmente receberão radioterapia adjuvante não devem ser candidatos à reconstrução imediata aloplástica. Em vez disso, deve ser oferecida reconstrução autóloga retardada.
As novas tendências que favorecem a reconstrução aloplástica nesses pacientes, após a melhora da qualidade dos retalhos com lipofilling, fogem ao escopo deste artigo. Devido às fenestrações no MDA e à permeabilidade da loja da mastectomia, o dreno submuscular pode não ser necessário. Muitos centros estão usando apenas um dreno. A redução do número de drenos pode contribuir para diminuir a taxa de infecção.
Em relação ao uso de MDA, e embora a maioria dos implantes infectados/extrudados na reconstrução de RDI estivesse associada ao MDA13,14, não há dados suficientes para que esse fato seja estatisticamente significativo.
Em conclusão, a reconstrução aloplástica continua sendo o padrão ouro na reconstrução imediata da mama. Permite alcançar resultados esteticamente satisfatórios que perduram por muitos anos de vida. No entanto, isso tem suas limitações, especialmente no tratamento de mulheres jovens com expectativa de vida longa. Espera-se que essas mulheres sejam submetidas a vários procedimentos ao longo da vida, como substituição de implantes, e muitas desenvolverão contratura capsular.
Outras complicações também podem surgir, como o linfoma anaplásico de células grandes associado ao implante de mama (BIA-ALCL), uma malignidade embora muito rara que está ganhando destaque em conferências de cirurgia plástica em todo o mundo, uma vez que foi certamente esquecido e subdiagnosticado. Essas complicações são parte do fardo de carregar um implante mamário para o resto da vida.
Por tudo isso, é imprescindível investir mais na reconstrução autóloga imediata e oferecer rotineiramente essa opção aos pacientes mais jovens, principalmente com o retalho DIEP de última geração.
REFERÊNCIAS
1. Filip CL, Jecan CR, Raducu L, Neagu TP, Florescu IP. Immediate versus delayed breast reconstruction for postmastectomy patients. Controversies and solutions. Chirurgia (Bucur). 2017 Jul/Aug;112(4):378-86.
2. Gfrerer L, Mattos D, Mastroianni M, Weng QY, Ricci JA, Heath MP, et al. Assessment of patient factors, surgeons, and surgeon teams in immediate implant- based breast reconstruction outcomes. Plast Reconstr Surg. 2015 Feb;135(2):245e-52e.
3. Wilkins EG, Hamill JB, Kim HM, Kim JY, Greco RJ, Qi J, et al. Complications in postmastectomy breast reconstruction one-year outcomes of the mastectomy reconstruction outcomes consortium (MROC) Study. Ann Surg. 2018 Jan;267(1):164-70.
4. Berlin Nl, Tandon VJ, Qi J, Kim HM, Hamill JB, Momoh AO, et al. Hospital variations in clinical complications and patient-reported outcomes at 2 years after immediate breast reconstruction. Ann Surg. 2019 May;269(5):959-65.
5. Azouz V, Lopez S, Wagner DS. Surgeon-controlled comparison of direct-to-implant and 2-stage tissue expander-implant immediate breast reconstruction outcomes. Ann Plast Surg. 2017 Mar;80(3):212-6.
6. Rudolph M, Moore C, Pestana IA. Operative risk stratification in the obese female undergoing implant-based breast reconstruction. Breast J. 2019 Nov;25(6):1182-6. DOI: https://doi.org/10.1111/tbj.13434
7. Ilonzo N, Tsang A, Tsantes S, Estabrook A, Ma AMT. Breast reconstruction after mastectomy: a ten-year analysis of trends and immediate postoperative outcomes. Breast. 2017 Apr;32:7-12.
8. Azouz V, Lopez S, Wagner DS. Surgeon-controlled comparison of direct-to-implant and 2-stage tissue expander-implant immediate breast reconstruction outcomes. Ann Plast Surg. 2018 Mar;80(3):212-6.
9. Davila AA, Mioton LM, Chow G, Wang E, Merkow RP, Bilimoria KY, et al. Immediate two-stage tissue expander breast reconstruction compared with one-stage permanent implant breast reconstruction: a multi-institutional comparison of short-term complications. J Plast Surg Hand Surg. 2013 Oct;47(5):344-9.
10. Blacam C, Momoh AO, Colakoglu S, Slavin SA, Tobias AM, Lee BT. Cost analysis of implant-based breast reconstruction with acellular dermal matrix. Ann Plast Surg. 2012 Nov;69(5):516-20.
11. Gdalevitch P, Ho A, Genoway K, Alvrtsyan H, Bovill E, Lennox P, et al. Direct-to-implant single-stage immediate breast reconstruction with acellular dermal matrix: predictors of failure. Plast Reconstr Surg. 2014 Jun;133(6):738e-747e.
12. Colwell AS, Damjanovic B, Zahedi B, Medford-Davis L, Hertl C, Austen Junior WG. Retrospective review of 331 consecutive immediate single-stage implant reconstructions with acellular dermal matrix. Plast Reconstr Surg. 2011 Dec;128(6):1170-8.
13. Salzberg CA, Ashikari AY, Koch RM, Chabner-Thompson E. An 8-year experience of direct-to- implant immediate breast reconstruction using human acellular dermal matrix (AlloDerm). Plast Reconstr Surg. 2011 Feb;127(2):514-24.
14. Salzberg CA. Focus on technique: one-stage implant-based breast reconstruction. Plast Reconstr Surg. 2012;130(5 Suppl 2):95S-103S.
1. Centro Hospitalar e Universitário de
Coimbra, Coimbra, Portugal, Portugal.
JBF Análise e/ou interpretação dos dados, Aprovação final do manuscrito, Coleta de Dados, Conceitualização, Concepção e desenho do estudo, Gerenciamento do Projeto, Metodologia, Redação - Preparação do original, Redação - Revisão e Edição
RM Análise e/ou interpretação dos dados, Redação - Revisão e Edição
SS Análise e/ou interpretação dos dados, Análise estatística, Conceitualização, Investigação, Metodologia, Redação - Preparação do original
Autor correspondente: João Baltazar Ferreira, Rua Av Bissaya Barreto, Unidade Queimados, Blocos de Celas HUC, Coimbra, Portugal, CEP 3000-075, E-mail: joao_cbf@msn.com
Artigo submetido: 21/02/2021.
Artigo aceito: 19/04/2021.
Conflitos de interesse: não há.
Instituição: Centro Hospitalar e Universitário de Coimbra, Coimbra, Portugal.










 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter