

Articles - Year 2000 - Volume 15 -
Decúbito Dorsal no Retalho Microcirúrgico do Músculo Grande Dorsal - Técnica de J. M. Servant
Dorsal Decubitus in the Microsurgical Flap of Latissimus Dorsi - J. M. Servant Technique
RESUMO
Foram realizados 100 retalhos microcirúrgicos no Hospital da Universidade de Paris VII - Hospital Saint-Louis e estudados na Universidade Federal de São Paulo (UNIFESP) - Escola Paulista de Medicina (EPM) e Universidade Federal de Alagoas (UFAL). A sistematização do decúbito dorsal como posição no pré-operatório propiciou uma opção que facilitou a dissecção do retalho e a realização da cirurgia numa só posição; a equipe de anestesia pôde, então, trabalhar com uma posição definitiva, o que favoreceu a fixação do tubo endotraqueal e a monitoração dos parâmetros clínicos. Graças a esses fatores, a cirurgia foi realizada com segurança e conforto.
A média de 9 pacientes operados por ano confirmou a tendência de não se supervalorizar os retalhos microcirúrgicos. Não houve limites de idade que contra-indicassem a microcirurgia, que foi realizada em pacientes de 6 e 78 anos, com média de 37,8 anos. As regiões dos membros inferiores e a da cabeça foram as que tiveram maior indicação do retalho microcirúrgico do grande dorsal; a porcentagem de reintervenção cirúrgica foi de 11% devida à trombose; e a perda total do retalho foi de 4%, todos localizados em membros inferiores.
Palavras-chave:
ABSTRACT
100 microsurqical flaps were peiformed at the University Hospital of Paris VII - Hospital Saint-Louis and studied at the Federal University of São Paulo (UNIFESP) - Escola Paulista de Medicina (EPM) and Federal University of Alagoas (UFAL). The implementation of dorsal decubitus as preoperative position provided an option that eased the dissection of the flap and the performance of the surgery in a single position; the anesthetic team thus, could worl: with a definite position, which favored the fixation of the endotracheal tube and the monitoring of vital signs. Thank to these factors, the surgery was carried out with safety and comfort. The average of 9 surgery patients per year confirmed the tendency of not overestimating microsurqical flaps. There was no age limit that contraindicated microsurgery, which was carried out in patients with ages from 6 to 78 years old, with an average of 37.8 years. The areas of lower limbs and head were those which were most indicated for great dorsal microsurgical flap; the percentage of a new surgical intervention was 11% due to thrombosis; and total flap loss was 4%, all of them located at the lower limbs.
Keywords:
O Retalho do Músculo Grande Dorsal (RMGD), usado pela primeira vez em 1896(1) para reconstrução da região torácica após mastectomia, teve sua grande aceitação na Europa no início no século, com a divulgação proporcionada por importante trabalho em 1912(2). Sua aplicação em cirurgia reconstrutora obteve nova repercussão com a apresentação da rotação de um retalho músculo-fáscio-cutâneo em ilha do Músculo Grande Dorsal (MGD)(3) e com a descrição de dois casos de retalho microcirúrgico (RM) toracodorsal, no qual incluíram o segmento anterior do MGD(4). A seguir, foram publicados muitos trabalhos sobre a aplicação clínica do MGD(5). Esses autores apresentaram um caso de Retalho Microcirúrgico do Músculo Grande Dorsal (RMMGD), com o paciente em decúbito lateral, para a reconstrução e tratamento de uma osteomielite com exposição dos parietais no crânio.
Atualmente, o RMMGD é amplamente utilizado na cirurgia plástica, em função de sua anatomia pouco variável e de suas múltiplas aplicações(6,7,8). Em microcirurgia, muitas vezes o MGD é indicado para as reconstruções que envolvem as extremidades distais, como o vértice do couro cabeludo e a face plantar do pé. Na individualização e rotação do MGD, é de grande importância a posição do paciente no intra-operatório. Posicionando-o em decúbito ventral ou lateral para a dissecção do MGD, a transferência do retalho requer a mudança da posição durante a cirurgia, podendo aumentar a morbidade e o tempo da cirurgia. A possibilidade de usar o MGD em decúbito dorsal (DD) dispensa a mudança de posição do paciente e cria uma opção para as reconstruções microcirúrgicas.
Este estudo tem a finalidade de analisar os RMGDs realizados com o paciente em DD.
CASUÍSTICA E MÉTODO
Neste estudo foram avaliados retrospectivamente 100 casos de RMMGD realizados no Hospital da Universidade de Paris VII - Hospital Saint-Louis e estudados no Hospital São Paulo, Universidade Federal de São Paulo (UNIFESP) - Escola Paulista de Medicina (EPM) e no Hospital Universitário da Universidade Federal de Alagoas (UFAL). Todos os pacientes foram protocolados por meio de fichas uniformizadas e informatizadas, 56% dos pacientes eram do sexo masculino e 44% do feminino, com idade variando entre 6 e 78 anos (média 38 anos).
O pré-operatório e os procedimentos cirúrgicos de individualização dos RMGDs e seu posicionamento no leito da região receptora foram semelhantes em todos os casos. Certas precauções foram importantes antes da indicação cirúrgica do RMMGD, como a realização de anamnese e pesquisa de antecedentes de radiação e/ou de intervenção cirúrgica, tanto na área doadora quanto na receptora(9). Foi feita também a radiografia da coluna em crianças, para servir de padrão para futuras avaliações(7). Os exames complementares, como arteriografia e doppler, não foram solicitados por não serem considerados decisivos(10).
A avaliação dinâmica do MGD era realizada com o paciente de pé ou sentado, com o braço em adução forçada e as mãos sobre as cristas ilíacas.
A demarcação do limite medial era iniciada com o músculo em contração, com o objetivo de visualizar e palpar a margem medial do MGD(11); o eixo de rotação do retalho correspondendo à origem do pedículo vascular, situado no centro da fossa axilar, estando o braço em elevação e abdução completa.
Após a demarcação do retalho e anestesia inalatória com entubação endotraqueal, o paciente era posicionado em DD, com o braço em abdução sobre um apoio auxiliar de uma mesa de cirurgia da mão.
A seguir, colocava-se um coxim (um campo cirúrgico grande envolto sobre si mesmo com mais ou menos 30 cm de comprimento e 14 cm de diâmetro) longitudinal, ao longo da linha paravertebral, do lado a ser operado, de modo a elevar a porção lateral do paciente.
A abordagem do pedículo vásculo-nervoso era iniciada por incisão em "V" invertido na fossa axilar com ápice medial e com angulação de aproximadamente 140º, que envolvia a pele e o tecido celular subcutâneo. A seguir, a incisão era prolongada conforme o desenho do retalho desejado e sua constituição. Quando o retalho era muscular, o prolongamento era longitudinal, acompanhando a linha axilar média. Quando usado um retalho músculo-fáscio-cutâneo, o prolongamento obedecia à demarcação medial, observando-se as relações do MGD com os músculos da região do tórax e do abdome.
A incisão do segmento cutâneo-lateral obedecia à largura desejada para a cobertura do defeito cutâneo e partia da extremidade distal para a proximal, com o intuito de facilitar a abordagem da região do pedículo.
Os vasos sangüíneos da região receptora eram preparados para a anastomose microcirúrgica, quando então se realizava a secção do pedículo vásculo-nervoso após a individualização e liberação do retalho, que era colocado dentro de um recipiente estéril, com solução de Ringer lactato e heparina, na posologia de duas ampolas de 5 ml, com 5000 U/ml em cada 1000 ml de Ringer lactato em temperatura ambiente. Logo em seguida, realizava-se a aposição do RM na região receptora e iniciavam-se as suturas vasculares em artérias com 8 a 10 pontos separados, fios cirúrgicos poliamida (náilon) monofilamentar, cor preta, 8 zeros, 13 cm, 3/8 de círculo, agulha cilíndrica de aço de 0,6 cm com diâmetro de 150µ; já nas veias, a sutura era feita com oito pontos separados com fios cirúrgicos do mesmo tipo. Os clamps vasculares usados tinham pressão de 30-60 g/mm para artérias e veias com 1 a 2 mm de diâmetro.
Em todos os casos, a síntese da área doadora foi feita com pontos separados de apoio dérmico, usando-se fios absorvíveis sintéticos, com composição de ácido glicólico de 90% e ácido láctico de 10%, e agulhas cortantes, 3/8 de círculo, 3 cm de comprimento, cor violeta, com diâmetro de aproximadamente zero.
Nos casos de retalhos com ilha cutânea menor que 12 cm, a pele era suturada com pontos separados, com fios de poliamida (náilon) monofilamentar, de cor preta, 2 zeros, agulha cortante.
No pós-operatório imediato, os retalhos foram avaliados quanto a sua viabilidade, usando-se como parâmetros a coloração, a digitopressão, a temperatura e o sangramento da derme distal após puncturas ou escoriações com agulha.
Nos casos cirúrgicos envolvendo o membro inferior, este era mantido elevado por 3 semanas consecutivas.
Em todos os casos, o curativo foi feito com contenção uniforme sobre a margem do retalho coberto com gaze aberta e acolchoada (curativo confeccionado com algodão hidrófilo e hidrófobo envolto com gaze fina), sendo que, no centro do retalho, deixava-se uma abertura para visualizá-lo e monitorá-lo, com o intuito de observação no pós-operatório imediato e de acompanhamento rigoroso dos parâmetros clínicos nos 3 dias seguintes.
O pedículo vascular do RM cruzado, realizado em 7 pacientes, foi anastomosado temporariamente em vasos sangüíneos que estavam localizados a distância da região receptora. Essa variação da técnica obedeceu aos princípios do retalho cruzado(12,13).
A técnica em que o retalho é dobrado sobre si mesmo por um tempo variável (entre 3 e 7 dias) serve para verificar sua viabilidade vascular antes da exérese da lesão da região receptora.
RESULTADOS
Tabela I - Número de RMs retirados por ano.
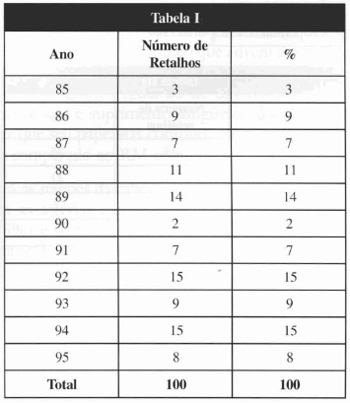
Tabela II - Área Receptora do RMMGD.
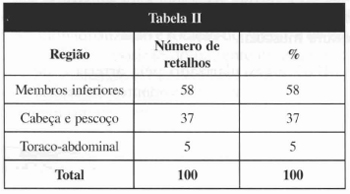
Tabela III - Distribuição dos RMs com relação à etiologia das lesões.
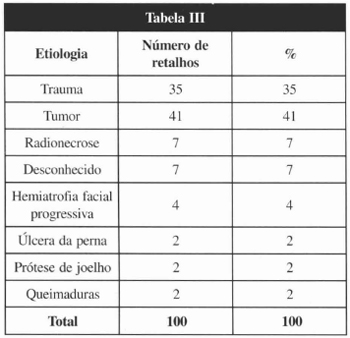
DISCUSSÃO
O MGD constitui um dos elementos mais importantes da parede póstero-lateral do tórax e a topografia do seu segmento lateral é de grande importância para a sua identificação durante a cirurgia. Esse músculo, além de volumoso, apresenta-se largo, porém de espessura fina, tendo base triangular e ápice externo-axilar(14), podendo ser usado para coberturas dos defeitos que exigem grande comprimento e pouca espessura muscular.
O MGD é vascularizado pela artéria e pela veia toracodorsal, ramos descendentes da artéria e veia subescapular, que possuem comprimento médio longo de 11 cm e pouca evidência de placa ateromatosa (8%)(14). Essas características são ideais para a realização de um RM.
Nos RMs estudados, foi realizada a dissecção do MGD com o paciente em DD, conforme outros(11). Tal fato foi importante no estabelecimento da sistematização do DD, como posição de possível realização cirúrgica, quando relacionada com as posições mais usadas, como decúbitos lateral e ventral.
O uso do DD viabilizou: a possibilidade de atuação concomitante de duas equipes, uma trabalhando na região doadora do retalho e a outra, na região receptora, o que pode colaborar para diminuir o tempo intra-operatório; a simplificação do ato cirúrgico, com maior conforto para o cirurgião, que pode realizar, sentado, toda a dissecção e hemostasia com mais facilidade, uma vez que não há mudanças do decúbito na totalidade dos casos; a síntese da área doadora torna-se mais fácil, podendo até ser realizada por uma outra equipe, enquanto o cirurgião concomitantemente pode iniciar a anastomose microcirúrgica; a abordagem do pedículo, que é curto quando penetra o MGD, estando perto da margem anterior do músculo, é facilitada com o DD e com o braço colocado naturalmente em abdução; a equipe de anestesia pode trabalhar com o paciente em uma posição definitiva, não sendo necessária a troca de decúbito e dos campos operatórios, pois o paciente é anestesiado em DD e permanece na mesma posição durante toda a cirurgia, o que facilita a fixação do tubo endotraqueal e a monitoração dos parâmetros clínicos.
Todos os pacientes foram submetidos à avaliação clínica laboratorial, sendo realizada a cirurgia só em pacientes hemodinamicamente estáveis. Foi solicitado aos pacientes fumantes que parassem de fumar três semanas antes da cirurgia. Autores relatam que o fumo não influência diretamente as possíveis complicações com o RM(10). Os portadores de doenças auto-imunes e Diabetes Mellitus só foram operados com os exames complementares dentro dos limites da normalidade(8).
Foram excluídos todos os pacientes com antecedentes de radioterapia ou cirurgia na região do pedículo vascular da área doadora, uma vez que a fibrose, provocada por radioterapia, compromete a possibilidade da realização de um RM, e a abordagem cirúrgica na região do pedículo pode, assim, causar lesão. A arteriografia e o doppler não foram considerados importantes, já que não trariam benefícios para a indicação cirúrgica e para o próprio paciente(7,15).
Foi considerada relevante a radiografia da coluna, em casos específicos, como os que envolvessem crianças, visto que poderia ocorrer modificação do plano frontal, diminuição da força muscular e desvio da coluna vertebral, após a liberação do retalho. Assim, a radiografia prévia serve de padrão para futuras avaliações da postura(7, 16).
É de importância cirúrgica a relação do MGD com as fibras do músculo oblíquo externo, precisamente sobre a face externa do arco posterior das quatro últimas costelas, pois, nessa região, há grande dificuldade de se separar o MGD - região, aliás, onde ocorre maior sangramento no ato cirúrgico(17).
A análise da média de 9 pacientes operados anualmente, no espaço de 10 anos dessa série de 100 casos, levou a crer que não houve, por parte dos serviços envolvidos (Hospital Saint-Louis/ Paris-França, Hospital São Paulo-Brasil e Hospital Universitário/ Maceió-Brasil) supervalorização das indicações dos RMs, pois os exemplos da literatura confirmam essa tendência(8, 10). Outro ponto a destacar: não houve limites de idade que contra-indicassem a microcirurgia, tendo sido realizada em pacientes de 6 a 78 anos de idade (com uma média de 37,8 anos).
A síntese da área doadora do retalho músculo-fáscio-cutâneo do MGD é um dos motivos pelos quais vários estudiosos do tema condenam a utilização do retalho com grande ilha cutânea (maior que 12 cm, há grande dificuldade para aproximar as margens da lesão). Nessa série de 100 pacientes, foram realizados 83 retalhos músculo-fáscio-cutâneos, e todos aqueles com ilha cutânea com largura menor do que 12 cm tiveram suas margens aproximadas com pontos de apoio dérmico(18).
Quanto à região dos membros inferiores e a da cabeça, com maior indicação do RMMGD, os resultados foram particularmente similares aos encontrados na literatura consultada(9,10,19). O RMMGD foi mais indicado em grandes perdas de substâncias diretamente relacionadas às extremidades do membro inferior e à cabeça, onde, ressalte-se, os retalhos músculos-fáscio-cutâneos não possuem capacidade de resolver determinados problemas, como o da exposição óssea ou osteomielite, que requer suprimento sangüíneo que só um músculo pode suprir. É importante ressaltar também que não há, nas regiões mais distais do corpo humano, retalhos pediculados que tenham condições de cobrir extensas perdas cutâneas.
As anastomoses cirúrgicas objetivaram a viabilidade máxima do RM, e as veias escolhidas para as anastomoses foram justamente as não comprimidas, tendo sido evitadas as regiões de flexão, com o paciente em DD. A propósito, a artéria e a veia de um RMMGD, em decorrência do alto débito sangüíneo, podem ser anastomosadas, sempre que necessário, com o auxílio de uma ponte de veia safena ou, preferencialmente, de veias do antebraço, já que essas veias possuem menor número de válvulas em relação àquela(20). Nos grandes retalhos músculo-fáscio-cutâneos utilizou-se o artifício de diminuir a quantidade de músculo em torno de pedículo, com a finalidade primeira de aumentar o fluxo sangüíneo direcionado para o retalho(12). Em alguns casos em particular, tal procedimento foi realizado com bons resultados, mas acredita-se que será necessário um ensaio clínico aleatório, para definir sua efetividade, e um estudo em animais de laboratório para comprovação de viabilidade vascular.
A porcentagem de reintervenção cirúrgica foi de 11%, em função da superveniência de trombose(8,21). Em 7% dos casos, houve completa viabilidade do retalho logo após o segundo ato cirúrgico; a porcentagem de perda total do retalho foi de 4%, todos em membros inferiores, sendo 3% de etiologia traumática. Acredita-se que a pequena porcentagem de perda total do RMMGD deve-se a suas características, como o pedículo vascular longo e de grosso calibre (em relação aos outros RMs), bem como a sua anatomia constante e presença limitada de placa ateromatosa no lúmen vascular das artérias subescapular e toracodorsal(6,10,14,15,19).
Nos membros inferiores, por ordem de preferência, foram feitas anastomoses término-terminais nas artérias tibiais anterior e posterior e nas veias safena interna, tibial anterior, tibial posterior e safena externa.
Quando não houve opção para realizar as anastomoses em vasos sangüíneos próximos à região da perda de substância, foram utilizados os vasos sangüíneos femorais (10,7%), realizando-se as anastomoses término-laterais com a utilização de ponte de veia safena ou do antebraço, no sentido de evitar trombose. Quando não foi possível realizar as anastomoses diretamente no membro que apresentava a lesão, foi adotado, então, o método do RM cruzado. Atualmente, opta-se pela utilização do retalho paraescapular cruzado, em decorrência da necessidade de ser sacrificado o MGD, quando da utilização deste como RM cruzado, já que, quando efetuada a secção do pedículo da anastomose, o músculo perderá seu suprimento sangüíneo e necrosará. Possivelmente, o inconveniente desse RM cruzado é que, após a secção da anastomose, ele se comportará como um "retalho parasita" (aquele que possui suprimento sangüíneo que advém das margens e do leito da área receptora) e não constituirá um aporte sangüíneo igual ao de um RMMGD, com anastomose e suprimento sangüíneo direto. Isso faz crer que seu papel nas consolidações ósseas não pode ser comparado ao RM comum(22).
Para as regiões da cabeça e do pescoço, foram utilizados as artérias carótida externa em término-lateral (25%) e os ramos da carótida externa em término-terminal (75%). Preferencialmente, escolheram-se as veias jugular externa em término-terminal (75%) e jugular interna em término-lateral (25%).
Acredita-se que a veia e a artéria temporal superficial são inadequadas como veia e artéria receptoras de um RM e, por princípio, optou-se sempre pelo sistema venoso jugular e pelos ramos da artéria carótida externa(12).
Na técnica do retalho dobrado, foi realizada a anastomose microcirúrgica, mas cumpre ressaltar que foi feita a aposição do retalho no segundo tempo da cirurgia, com o intuito de observar o suprimento sangüíneo e, desse modo, ter maior segurança de que se poderia, ali, apor o retalho. Esse procedimento foi usado unicamente em casos extremos, isto é, nos casos específicos em que os retalhos possuíam grandes dimensões ou naqueles decorrentes do estado geral da área receptora ou do próprio paciente que foi impelido a optar por essa técnica cirúrgica. Assim, retardou-se a exérese para poder então apor o retalho. A duração da internação, com média de 41 dias, está de acordo com a alta complexidade dos procedimentos e com as doenças envolvidas.
Por fim, salienta-se que o grau de dificuldade cirúrgica, com o paciente em DD, não possuiu, neste trabalho, um elemento de comparação, mas tornou essa posição exeqüível, já que todos os procedimentos cirúrgicos foram realizados em DD e não houve complicação estritamente decorrente da posição cirúrgica.
CONCLUSÃO
A dissecção do RMMGD é factível na posição operatória do paciente em decúbito dorsal.
BIBLIOGRAFIA
1. TANSINI I. Nuovo processo per I'amputazione della mammella per cancro. Riforma Med. 1896;1.
2. D'ESTE S. La technique de I'amputation de la mammelle pour carcinome mammaire. Rev. Chir. Orthop. Paris. 1912;45:164.
3. OLIVARI N. The latissimus dorsi flap. Brit. J. Plast. Surg. 1976;29:126-8.
4. BAUDET J, GUIMBERTEAU J, NASCIMENTO E. Successful clinical transfer of two free thoracodorsal axillary flaps. Plast. Reconstr. Surg. 1976;58:680-8.
5. MAXWELL GP, STUEBER K, HOOPES JE. A free latissimus dorsi myocutaneo flap. Plast. Reconstr. Surg. 1978;62:462-6.
6. LEGRE R, BARDOT O, KEVORKIAN B, VASSE D, EMRAM A, AUBERT JP, MAGALON G, BUREAU H. Evaluation of 106 free flaps. Analysis of the failures and the indications. Ann. Chir. Plast. Esthet. 1989;34:385-9.
7. LEGRE R, BOGHOSSIAN V, SERVANT JM. Analyse des séquelles du prélèvement du lambeau de grand dorsal (à propos de quarante quatre cas revus et testés) Ann. Chir. Plast. Esthet. 1990;35:512-7.
8. GLICKSMAN A, FERDER M, CASALE P, POSNER J, KIM R, STRAUCH B. 1457 Years of microsurgical experience. Plast. Reconstr. Surg. 1997;100:355-67.
9. HIDALGO DA, CARRASQUILO IM. The treatment of lower extremity sarcomas with excision, radiotherapy and free flap reconstruction. Plast. Reconstr. Surg. 1992;89:96-101.
10. KROLL SS, SCHUSTERMAN MD, MARK A, REECE MD, GREGORY P, MILLER MD, EVANS MD, GREGORY R, ROBB MD, GEOFFREY L, ROBB MB, BONNIE J, BALDWIN MD. Choice of Flap and incidence of Free Flap Success. Plast. Reconstr. Surg. 1996;98;459-63.
11. MOLE B, SERVANT JM, BANZET P. Le prélèvement du lambeau de grand dorsal en decubitus dorsal. Ann. Chir. Plast. Esthet. 1986;31:79-81.
12. REVOL M, VERGOTE T, SERVANT JM, BANZET P. Transferts tissulaires libres en chirurgie plastique (urgences exclues): A propos d'une experience de dix ans. Ann. Chir. Plast. Esthet. 1992;37:450-9.
13. DING SY. Treatment of chronic osteomyelitis of leg with free latissimus dorsi musculocutaneous flap anastomosed to contralateral leg vessels. Chung Hua Cheng Hsing Shao Shang Wai Ko Tsa Chih. 1993;9(2):106-7,159.
14. BARTLETT SP, MAY JW, YARENCHUK MJ. The latissimus dorsi muscle: a fresh cadaver study of the primary neurovascular pedicle. Plast. Reconstr. Surg. 1981;67:631-6.
15. HIDALGO DA, JONES CS. The role of emergent exploration in free tissues transfer: A review of 150 consecutive cases. Plast. Reconstr. Surg. 1990;492-8-86.
16. FRAULIN F, LOUIE G, ZORRILLA L, TILLERY W. Functional evaluation of the shoulder following latissimus dorsi muscle transfer. Ann. Plast Surg. 1995;35:349-55.
17. FRIEDRICH W, HERHOLD C, LIERSE W. Vascularization of the myocutaneous latissimus dorsi flap. Injection study on the thoracodorsal artery. Acta Anat. 1988;131:97-102.
18. BRICOUT N, SERVANT JM. Fermature de la zone de prélèvement dun lambeau de grand dorsal. Ann. Chir. Plast. Esthet. 1987;2:228-7.
19. FEARON JA, CUADROS CL, MAY JW. Flap failure after microsurgical free tissue transfer: The fate of a second attempt. Plast. Reconstr. Surg. 1990;86:746-51.
20. TESTUT L. Traité d'anatomie humaine. 7ème. ed. Paris, Octave Doin, 1921. 3 vols.
21. JONES NF, JOHNSON JT, SHESTAK KC, MYERS EN, SWARTZ WM. Microsurgical reconstruction of the head and neck: interdisciplinary collaboration between head and neck surgeons and plastic surgeons in 305 cases. Ann. Plast. Surg. 1996;36:37-43.
22. CARIOU JL. Transferts tissulaires libres en chirurgie plastique (urgences exclues) a propos d'une experience de dix ans. Ann. Chir. Plast. Esthet. 1992;37:460-1. [Comentaire].
I. Chefe do Serviço de Cirurgia Plástica Reconstrutora da Universidade Federal de Alagoas (UFAL) - Brasil.
II. Chefe do Serviço de Cirurgia Plástica do Hospital Saint-Louis - Paris - França.
III. Chefe do Serviço de Cirurgia Plástica da UniFESP - São Paulo - Brasil.
IV. Adjunto do Serviço de Cirurgia Plástica do Hospital Saint-Louis - Paris - França.
V. Adjunto do Serviço de Cirurgia Plástica da UniFESP - São Paulo - Brasil.
VI. Estudante de Medicina da Universidade Federal de Alagoas - Brasil.
Endereço para correspondência:
Centro de Saúde (CSAU)
Campus Universit. A. C. Simões BR 101 Norte Km 14
Maceió - AL - 57081-000
Fone/Fax: (82) 221-5081
Dept. Clínica Cirúrgica - Disciplina de Cirurgia Plástica Reconstrutora - Prof. Dr. Fernando Antônio Gomes de Andrade


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter