

35ª Jornada Sul Brasileira de Cirurgia Plástica - Year 2019 - Volume 34 - (Suppl.1)
Tratamento conservador em infecção de prótese mamária: relato de caso
Conservative treatment in breast prothesis infection: case report
RESUMO
A mamoplastia de aumento teve um crescimento de 64% no número de procedimentos realizados desde o ano 2000, tornando-se um dos procedimentos cirúrgicos estéticos mais realizados no mundo. Dentre as complicações pós-operatórias, as mais comumente relatadas são infecção, hematoma e contratura capsular. A infecção pós-operatória é uma complicação pouco comum no implante de prótese mamária, ocorrendo em cerca de 2% nos casos estéticos. Este trabalho tem como objetivo relatar o caso de uma paciente que evoluiu com infecção de prótese mamária em pós-operatório precoce, sendo submetida a tratamento conservador com sucesso sem necessidade de intervenção cirúrgica.
Palavras-chave: Implante mamário; Infecção; Cirurgia plástica; Mamoplastia
ABSTRACT
Breast augmentation has increased 64% since 2000, and became one of the most common surgical procedures in the world. The most common postoperative complication are infection, bruise and capsular contraction. The postoperative infection is uncommon, and occurs in 2% of cosmetic surgeries. This case reports a successful nonsurgical treatment of breast implant infection.
Keywords: Infection; Breast implants; Plastic surgery
INTRODUÇÃO
No Brasil e no mundo, vem aumentando o número de pacientes que se submetem a realização de cirurgia estética ou reparadora com uso de prótese mamária. A mamoplastia de aumento teve um crescimento de 64% no número de procedimentos realizados desde o ano de 2000, tornando-se um dos procedimentos cirúrgicos estéticos mais realizados no mundo. No Brasil, é o segundo procedimento cirúrgico estético mais realizado6.
As próteses de silicone podem ser colocadas sob o músculo peitoral (submuscular), sob a glândula mamária (subglandular) ou por técnica dual plane, na qual a prótese contempla os dois planos. As técnicas de inserção da prótese podem ser inframamária, transaxilar, periareolar ou transareolar. No Brasil, a abordagem mais usada é a inframamária, usando-se o sulco mamário para a inserção da prótese, o que limita o risco de contaminação pela flora endógena da mama, porém resulta em cicatriz visível.
Dentre as complicações pós-operatórias, as mais comumente relatadas são infecção, hematoma e contratura capsular, mas suas frequências diferem7. Um estudo retrospectivo realizado com 3.002 mulheres com aumento estético primário de mama evidenciou frequência de 4,6% de complicações, sendo essas com hematomas em 1,5%, contraturas capsulares em 0,5% e infecções representando 1,1%8. Em outro estudo prospectivo realizado na Dinamarca em 1.090 mulheres submetidas a aumento estético de mama, foram observadas 4,1% com contratura capsular, 1,1% com hematomas e 0,8% registradas com infecção9.
A mama humana não é uma estrutura estéril, pois contém a flora endógena derivada do mamilo. Essa flora pode ser responsável pela contaminação da prótese no momento da implantação, em particular quando se usam técnicas cirúrgicas com abordagem via periareolar ou transareolar9.
A infecção pós-operatória é uma complicação pouco comum no implante de prótese mamária, ocorrendo em cerca de 2% nos casos estéticos1 e até 20% nas cirurgias reconstrutivas,2 sendo que em 2/3 dos casos, a infecção ocorre dentro dos 12 meses do pós-operatório3. Apesar de incomum, a infecção periprotética é a complicação mais temida e que inclusive pode levar ao óbito por choque tóxico-infeccioso2. Entre esses casos, a grande maioria das infecções são causada por bactérias Gram-positivas, especificamente o Staphylococcus aureus e Staphylococcus epidermidis1.
Associado aos procedimentos de assepsia e antissepsia, para o implante de próteses é recomendável o uso profilático de antibióticos que se concentram na atividade das bactérias em questão, recomendando-se o uso de cefalosporina de primeira geração, como a cefazolina intravenosa (1 g administrado dentro de 30 minutos antes da incisão e por até 10 dias no pós-operatório.)1.
Como qualquer colocação de implante, as medidas de prevenção de infecção devem ser tomadas. A Sociedade Francesa de Higiene Hospitalar (SFHH), em um consenso em 2004, sugere medidas como rastreamento de transporte nasal de S. aureus; tratamento com mupirocina; profilaxia antibiótica intravenosa na indução anestésica; não depilação ou, em caso de depilação, realizar tricotomia fora do quarto; banho com antisséptico no dia anterior e na manhã da operação no campo cirúrgico; não secar o antisséptico; evitar tecidos 100% algodão; Mminimizar a exposição ao ar e manipulações dos implantes; hemostasia.
Após identificado o quadro de infecção dos implantes mamários, embora tenhamos poucos estudos na literatura como proposta de protocolo no tratamento, sugere-se a utilização de antibioticoterapia, irrigação e a remoção precoce do implante mamário para evitar a extrusão do implante e contratura tecidual3, e a reinserção tardia após o desaparecimento do processo infeccioso4, por pelo menos após 6 meses5, gerando importantes implicações psicológicas para a paciente.
OBJETIVO
Este trabalho tem como objetivo relatar o caso de uma paciente que evoluiu com infecção de prótese mamária em pós-operatório precoce, sendo submetida a tratamento conservador com sucesso sem necessidade de intervenção cirúrgica.
MÉTODO
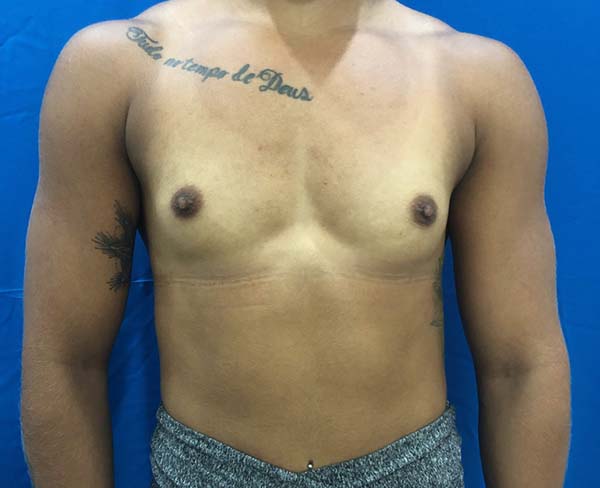
BMS, feminina, 19 anos, submetida a mamoplastia de aumento no dia 18 de dezembro de 2018, por meio de técnica dual plane, prótese Polytech, 300 mL, extra alto, microtexturizada.
Técnica utilizada: (1) paciente em decúbito dorsal, submetida a anestesia geral; (2) assepsia e antissepsia e colocação de campos estéreis; (3) infiltração com solução anestésica e incisão em sulco inframamário; (4) dissecção do plano subglandular até a região do bordo inferior da aréola onde foi divulsionado e dissecado o plano submuscular; (5) realizado revisão de hemostasia rigorosa, lavagem da loja com SF 0,9% e keflin; (6) colocação de próteses bilateralmente e dreno de portovac; (7) fechamento em três planos com náilon 3.0, 4.0 e monocryl 4.0; (8) curativo e soutien cirúrgico.
Paciente recebeu profilaxia com keflin 1 g, endovenosa, 30 minutos antes da incisão anestésia e a cada 6 horas por dia via endovenosa. Recebeu alta na manhã seguinte com recomendações e uso de ciprofloxacino por 7 dias.
RESULTADOS
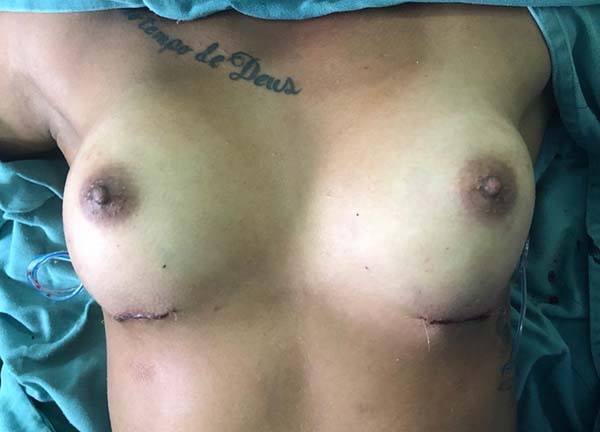
Primeiro retorno foi realizado com 9 dias, paciente com ótima evolução pós-operatória. Ao 12º dia pós-operatório, paciente relata por meio de contato com médico assistente a saída de secreção purulenta em incisão inframamária direita. Paciente foi atendida e evidenciado por meio de exame físico a saída de grande quantidade de secreção purulenta. Foi iniciada antibioticoterapia com amoxicilina + clavulanato 875 mg associada à clindamicina 300 mg empiricamente e foi coletado material para cultura. Foi optado pela equipe a limpeza diária da loja com soro fisiológico 100 mL enquanto aguardava resultado da cultura.
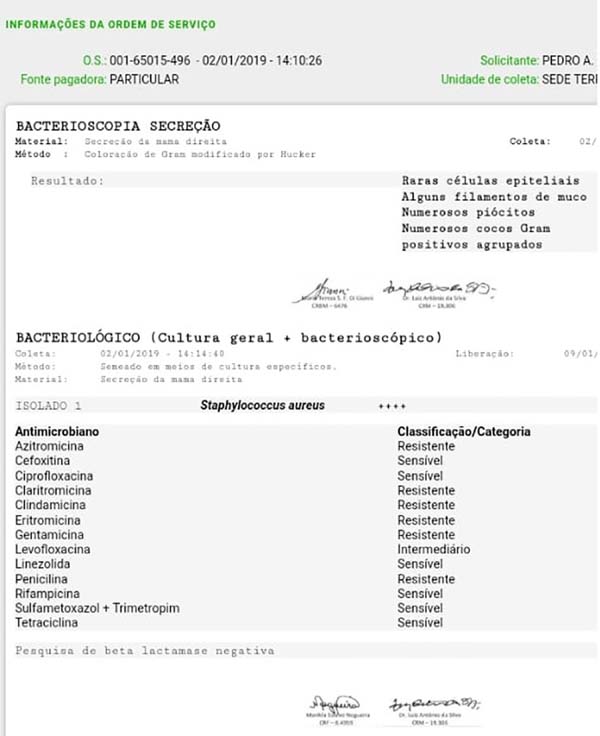
Resultado da cultura (Figuras 1, 2 e 3) demonstrou contaminação por Staphylococcus aureus sensível a sulfametoxazol + trimetropim e resistente à antibioticoterapia inicialmente utilizada; foi optado então pela troca da medicação e manutenção da limpeza diária com 100 mL de soro fisiológico 0,9%.
A paciente foi mantida com a conduta por 25 dias, com melhora diária significativa e parada total da eliminação de líquido purulento. Após esse período foram realizados pontos de reforço na incisão e solicitada ultrassonografia de controle; esta foi realizada com 42 dias de pós-operatório e laudo apresentou-se sem alterações detectáveis ao método (Figuras 4 e 5).
DISCUSSÃO
A infecção é sem dúvida uma das complicações mais temidas após colocação de prótese mamária, traz consigo uma série de dúvidas para a equipe médica e pode abalar seriamente a relação médico/paciente. A literatura sobre o assunto relata uma taxa de infecção entre 1% a 35% dos casos; em sua grande maioria esses estudos abordam infecção de próteses após mastectomias. A terapia com antibiótico é sem dúvida a mais conservadora, porém seus resultados são inconsistentes: sucesso sem necessidade de remoção da prótese em menos de 25% dos casos10.
CONCLUSÃO
Atualmente não há nenhum protocolo sobre o assunto, orientação sobre o tempo de antibiótico pós-operatório ou conduta definida após diagnóstico de infecção. Sabe-se que na grande maioria dos casos a retirada da prótese é inevitável. Este relato de caso abre a discussão para realização de estudos mais específicos e montagem de protocolos específicos para segurança da equipe cirúrgica e do paciente.
REFERÊNCIAS
1. Feldman EM, Kontoyiannis DP, Sharabi SE, Lee E, Kaufman Y, Heller L. Breast Implant Infections: Is Cefazolin Enough? Division of Plastic Surgery, Baylor College of Medicine, and the Department of Infectious Diseases, Infection Control and Employee Health, University of Texas; 2010.
2. Atallah D, Kassis N, Araj G, Nasr M, Nasnas R, Veziris N, et al. Mycobacterial Infection of Breast Prosthesis - A Conservative Treatment: A Case Report. BMC Infect Dis. 2014; 14:238. DOI: https://doi.org/10.1186/1471-2334-14-238
3. Laveaux C, Pauchot J, Loury J, Leroy J, Tropet Y. Acute Periprosthetic Infection after Aesthetic Breast Augmentation. Report of Three Cases of Implant "Salvage". Proposal of a Standardized Protocol of Care. Ann Chir Plast Esthét. 2009; 54:358-64. DOI: https://doi.org/10.1016/j.anplas.2009.02.006
4. Chun JK, Schulman MR. The Infected Breast Prosthesis after Mastectomy Reconstruction: Successful Salvage of Nine Implants in Eight Consecutive Patients. Mount Sinai Medical Center. Plast Reconstr Surg; 2006.
5. Luzzati R, Sanna A, Allegranzi B, Nardi S, Berti M, Barisoni D, et al. Pharmacokinetics and Tissue Penetration of Vancomycin in Patients. J Antimicrob Chemother. 2000; 45:243-5.
6. Maximiliano J, Oliveira ACPO, Lorencetti E, Bombardelli J, Portinho CP, Deggerone D, et al. Mamoplastia de aumento: correlação entre o planejamento cirúrgico e as taxas de complicações pós-operatórias. Rev Bras Cir Plást. 2017; 32(3):332-9.
7. Hvilsom GB, Hölmich LR, Henriksen TF, Lipworth L, McLaughlin JK, Friis S. Local Complications after Cosmetic Breast Augmentation. Plast Surg Nurs; 2010. PMID: 20814274
8. Araco A, Gravante F, Araco D, Delogu V, Cervelli K, Walgenbach. A Retrospective Analysis of 3,000 Primary Aesthetic Breast Augmentations: Postoperative Complications and Associated Factors. Aesth Plast Surg. 2007; 31:532-9. DOI: https://doi.org/10.1007/s00266-007-0162-8
9. Pittet B, Montandon D, Pittet D. Infection in breast implants. Lancet Infect Dis. 2005; 5:94-106. DOI: https://doi.org/10.1016/S1473-3099(05)70084-0
10. Rivera M, Moon W. Breast Implant Infection Can be Successfully Treated with Nonsurgical Therapy. Plast Reconstr Surg Glob Open. 2017 set; 5(supl 9):56-7.
1. Serviço de Cirurgia Plástica Dr. Ewaldo Bolivar
de Souza Pinto, São Paulo, SP, Brasil.
2. Sociedade Brasileira de Cirurgia Plástica, São
Paulo, SP, Brasil.
Endereço Autor: Pedro Cordova Avenida Ana Costa, nº 120 - Gonzaga, Santos, SP, Brasil CEP 11060000 E-mail: pedro_cordova@hotmail.com







 Read in Portuguese
Read in Portuguese
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter