

Special Article - Year 2019 - Volume 34 -
Complicação grave do uso irregular do PMMA: relato de caso e a situação brasileira atual
Severe complication due to inappropriate use of polymethylmethacrylate: a case report and current status in Brazil
RESUMO
Introdução: Os preenchedores permanentes, apesar de resultados duradouros, são verdadeiros problemas quando causam complicações. No Brasil, o PMMA é um produto aprovado pela Anvisa, mas seu uso extrapola suas indicações, levando a complicações graves. Há mais de uma década, existem recomendações sobre sua restrição, mas casos com consequências graves do seu uso irresponsável são atuais.
Objetivo: Relatar complicação grave do uso irregular do PMMA e discutir a realidade brasileira atual baseado em determinações das entidades médicas, assim como dos órgãos reguladores.
Métodos: É relatado um caso de necrose extensa da região glútea após a injeção de PMMA por profissional não qualificado e discutida a situação brasileira atual do produto com base nas entidades médicas e revisão da literatura do Brasil.
Discussão: Apesar do esforço das entidades médicas, são inúmeros os casos de complicações agudas e crônicas relatados na literatura brasileira. No ano de 2016, foram registradas mais de 17 mil complicações relacionadas ao PMMA, mesmo assim, é difícil estabelecer dados epidemiológicos confiáveis, pois não há controle do número de aplicações, da qualidade do produto utilizado e da capacitação dos profissionais que o utilizam.
Conclusão: No Brasil, há um número expressivo de procedimentos reparadores para correção de complicações decorrentes do uso do PMMA. A gravidade do caso relatado traz à tona a necessidade de combate à má prática por profissionais não capacitados, assim como um controle mais rigoroso da comercialização do produto por entidades reguladoras.
Palavras-chave: Polimetil metacrilato; Preenchedores dérmicos; Brasil; Agência Nacional de Vigilância Sanitária; Conselhos de saúde; Procedimentos cirúrgicos reconstrutivos/efeitos adversos
ABSTRACT
Introduction: Use of permanent fillers can lead to significant complications. In Brazil, polymethylmethacrylate (PMMA) is a product approved by the Agência Nacional de Vigilância Sanitária (ANVISA), but its use exceeds its indications, leading to serious complications. Recommendations for restricted use have been in place for more than a decade, but cases with serious consequences due to inappropriate use are still seen.
Objective: To report a serious complication due to inappropriate use of PMMA and discuss the current status of PMMA use in Brazil based on recommendations of medical societies and regulatory agencies.
Methods: This report describes a case of extensive necrosis of the gluteal region after injection of PMMA by a non-qualified practitioner; the report also reviews the literature on the current status of PMMA use in Brazil.
Discussion: Despite the efforts of medical societies, acute and chronic complications are still reported in the Brazilian literature. In 2016, more than 17,000 PMMArelated complications were reported; nevertheless, reliable epidemiological data remain unavailable because the number of treatments, the quality of the product, and the training of practitioners remain unregulated.
Conclusion: A significant number of repair procedures are performed in Brazil to correct complications resulting from the use of PMMA. The severity of the reported case highlights the need to combat bad practice by untrained professionals, as well as the need for greater control of PMMA marketing by regulatory agencies.
Keywords: Polymethylmethacrylate; Skin fillers; Brazil; National Health Surveillance Agency; Health advice; Reconstructive surgical procedures/adverse effects
INTRODUÇÃO
Os preenchedores de volume na medicina estética podem ser divididos em 2 grupos principais: os preenchedores absorvíveis e os permanentes1. Entre as vantagens dos absorvíveis está a reversibilidade de resultados indesejados, seja por ação de um “antídoto” ou pela reabsorção do próprio organismo. No caso dos permanentes, apesar de resultados mais duradouros, complicações tornam-se um verdadeiro problema devido à persistência do produto no organismo e perpetuação do resultado indesejado2.
Essas complicações são inerentes a todos os tipos de preenchedores e podem ser classificadas em agudas e crônicas. Entre as agudas, podemos destacar embolia vascular, necrose, reação alérgica e infecção. Nas crônicas há a formação de granulomas, deformidades e reação inflamatória crônica2.
As complicações agudas merecem destaque por dependerem diretamente da qualificação e treinamento do profissional. Em sua maior parte, esse tipo de complicação está mais relacionado à técnica de aplicação e não necessariamente ao produto utilizado3.
O preenchedor permanente mais utilizado atualmente é o polimetilmetacrilato (PMMA). Trata-se de um polímero de microesferas que variam de tamanho de 30 a 103µm. Essas microesferas são diluídas em veículo próprio de colágeno bovino, carboximetilcelulose ou hialuronato de sódio, que são reabsorvidos após alguns dias pelo organismo2.
Desde 2006, o U.S. Food and Drug Administration (FDA) aprova a sua aplicação (ArteFill®), exclusiva por médicos, para o uso restrito do aumento de volume ao redor da boca (exemplo: sulco nasolabial), com exceção dos lábios4. No Brasil, a Agência Nacional de Vigilância Sanitária (Anvisa) recomenda o seu uso por profissionais médicos capacitados, não contraindica o seu uso para preenchimento corporal, como também não cita diretrizes para seu uso estético5.
Por ser um produto barato e de fácil obtenção, há inúmeros casos de complicações decorrentes de profissionais não capacitados e em centros de estéticas inadequados. O objetivo deste estudo é relatar um caso de aplicação do preenchedor em clínica clandestina na cidade de São Paulo com evolução dramática e discutir a realidade atual do PMMA no Brasil.
RELATO DE CASO
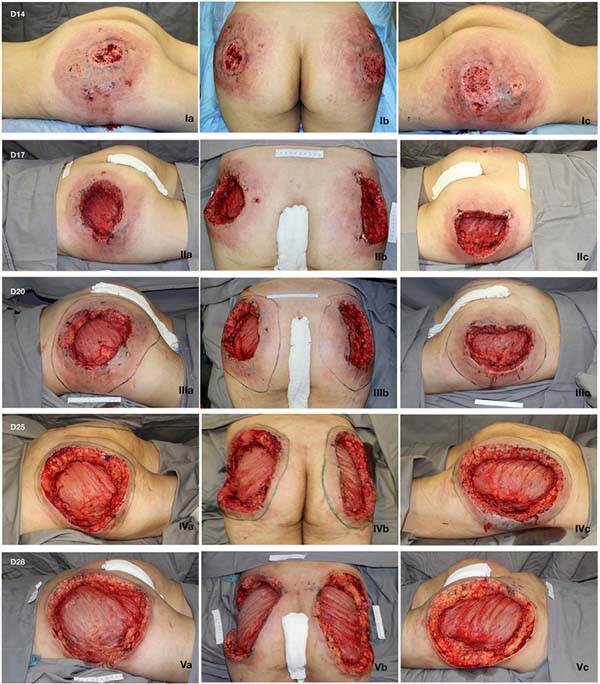
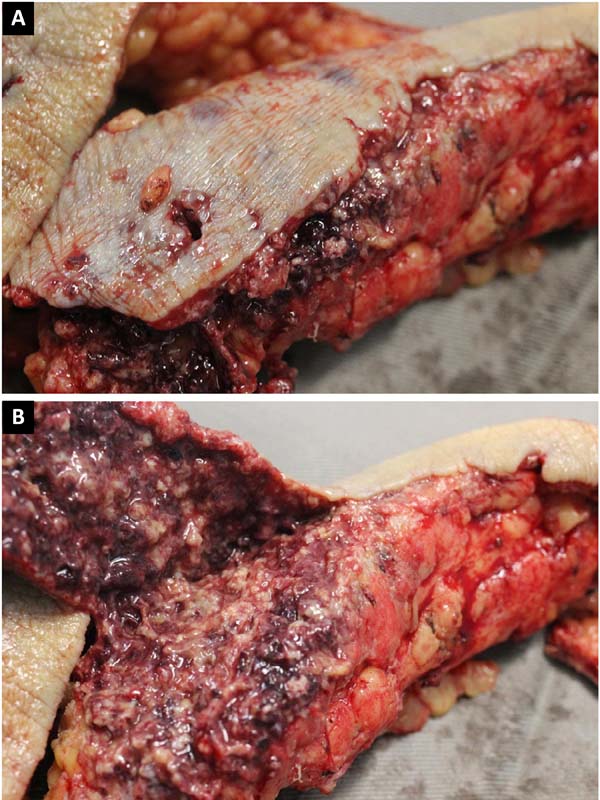
Paciente feminina de 21 anos atendida com história de injeção de 900ml de PMMA em glúteos há 12 dias. Procedimento realizado em salão de beleza por profissional não médico. Chega com quadro de dor e feridas ulceradas com secreção purulenta em local de aplicação (Figura 1). Já havia recebido tratamento prévio com os antibióticos ciprofloxacino e clindamicina por 7 dias (sem melhora) e mais ceftriaxona e prednisona em regime de hospital dia.
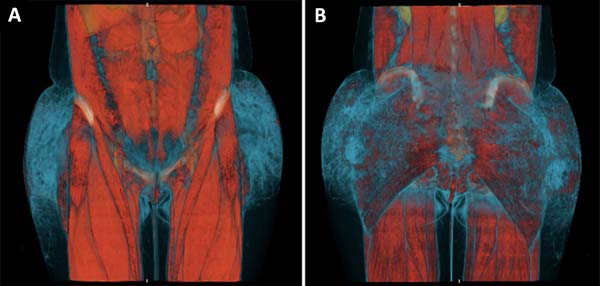
Na admissão, apresentava-se afebril e estável hemodinamicamente. Exames laboratoriais mostravam leucocitose, proteína C reativa elevada e tomografia computadorizada com evidência de espessamento e densificação da pele e tecido celular subcutâneo das regiões glúteas, além de múltiplas formações nodulares que poderiam corresponder à material exógeno/granulomas (Figura 2), sem evidência de coleções.
Inicialmente, submetida a antibioticoterapia empírica de amplo espectro, evoluiu com piora da ferida. Foram realizados desbridamentos seriados (Figura 1) com instalação de terapia por pressão negativa de forma contínua a 125mmHg e trocas sequenciais com intervalo de 3 a 5 dias. Achado de supuração e necrose da derme (Figura 3) e tecido celular subcutâneo com formações nodulares contendo pus e material exógeno, além de sinais de fasceíte do músculo glúteo máximo bilateralmente. Enviados fragmentos de partes moles para cultura, não sendo identificado nenhum micro-organismo.
Devido ao processo inflamatório/infecioso, permaneceu em leito de UTI por 14 dias, evoluindo com insuficiência renal aguda. Apresentou melhora progressiva após o 3º desbridamento.
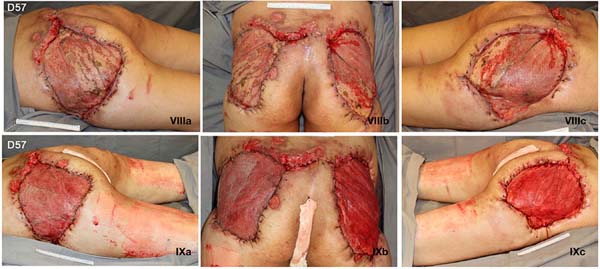
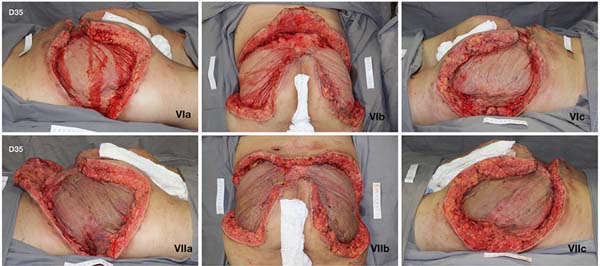
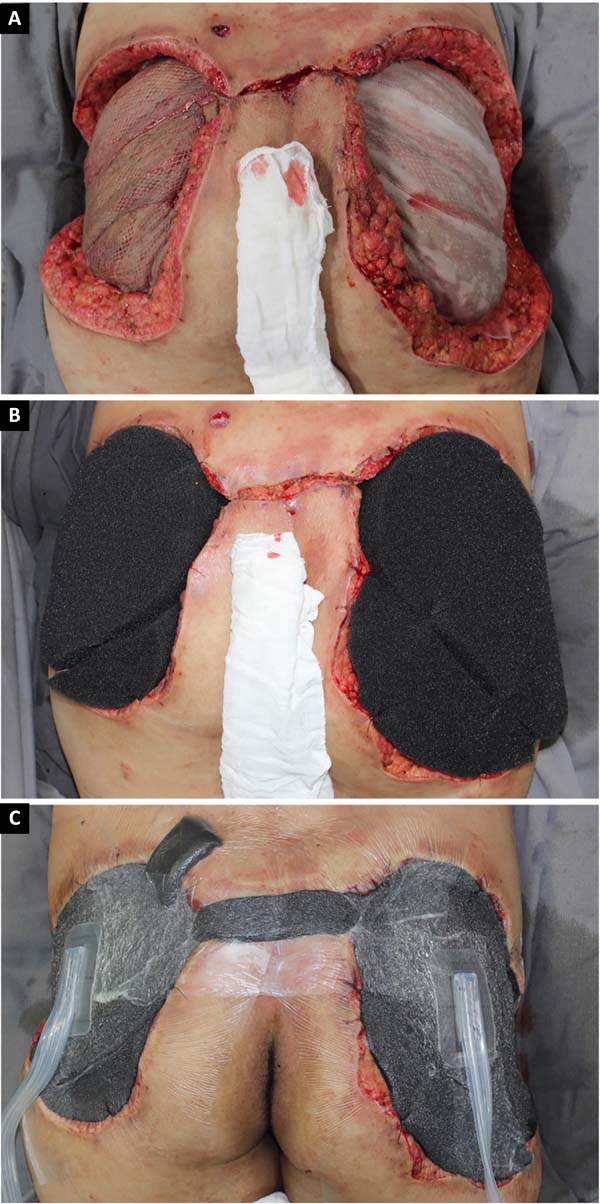
Tendo em vista as dimensões da ferida após os procedimentos de desbridamento sequenciais e o grau elevado de espoliação de nutrientes, hemoglobina e microelementos, optou-se pela enxertia de pele homógena sobre o músculo glúteo máximo bilateralmente (Figura 4), com instalação de terapia por pressão negativa (Figura 5).
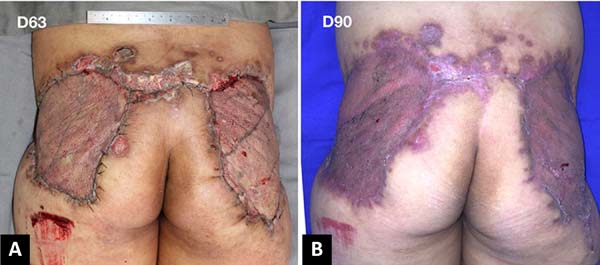
Após 3 semanas com curativo biológico (enxerto homógeno) e melhora dos parâmetros nutricionais, realizada enxertia de pele autóloga (Figura 6) em malha 1:1,5. Paciente evolui com boa integração do enxerto (Figura 7), sem déficits funcionais, recebendo alta hospitalar após 68 dias de internação.
PMMA no Brasil
Para fim reparador, desde 2004, o uso do PMMA para o tratamento de paciente portador de HIV com síndrome lipodistrófica é garantido por lei federal6. Para fins estéticos, entretanto, o seu uso indiscriminado mereceu alerta público do Conselho Federal de Medicina (CFM) em 2006 devido à aplicação sem embasamento científico, por profissionais não qualificados, e propaganda fantasiosa e exagerada da técnica conhecido por “bioplastia”7.
A Anvisa, em 2007, proibiu a manipulação do PMMA em farmácias de produtos compostos com a finalidade de regular a qualidade, características e pureza do produto8.
Em 2008, uma série de 32 casos de complicações referentes ao uso PMMA classificou as mesmas em 5 grupos: necrose, granulomas, reação inflamatória crônica, complicações em lábios, infecção. Observou-se que a necrose é sempre uma complicação aguda, enquanto as complicações inflamatórias podem ocorrer muitos anos após a injeção. Destacou-se a raridade das complicações, mas com a ressalva da dificuldade de estimar a incidência e prevalência em toda a população. Além disso, alertou-se sobre a preocupação com complicações graves, que, além de permanentes, muitas vezes são intratáveis2.
Em 2009, em outra série de casos com 18 pacientes com complicações diversas referentes ao PMMA, destacou-se o uso indiscriminado dessa substância devido ao baixo custo e à falta de controle de sua venda, sendo aplicado por médicos sem especialização e não médicos9. Em 2012, um estudo histopatológico de 63 casos de complicação atribuídas ao PMMA revelou 5 desses casos com complicações agudas, todas evoluindo com necrose após a injeção10.
Em 2010, em questionamento sobre o uso do PMMA em aumento glúteo, o Conselho Regional de Medicina do Paraná (CRM-PR) deu parecer alertando que a comunidade médica já encarava o uso irrestrito e em grandes quantidades do produto como inseguro e imprevisível, podendo levar a reações crônicas e complicações intratáveis11. Em 2012, a Anvisa, por meio de alerta de segurança, destacou as complicações crônicas possíveis do PMMA, assim como a necessidade de qualificação profissional para sua aplicação12,13.
Em 2013, o CFM emitiu novo parecer reforçando o parecer de 2010 do CRM-PR e reafirmando o uso limitado do PMMA e, quando realizado em grandes quantidades, apresentando resultados imprevisíveis14. Neste parecer, tanto a Sociedade Brasileira de Cirurgia Plástica (SBCP) quanto a Câmara Técnica de Cirurgia Plástica do CFM recomendam que a substância seja utilizada apenas por médicos, em pequenas doses e com restrições.
Em censo de 2016, realizado pela SBCP-SP (regional São Paulo), constatou-se um total de 4432 procedimentos para correção de sequelas de PMMA, o equivalente a 0,7% de do total de procedimentos reparadores daquele ano15. Ainda neste ano, foram realizados mais de 17 mil registros relacionadas a complicações do uso dessa substância em todo o Brasil. Vale destacar também o crescimento de 390% em 2 anos pela procura de procedimentos não cirúrgicos, sendo o preenchimento o principal deles16.
DISCUSSÃO
Frente aos fatos da última década, é incontestável a preocupação com esse tipo de procedimento. Apesar de resultados surpreendentes e imediatos, a popularização sem regulação da aplicação do PMMA para preenchimentos estéticos e o seu uso em grandes volumes com técnicas inadequadas têm evidenciado o PMMA como substância nociva para essa finalidade.
No Brasil, ainda há a falha na regulação e fiscalização pelos órgãos competentes de centros de medicina estética. Aliado a isso, apesar do esforço das entidades médicas, há excesso de propaganda falaciosa, agravado pela crescente exposição das mídias sociais. Isto tudo leva à desinformação da população em geral e à submissão de pacientes a procedimentos sem segurança.
Após episódios marcantes na mídia brasileira nos últimos anos, com casos mutilantes e fatais, as entidades médicas têm se manifestado contra a utilização dessa substância para fins estéticos. Em 2018, tanto a SBCP quando a Sociedade Brasileira de Dermatologia (SBD) emitiriam nota de agravo sobre a utilização do produto e contraindicam o uso do PMMA em grande quantidade, reforçando a imprevisibilidade dos resultados e solicitando a reorientação e restrição do seu uso por parte da Anvisa17.
Na literatura médica, as complicações relacionadas ao PMMA são raras. Variam de 0,01% a 3%2,18. Apesar de baixos, esses dados merecem atenção, pois sabe-se que há falha no registro das complicações, tanto por se tratarem de complicações tardias em sua maior parte quanto pela omissão dos fatos em prontuário médico3. Além disso, não há informação e distinção se as complicações são decorrentes do próprio PMMA ou da falha de técnica para o seu uso. No caso do preenchedor permanente essas complicações merecem atenção especial, pois tornam-se problemas crônicos e de difícil tratamento. Há protocolos, mas não há consenso na padronização do tratamento desse tipo complicação19.
Complicações como necrose são ainda mais raras (0,003%)18. São atribuídas a falha técnica por aplicação com agulhas em planos superficiais e não, necessariamente, ao PMMA. Em 2012, em relato de experiência pessoal em mais de 5000 pacientes, um autor20 revelou taxas de complicações de 0,01% sem nenhuma necrose. Atribui a isso o uso de 3 princípios: aplicação em plano profundo, uso de microcânulas e uso de PMMA puro e certificado.
No caso descrito pode-se afirmar que tanto a qualidade do produto é questionável quanto a técnica utilizada. Neste caso, a combinação de ações não recomendadas levou à complicação e evolução dramática do caso.
Inflamação aguda local nas primeiras horas após a aplicação mostrou-se um sinal de alarme importante que deve ser acompanhado de perto. Em caso de necrose, o desbridamento cirúrgico agressivo aliado a terapia com pressão negativa foram imperativos para melhora inflamatória da paciente e no preparo do leito da ferida21. A cirurgia de desbridamento é um desafio, pois há tecido saudável permeado por tecido necrótico, gerando a falsa impressão de desbridamento satisfatório. A cobertura da ferida após limpeza adequada é desafiadora, entretanto, as sequelas e deformidades causadas dificilmente serão corrigidas plenamente e serão de difícil resolução para o cirurgião plástico.
O uso da tomografia diagnóstica mostrou-se um preditor da extensão da necrose, uma vez que revelou densificação do tecido acometido, mesmo em tecidos ainda clinicamente saudáveis. Esse achado coincidiu com a área desbridada. Não há estudos relacionados a isso na literatura.
CONCLUSÃO
Apesar de índices baixos de complicações na literatura, há um número expressivo, no Brasil, de procedimentos reparadores para correção de complicações do uso do PMMA. A gravidade do caso relatado traz à tona a necessidade de combate a má prática por profissionais não capacitados, assim como um controle mais rigoroso da comercialização do produto pelas entidades reguladoras. O tratamento de complicações é um desafio e pode levar a consequências fatais e a deformidades permanentes.
COLABORAÇÕES
|
KTK |
Análise e/ou interpretação dos dados, aprovação final do manuscrito, coleta de dados, concepção e desenho do estudo, gerenciamento do projeto, investigação, metodologia, realização das operações e/ ou experimentos, redação - preparação do original, redação - revisão e edição. |
|
MM |
Realização das operações e/ou experimentos. |
|
DAM |
Realização das operações e/ou experimentos, redação - revisão e edição, supervisão. |
|
AAMJ |
Supervisão. |
|
RG |
Supervisão, visualização. |
REFERÊNCIAS
1. Carruthers J, Carruthers A, Humphrey S. Introduction to Fillers. Plast Reconstr Surg. 2015;136(5 Suppl):120S-31S.
2. Salles AG, Lotierzo PH, Gemperli R, Besteiro JM, Ishida LC, Gimenez RP, et al. Complications after polymethylmethacrylate injections: report of 32 cases. Plast Reconstr Surg. 2008;121(5):1811-20. PMID: 18454007 DOI: https://doi.org/10.1097/PRS.0b013e31816b1385
3. Rzany B, DeLorenzi C. Understanding, Avoiding, and Managing Severe Filler Complications. Plast Reconstr Surg. 2015;136(5 Suppl):196S-203S.
4. U. S. Food and Drug Administration - FDA. ArteFill® - P020012. Silver Spring: FDA; 2006 [acesso 2018 Set 5]. Disponível em: https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfpma/pma.cfm?id=P020012
5. Brasil. Ministério da Saúde. Agência de Vigilância Sanitária (Anvisa). Anvisa esclarece sobre indicações do PMMA. Brasília: Anvisa; 2018 [acesso 2018 Set 5]. Disponível em: http://portal.anvisa.gov.br/rss/-/asset_publisher/Zk4q6UQCj9Pn/content/anvisa-esclarece-sobre-indicacoes-do-pmma/219201?inheritRedirect=false
6. Brasil. Ministério da Saúde. Secretaria de Atenção à Saúde. Portaria Conjunta SAS SVS Nº 01, de 20 janeiro de 2009. Brasília: Ministério da Saúde; 2009 [acesso 2018 Set 5]. Disponível em: http://portal.anvisa.gov.br/documents/33868/2492231/doc_alerta_954.pdf
7. Jornal da Associação Médica. Especialidade: CFM faz alerta sobre bioplastia [acesso 2018 Set 5] 2006. Disponível em: http://portal.anvisa.gov.br/documents/33868/2492231/doc_alerta_953.pdf
8. Brasil. Ministério da Saúde. Agência de Vigilância Sanitária (Anvisa). Resolução - RE Nº 2.732, de 5 de setembro de 2007. Brasília: Diário Oficial da União; 2007 [acesso 2018 Set 5]. Disponível em: http://portal.anvisa.gov.br/documents/33868/2492231/doc_alerta_955.pdf
9. Vargas AF, Amorim NG, Pitanguy I. Complicações tardias dos preenchimentos permanentes. Rev Bras Cir Plást. 2009;24(1):71-81.
10. de Melo Carpaneda E, Carpaneda CA. Adverse results with PMMA fillers. Aesthetic Plast Surg. 2012;36(4):955-63. DOI: 10.1007/s00266-012-9871-8 DOI: https://doi.org/10.1007/s00266-012-9871-8
11. Conselho Regional de Medicina do Paraná. PARECER Nº 2238/2010 CRM-PR. Processo Consulta Nº 107/2010. Assunto: Procedimento de Bioplastia de Glúteo. EMENTA: Bioplastia - Uso da Substância Polimetilmetacrilato (PMMA) [acesso 2018 Set 5]. Disponível em: https://sistemas.cfm.org.br/normas/visualizar/pareceres/PR/2010/2238
12. Brasil. Ministério da Saúde. Agência de Vigilância Sanitária (Anvisa). Alerta de Segurança para a utilização do Produto POLIMETILMETACRILATO PMMA. Brasília: Anvisa; 2012 [acesso 2018 Set 5]. Disponível em: http://portal.anvisa.gov.br/resultado-de-busca?p_p_id=101&p_p_lifecycle=0&p_p_state=maximized&p_p_mode=view&p_p_col_id=column-1&p_p_col_count=1&_101_struts_action=%2Fasset_publisher%2Fview_content&_101_assetEntryId=2633703&_101_type=content&_101_groupId=33868&_101_urlTitle=2633700&inheritRedirect=true
13. Requena L, Requena C, Christensen L, Zimmermann US, Kutzner H, Cerroni L. Adverse reactions to injectable soft tissue fillers. J Am Acad Dermatol. 2011;64(1):1-34. DOI: https://doi.org/10.1016/j.jaad.2010.02.064
14. Brasil. Conselho Federal de Medicina (CFM). Processo-Consulta CFM Nº 70/12 - Parecer CFM Nº 5/13. Uso indiscriminado do polimetilmetacrilato (PMMA). EMENTA: Recomenda-se que o PMMA, quando utilizado, seja feito por médicos, em pequenas doses, pois o uso em grandes doses pode produzir resultados indesejáveis. Brasília: CFM; 2013 [acesso 2018 Set 5]. Disponível em: http://www.portalmedico.org.br/pareceres/cfm/2013/5_2013.pdf
15. Sociedade Brasileira de Cirurgia Plástica (SBCP). Censo 2016. Situação da Cirurgia Plástica no Brasil. Análise Comparativa das Pesquisa 2014 e 2016. São Paulo: SBCP; 2017 [acesso 2018 Set 5]. Disponível em: http://www2.cirurgiaplastica.org.br/wp-content/uploads/2017/12/CENSO-2017.pdf
16. Aplicação de PMMA resulta em mais de 17 mil complicações em 2016. Plast Pau. 2016;60:24 [acesso 2018 Set 5]. Disponível em: http://sbcp-sp.org.br/downloads/revista-plastica-paulista-2016-ed-60.pdf
17. Conselho Regional de Medicina do Estado de São Paulo (Cremesp), Sociedade Brasileira de Cirurgia Plástica (SBCP), Sociedade Brasileira de Dermatologia (SBD). Nota de Agravo: CREMESP, SBCP e SBD pedem retratação à Anvisa sobre indicações do PMMA. São Paulo: Cremesp, SBCP, SBD [acesso 2018 Set 5]. Disponível em: http://www.sbd.org.br/noticias/nota-de-agravo-cremesp-sbcp-e-sbd-pedem-retratacao-a-anvisa-sobre-indicacoes-do-pmma/
18. Blanco Souza TA, Colomé LM, Bender EA, Lemperle G. Brazilian Consensus Recommendation on the Use of Polymethylmethacrylate Filler in Facial and Corporal Aesthetics. Aesthetic Plast Surg. 2018;42(5):1244-51. DOI: https://doi.org/10.1007/s00266-018-1167-1
19. Cassuto D, Pignatti M, Pacchioni L, Boscaini G, Spaggiari A, De Santis G. Management of Complications Caused by Permanent Fillers in the Face: A Treatment Algorithm. Plast Reconstr Surg. 2016;138(2):215e-27e. PMID: 27465182
20. Nácul AM, Valente DS. Complications after polymethylmethacrylate injections. Plast Reconstr Surg. 2009;124(1):342-3. PMID: 19568132 DOI: https://doi.org/10.1097/PRS.0b013e3181a83ac2
21. Milcheski DA, Ferreira MC, Nakamoto HA, Pereira DD, Batista BN, Tuma P Jr. Subatmospheric pressure therapy in the treatment of traumatic soft tissue injuries. Rev Col Bras Cir. 2013;40(5):392-6. DOI: https://doi.org/10.1590/S0100-69912013000500008
1. Hospital das Clínicas, Faculdade de Medicina,
Universidade de São Paulo, São Paulo, SP, Brasil.
Autor correspondente: Kleber Tetsuo Kurimori Rua Estela, nº 287, Apto 13 - Vila Mariana, São Paulo, SP, Brazil CEP 04011-001 E-mail: kleber.kurimori@gmail.com
Artigo submetido: 18/10/2018.
Artigo aceito: 10/2/2019.
Conflitos de interesse: não há.




 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter