

Original Article - Year 2018 - Volume 33 -
Reconstrução mamária com o retalho miocutâneo do grande dorsal e implantes: avaliação de estratégias adotadas para melhoria dos resultados e avaliação de satisfação pelo Breast-Q
Breast reconstruction with a latissimus dorsi myocutaneous flap and implants: evaluation of strategies adopted to improve the results and evaluation of satisfaction by Breast-Q
RESUMO
Introdução: O trabalho descreve 14 anos em reconstrução mamária com o retalho miocutâneo
do grande dorsal (RGD) e implantes mamários. O objetivo é delinear
experiência com o RGD e implantes mamários, programações das ilhas de pele e
detalhes da dissecção, transposição de retalho e colocação do implante sob
dupla camada muscular, estratégias para minimizar os danos na área doadora,
estratégias de simetrização mamária e reconstrução do complexo
areolopapilar, associado a avaliação do questionário
Breast-Q.
Métodos: Foi realizada revisão de prontuários entre abril de 2003 a junho de 2017.
Resultados: No período 76 pacientes foram reconstruídas com o RGD, com idade média de
50,09 anos, sendo 11 bilaterais, 34 mama direita e 31 mama esquerda. 41
imediatas, 22 tardias e 13 de resgate. A média de satisfação foi 72,36% por
meio do Breast-Q.
Conclusão: Concluímos e comprovamos com o questionário do Breast-Q que
a indicação precisa aliada a técnica de reconstrução proposta com plano
duplo subpeitoral associada a cobertura do RDG, propicia uma loja mais
segura, diminuído o índice de rippling.
Palavras-chave: Neoplasias da mama; Inquéritos e questionários; Retalho miocutâneo; Resultado do tratamento; Implantes de mamas
ABSTRACT
Introduction: The paper describes a 14-year experience with
breast reconstruction using a latissimus dorsi myocutaneous
flap (LDMF) and breast implants. The objective was to
delineate the experience with LDMF and breast implants, skin
island schedules and dissection details, flap transposition and
placement of the implant under a double layer, strategies to
minimize damage in the donor area, and strategies of breast
symmetry and reconstruction of the nipple-areola complex, in
association with evaluation using the Breast-Q questionnaire.
Methods: A review of medical records was performed between
April 2003 and June 2017.
Results: In the period, 76 patients
with a mean age of 50.09 years underwent reconstruction with
a LDMF, which was bilateral in 11, for the right breast in 34, for
the left breast in 31, immediate in 41, late in 22, and for rescue
in 13.
Conclusion: We conclude and verified with the Breast-Q
questionnaire that with a precise indication, the proposed
reconstruction technique with a double subpectoral plane and
coverage with a LDMF is safer with a lower complication rate.
Keywords: Breast neoplasms; Surveys and questionnaires; Myocutaneous flap; Treatment outcome; Breast implants
INTRODUÇÃO
O câncer de mama é o tipo de câncer mais comum entre as mulheres no mundo e no Brasil, depois do câncer de pele não melanoma, respondendo por cerca de 28% dos casos novos a cada ano. O câncer de mama também acomete homens, porém é raro, representando apenas 1% do total de casos da doença. Relativamente raro antes dos 35 anos, acima desta idade sua incidência cresce progressivamente, especialmente após os 50 anos. Estatísticas indicam aumento da sua incidência tanto nos países desenvolvidos quanto nos em desenvolvimento.
Existem vários tipos de câncer de mama, alguns evoluem de forma rápida e até devastadora, outros não. A maioria dos casos tem bom prognóstico. Estimativa de novos casos: 57.960 (2016 - INCA). Número de mortes: 14.388, sendo 181 homens e 14.206 mulheres (2013 - SIM)1. A mastectomia, frequentemente utilizada no tratamento e profilaxia da neoplasia maligna da mama, pode ser um procedimento que salva a vida da mulher com câncer mamário, entretanto, a perda da mama pode causar um trauma psicológico e psicossocial. A reconstrução mamária se torna um passo importante na recuperação pós-mastectomia, podendo ajudar as pacientes a recuperar o senso de feminilidade2. Para tanto, é necessário avaliar o grau de satisfação das paciente que são submetidas à reconstrução.
No âmbito da medicina privada (em que foi desenvolvido o trabalho) houve aumento na detecção mais precoce das doenças neoplásicas das mamas que demandou maior número de profissionais e equipes para ofertar um maior número de reconstruções mamárias. Essa interação e cooperação entre as especialidades médicas (mastologia, cirurgia plástica, oncologia, radioterapia, fisioterapia, etc.) de modo multidisciplinar conseguem amenizar o sofrimento das pacientes com o uso de tratamentos e técnicas mais eficientes.
Dentre as várias técnicas para a reconstrução de mama, que vão desde técnicas com retalhos locais, como o Plug Flap3, e as técnicas de mamoplastia, retalhos de vizinhança, como o retalho toracodorsal4 até as que usam materiais aloplásticos (expansores, próteses) e numerosos retalhos autólogos5, há ainda as técnicas combinadas. Temos como norte que nenhum procedimento é superior a outro em todos os quesitos, no entanto, as pacientes se beneficiam quando há uma escolha criteriosa5, baseada no conhecimento do cirurgião, na vontade da paciente e principalmente nas indicações/contraindicações de cada método.
O retalho do músculo grande dorsal (RGD), descrito por Tansini6 e modificado por Bostwick et al.7, em 1978, apesar de não fornecer um grande volume à neomama quando usado isoladamente, porém quando associado a um implante mamário garante bons resultados. Pela sua versatilidade e segurança, aliado a curta curva de aprendizado, o RGD é muitas vezes uma alternativa de resgate caso haja falha de uma reconstrução inicial5.
Entretanto, em alguns casos a indicação da reconstrução inicial pelo RGD se torna adequada: ausência de área doadora abdominal para uma possível reconstrução com o músculo reto abdominal (TRAM), fatores de risco que contra indiquem outros retalhos, impossibilidade de reconstruções com retalhos locais, falta de tecido para reconstruções com materiais aloplásticos (próteses e expansores) e aceitação por parte das pacientes8.
Com a popularização das reconstruções mamárias e com o melhor conhecimento por parte das pacientes as expectativas mudaram, deixando de serem analisados somente como procedimentos reconstrutores, mas também como procedimentos estéticos, e por mister exigindo resultados mais harmônicos9. Dessa forma, nos casos de reconstrução unilateral ou mesmo bilateral com as mais variadas técnicas, a simetrização se torna um passo fundamental. Apesar de vários trabalhos compararem as diversas técnicas de reconstrução mamária, estudos que avaliam os fatores que influenciam na simetria mamária após reconstrução são escassos10.
OBJETIVO
O objetivo é delinear experiência de 14 anos em reconstrução mamária com o retalho miocutâneo do grande dorsal e implantes mamários, programações das ilhas de pele e detalhes da dissecção, transposição de retalho e colocação do implante sob dupla camada muscular, além de estratégias para minimizar os danos na área doadora. O trabalho também mostrará as estratégias de simetrização mamária e reconstrução do complexo areolopapilar (CAP) associado a avaliação da satisfação das pacientes através do questionário Breast-Q.
MÉTODOS
Todas as 76 pacientes estudadas submetidas à reconstrução mamária com o RGD assinaram o termo de consentimento pré-operatório e foram operadas pelo mesmo cirurgião sênior com a mesma rotina. Para o confecção do trabalho foram revisados os prontuários, fotos de pré e pós- operatório e o questionário do Breast-Q, no período de abril de 2003 a junho de 2017 na Clínica Privada do autor. J.D.L.G.A, em Brasília, DF.
O questionário Breast - Q foi aplicado a todas as pacientes submetidas à reconstrução mamária pós-mastectomia por câncer de mama com o RGD. O Breast-Q foi aplicado a partir do sistema SurveyMonkey, que é o software de questionários e pesquisas online mais popular do mundo. Essa plataforma facilita a criação de enquetes e questionários de pesquisa que ajudam a gerenciar melhor aspectos essenciais do seu negócio, como a satisfação do cliente e o envolvimento dos funcionários.
Foram excluídas as pacientes que sabidamente tinham indicação de radioterapia pós-reconstrução, e, portanto, não foram submetidas à técnica com o RGD, e as pacientes que não desejavam retalhos miocutâneos.
RESULTADOS
No período de abril de 2003 a junho de 2017, as 76 pacientes foram analisadas segundo os dados seguintes:
- Dados epidemiológicos: idade, tipo de câncer e lateralidade. Em 11
pacientes foram feitas reconstruções bilaterais, em 34 da mama direita e
em 31 na mama esquerda. A média de idade no momento da reconstrução foi
de 50,09 anos; destaca-se que havia 23 pacientes com menos de 45 anos de
idade; em 29 pacientes a biópsia mostrou carcinoma ductal invasor, em 5
encontrou-se carcinoma lobular invasivo e em 1 carcinoma papilífero
invasivo e em 41 não encontramos registros no prontuário do
anatomopatológico.
- Se imediata, tardia ou de resgate: 41 reconstruções foram imediatas, 22
tardias e 13 de resgate.
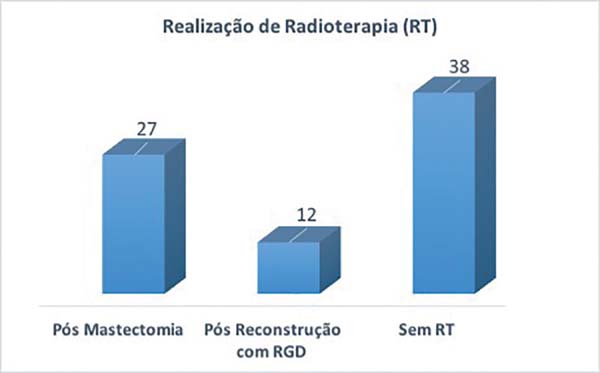
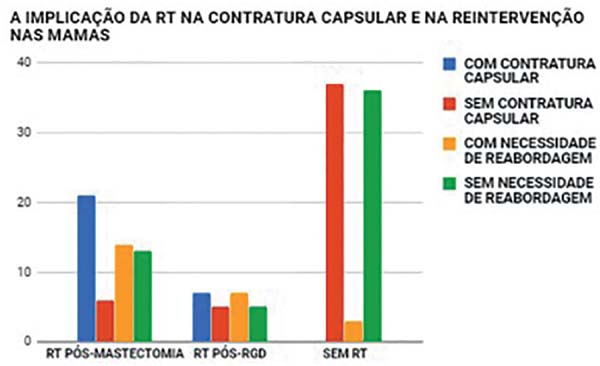
- Realização de quimioterapia e/ou radioterapia: 27 pacientes foram
submetidas à radioterapia pós-mastectomia (são aquelas de reconstrução
tardia e as de resgate), 12 pós-reconstrução com RGD, mesmo que no
pré-operatório não houvesse indicação ou indícios da indicação, e 38 não
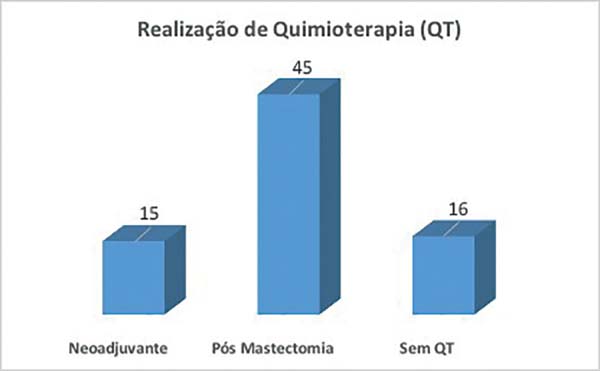
foram submetidas à radioterapia (Figura 1). 15 paciente foram submetidas a quimioterapia
neoadjuvante, 45 pós- mastectomia, e 16 não foram submetidas a
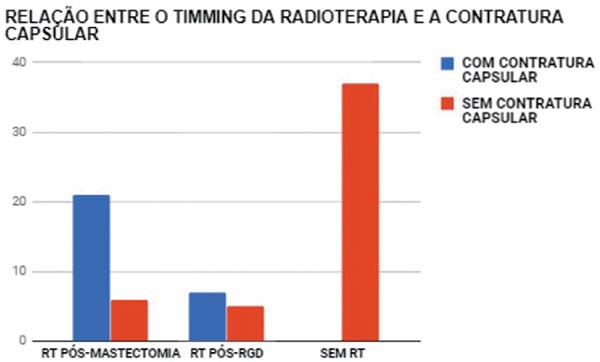
quimioterapia. (Figura 2). Há
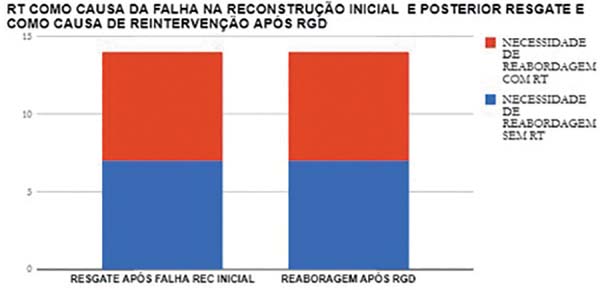
relação direta entre as pacientes que fizeram radioterapia e tiveram que
realizar reconstrução de resgate com RGD ou reabordagem das mamas (Figura 3).
- Intervalos entre o primeiro, segundo e terceiro tempos das
reconstruções: entre a primeira e segunda cirurgia o tempo médio de 8,6
meses e entre o segundo e o terceiro tempo foi de 11 meses; 35 pacientes
finalizaram a reconstrução em duas etapas, 12 em 3 etapas e 28 pacientes
fizeram apenas 1 etapa e não desejaram realizar a segunda/terceira
etapas.
- Tipos dos implantes: em 61 pacientes foram utilizados implantes
texturizados, em 11 pacientes usou-se implantes de poliuretano, em 2
expansor bicompartimental texturizado permanente e 2 não se usou
implantes.
- Plano de inclusão dos implantes: em 70 pacientes com RGD o implante foi
colocado em duplo plano (sob o músculo peitoral maior e o retalho do
músculo grande dorsal) e na simetrização da mama oposta foram 49
retropeitorais; 15 não fizeram a simetrização, 2 foram submetidas à
mastopexia sem prótese, 3 no plano subglandular.
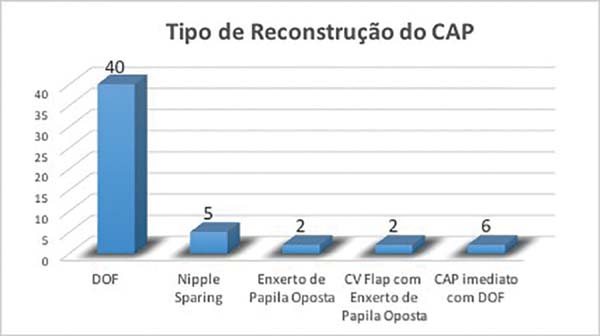
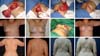
- Tipo de reconstrução do CAP: das 76 pacientes foram realizadas 51
reconstruções de CAP, sendo 40 double opposing flap
(DOF), 5 nipple sparing, 2 enxerto de papila oposta, 2
C-V Flap com enxerto de aréola oposta, 6 CAP
imediato com o DOF (Figura 4).
- Taxas de intercorrências e de complicações: das 12 pacientes que foram
submetidas à radioterapia pós-reconstrução, mesmo que não tenha sido
prevista/programada no pré-operatório, 7 evoluíram com contratura
capsular com necessidade de reabordagem. (Figura 5).
Houve perda do implante por infecção e extrusão em duas pacientes e intercorrências menores em 14 pacientes (seromas, pequenas deiscências, necrose parcial do retalho da mastectomia, ptose precoce do implante e outras menos importantes). Em 24 pacientes houve necessidade de reintervenção, que fora feito em virtude de perda do implante, contratura capsular ou ptose do implante (Figura 6).
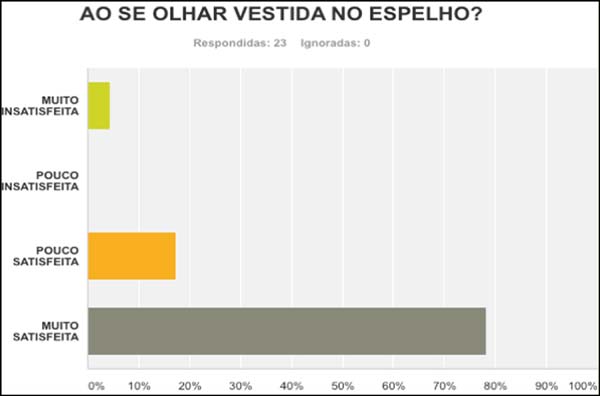
- Com relação à avaliação do grau de satisfação das pacientes após a
reconstrução por meio do Breast-Q modificado para o
português, respondido por 23 pacientes. Destas, 78,26% referiram estar
muito satisfeitas ao se olhar no espelho (Figura 7). Em relação à forma da mama reconstruída, 69,57%
das pacientes referiram estar muito satisfeitas e em relação ao tamanho
da mama esta taxa foi de 81,82%. No que tange à simetrização, a
satisfação ocorreu em 72,73% das pacientes. No quesito aparência da mama
reconstruída em comparação a como elas eram antes de ter feito qualquer
cirurgia na mama, 63,64% das pacientes referiram estar muito satisfeitas
e para 95,65% das pacientes ter feito a reconstrução é muito melhor do
que não ter mama, sendo que este mesmo percentual (95,65%) gostaria de
incentivar outras mulheres a fazerem a cirurgia de reconstrução mamária.
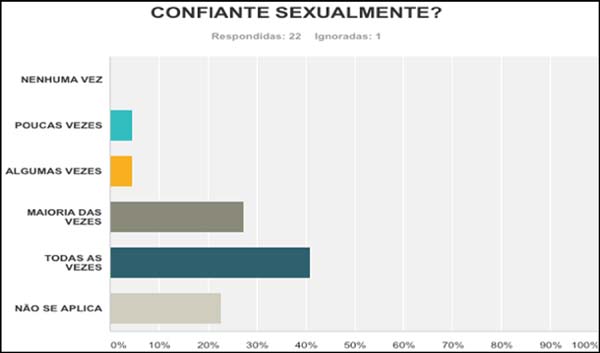
Não houve caso de arrependimento em realizar a reconstrução mamária. Com
relação à confiança, 60,87% referem confiança em ambiente social em
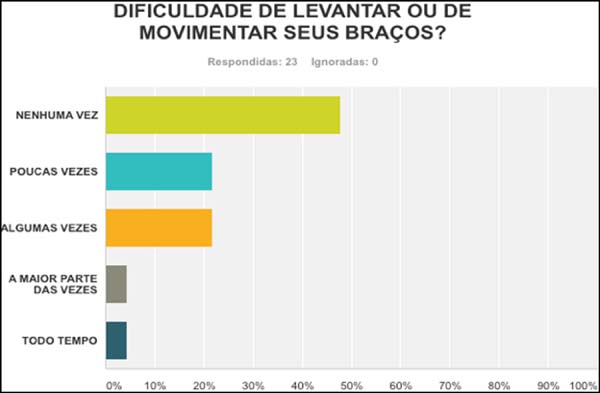
todas as vezes e confiante sexualmente 40,91% em todas as vezes (Figura 8); 47,83% das pacientes
responderam não apresentar dificuldade de levantar ou movimentar seus
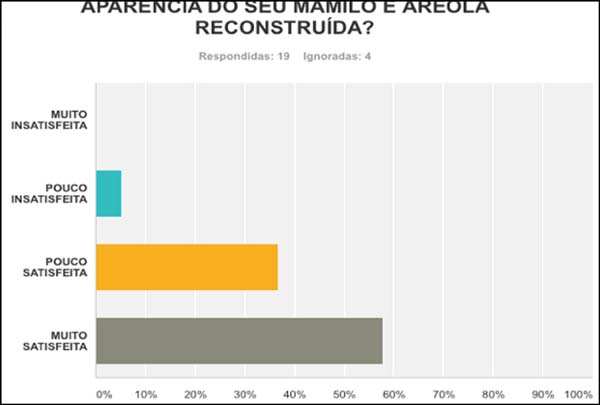
braços (Figura 9). Quanto à
sensibilidade da mama, 50% das pacientes responderam não ter; quanto ao
formato do mamilo, 65% das pacientes estavam muito satisfeitas; e quanto
a aparência do mamilo e aréola reconstruída, 57,89% das pacientes
afirmaram estar muito satisfeitas (Figura 10). A média geral de pacientes muito satisfeitas pela
análise do Breast Q foi de 72,36%.
DISCUSSÃO
A indicação da reconstrução mamária imediata com o grande dorsal foi feita em maioria dos casos (53,94%), enquanto a demanda de pacientes para reconstrução tardia foi de 28,94%. O que norteou a indicação para o RGD foi em primeiro plano a impossibilidade de uso do expansor que é nossa primeira escolha em virtude de ser menos invasiva, a discordância das pacientes em se submeterem à reconstrução com os expansores teciduais, e o fato de serem tumores em estádios 1 ou 2 com baixa probabilidade de radioterapia no pós-reconstrução com o RGD (Figura 11).
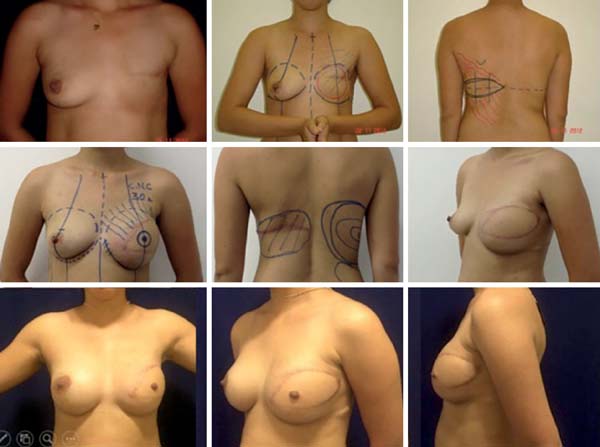
A concepção desses conceitos remonta há mais de 10 anos conforme publicação original de Di Lamartine et al.11 e da observância de outros conceitos igualmente favoráveis ao bom cabo de uma reconstrução mamária, tais como o uso do lipofilling, as táticas de reconstrução do CAP e as estratégias para a simetrização mamária (Figura 12).
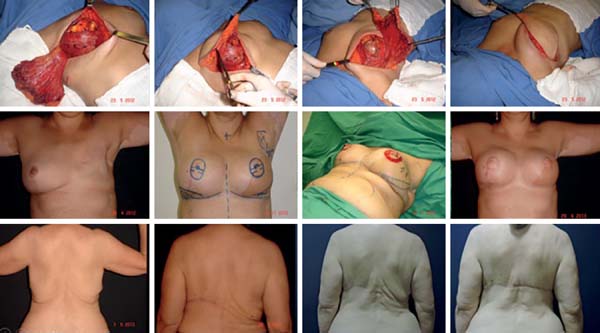
Se houve evolução no diagnóstico precoce e no uso de irradiação com menores danos teciduais, houve também um incremento nas possibilidades de reconstruções menores com os tecidos da própria mama com menores indicações das cirurgias com retalhos à distância. Sem sombra de dúvidas, esse é o melhor horizonte em se tratando de pacientes com diagnóstico precoce ou naqueles casos em que não indicações de adenomastectomia redutora de risco.
O retalho em ilha plug-flap3, com sua excelente versatilidade, proporciona um bom preenchimento dos defeitos gerados pelo tratamento oncológico nas porções superiores internas, superiores externas e centrais. A zona doadora ideal para os retalhos em ilha é definida por duas razões: a primeira é a presença de um grande número de perfurantes que são encontradas do quarto ao sexto espaços intercostais; a segunda é o fechamento da área doadora nesta área permite modelar a mama como se fosse uma mastoplastia convencional3.
Classicamente, os retalhos à distância de relevância são: o retalho miocutâneo do reto abdominal (TRAM), descrito por Drever12, em 1977, e modificado por Hartrampf et al.13 e Gandolfo14, em 1982, e o retalho do músculo grande dorsal (RGD), descrito por Tansini15 e modificado por Bostwick et al.16 , em 1978. O RGD frequentemente é associado a próteses ou expansores de silicone, com o objetivo de aumentar o volume e dar forma ao cone mamário. O emprego de expansores permanentes bicompartimentais é mais recente e teve seu uso metodizado e difundido por Becker17.
Seguindo os critérios adotados pela literatura mundial, contraindicar a reconstrução imediata é hoje cientificamente intolerável e contraria o conceito já preconcebido das pacientes de que sempre é possível reconstruir de imediato. Logo, o cirurgião assume os altos índices de contratura capsular quando indica a reconstrução imediata, que podem chegar a 68% segundo dados de McCarthy et al.17. Um alento ao cirurgião é que esse mesmo estudo demonstra que o índice de contratura capsular em reconstruções mamárias com aloplásticos, mesmo sem radioterapia pós-operatória, pode chegar a 40%. Os índices de sucesso final das reconstruções foram de 90% com radioterapia e de 99% sem radioterapia.
A utilização da radiação sobre o retalho miocutâneo também se encontra relacionada à contratura capsular, queimadura e radiodermite, sendo o tratamento cirúrgico mais complexo e a possibilidade de resultados insatisfatórios elevada. Além dessas complicações, a hipoestesia, dor e linfedema são descritas na literatura18. Esse pensamento norteou sempre nossas indicações na escolha das técnicas em reconstruções mamárias, de forma que ao menor indício de radioterapia a reconstrução era tentada apenas com expansores quando possível, deixando o RGD intacto e disponível para uma possível falha da reconstrução imediata em virtude dos danos potenciais da RT sobre as reconstruções (Figura 13).
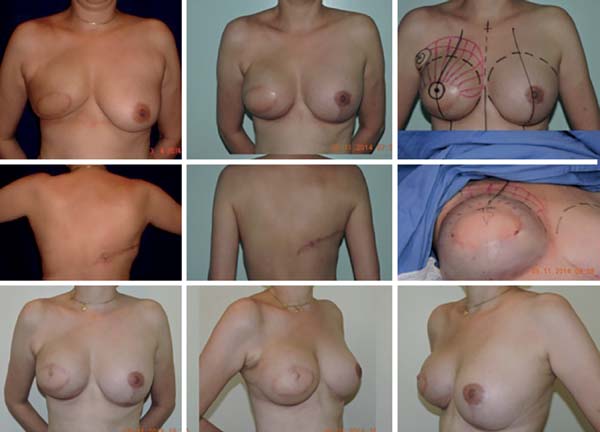
A pesquisa por linfonodos sentinela tem um papel chave quando nos atemos ao tratamento cirúrgico conservador na neoplasia de mama. Sabe-se que em torno de 25% das pacientes submetidas ao mapeamento linfático vão apresentar algum acometimento linfonodal, o que pode implicar em complementação do tratamento com radiação. Segundo a American Society of Clinical Oncologists Guidelines, todos os casos com 4 ou mais linfonodos positivos, tumores maiores que 5cm com qualquer linfonodo positivo (T3) e todos tumores operáveis no estágio 3, tem indicação de RT pós mastectomia. Fato que definitivamente irá traçar a estratégia de reconstrução, podendo- se até postergar a reconstrução em casos específicos em virtude de fatores próprios do tumor ou das pacientes, somados ao ato incontestavelmente deletério da radioterapia para os implantes/reconstruções19.
A mastectomia skin sparing ou niple sparing tornou-se mais usada à medida que se diagnostica a doença em fases mais precoces. Sabe-se que por mais efetiva que seja a mastectomia com preservação de pele, sobrará cerca de 9,5%20 de tecido mamário, por isso, é de grande valor que se tenha um planejamento pré-operatório adequado, com mastologistas e cirurgiões plásticos sempre que possível para manter o mínimo de tecido que possa manter a viabilidade dos retalhos necessários para as reconstruções e as incisões dentro de um “T imaginário” como descrito por Pitanguy21. (Figura 14).
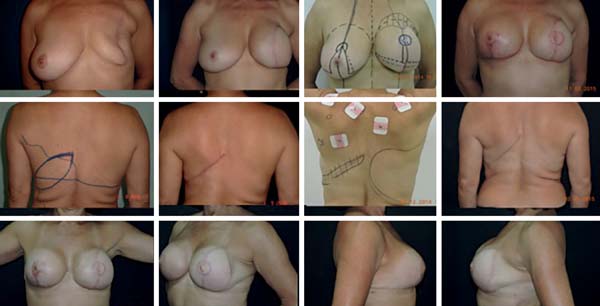
Em um estudo prospectivo, Sbitany et al.22 comparam a reconstrução imediata com expansores/implantes em pacientes submetidas à RT (pré ou pós-mastectomia) e não submetidas. Foi notada maior taxa de complicações no grupo de pacientes irradiadas - como infecções, deiscência de ferida, necrose de pele, exposição e perda do implante. Uma taxa de 19,2% maior em comparação com o outro grupo. Outros estudos mostraram que as complicações após RT podem chegar a 40%. Isso ocorre pela falta de complacência do tecido irradiado além do dano na vascularização, da maior tendência a fazer contratura capsular (presente em até 60% dos casos), maiores taxas de liponecroses, lipoatrofias e radiodermite.
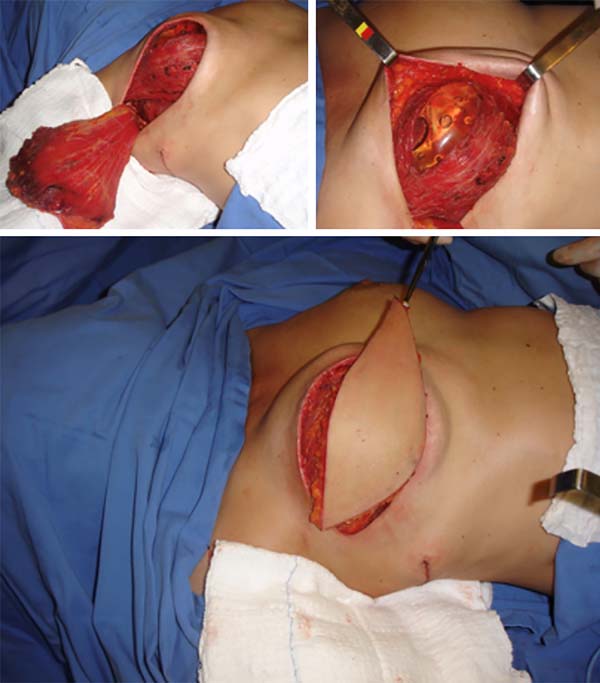
Nos casos em que há contraindicação do TRAM ou por motivos de escolha da paciente, o retalho miocutâneo do latissimus dorsi (grande dorsal) pode ser uma saída. Apesar de confiável e versátil, sua projeção geralmente é inadequada necessitando ser associado à um implante ou expansor (na maioria dos casos). Trata-se de uma retalho seguro, com pedículo vascular robusto. Por esse motivo, pode ser indicado em pacientes que apresentam fatores de risco maiores, que contraindicariam outros tipos de retalhos autólogos e é muitas vezes utilizado na reconstrução de resgate.
Nos casos em que existe história de radioterapia ou esvaziamento axilar, deve-se prosseguir investigação com exames de imagem (Doppler) para verificar a patência do pedículo toracodorsal. O ideal é que seja planejado um fuso de pele horizontal, onde a cicatriz resultante ficará na linha do sutiã, todavia, em pacientes idosos e naqueles em se necessita de grandes ilhas de pele o desenho oblíquo é preferível.
Simetrização, reconstrução do CAP, refinamentos e complicações
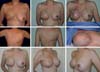
Sob nossa concepção a simetrização mamária é etapa de fundamental importância para o bom cabo de uma reconstrução mamária. Perante as mais diversas formas e volumes das mamas a serem tratadas, o raciocínio do cirurgião reconstrutor deve ser aguçado ao ponto de na avaliação inicial já prospectar o tamanho, forma e volume das mamas que se pode alcançar. Da mesma forma, há que se pensar que a neomama terá um envelope cutâneo e uma textura determinada pelo tipo de reconstrução adotada.
Na maioria das vezes, com exceção feita às reconstruções com o TRAM, a cobertura que se consegue para o implante nos casos de reconstrução com implantes, mesmo quando se usa o RGD, é delgada com possibilidades até de ter rippling no pós-operatório tardio. Na estratégia que adotamos colocando o implante sob dupla camada muscular (Figura 15), além de definirmos uma loja mais justa para a colocação do implante (texturizado na maioria das vezes) com menores possibilidades de distopias do mesmo, conseguimos um trunfo a mais na prevenção do rippling - no segundo e terceiro tempos ainda se usa o lipoenxerto com a mesma finalidade se for necessário.
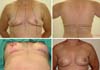
A simetrização obrigatoriamente passa por fazer uma redução tecidual visando, em primeiro plano, semelhança de cobertura dos implantes entre as mamas, e em segundo plano reduzir o volume glandular na mama oposta com benefícios na prevenção contra o câncer na mama oposta. Essa estratégia de retirar 60-70% do volume da mama oposta, associado à inclusão do implante em plano retropeitoral se mostrou bastante efetiva em estudo prévio feito por nós (Figura 16).
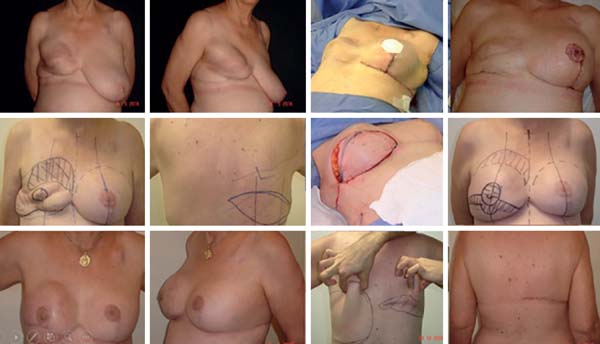
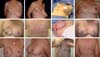
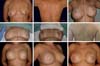
Findadas a reconstrução e a simetrização, o novo CAP se torna o toque final de todo um trabalho. Em meio a várias técnicas/táticas de reconstrução do CAP a escolha de algumas, que se possa dominar e usar com todo conhecimento, é muito importante. Em nossa casuística usamos em maioria dos casos o DOF por ter encontrado nessa técnica a que melhor mimetiza o CAP oposto, pois além de possibilitar uma papila com forma e projeção que se mantêm a longo prazo, criam uma aréola com relevo em relação aos tecidos vizinhos, semelhante à anatomia de uma CAP natural. Uma estratégia que adotamos foi desenhar o retalho na forma oval/elíptica, pois ao final conseguimos um CAP de fato redondo - o que não acontecia com o desenho do trabalho original, pois o CAP não ficava de fato circular e o mamilo não ficava exatamente no centro da aréola23 (Figura 17).
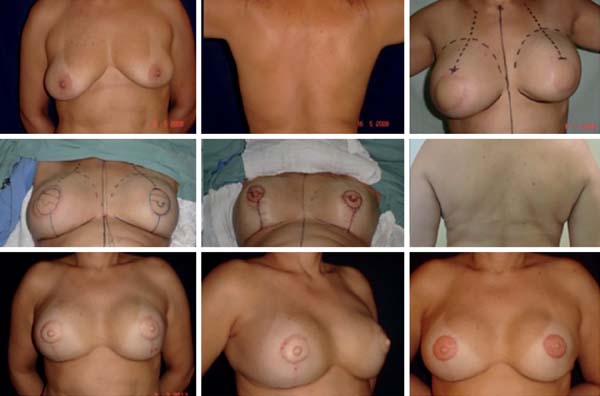
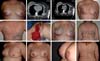
Houve casos em que fizemos reconstrução unilateral, ou bilateral, e já reconstruímos o CAP no primeiro tempo, pois a situação era favorável a isso (Figura 18). A presença de cicatrizes e a radioterapia não são impeditivos à utilização do DOF, pois trata-se de um retalho bastante seguro e previsível em virtude de sua base séssil23.
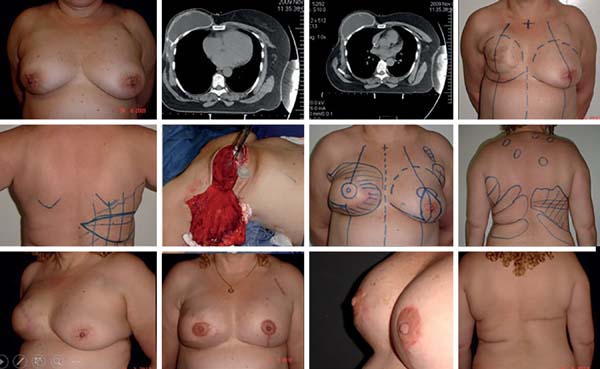
O momento da simetrização, e depois no tempo de reconstrução do CAP, é oportuno também para os refinamentos necessários em casos em que houve assimetria do posicionamento e volume dos implantes; contraturas capsulares; excessos tegumentares inadequados; cicatrizes inadequadas; retalhos e cobertura finos em que o lipoffiling propicia a solução adequada (Figura 18).
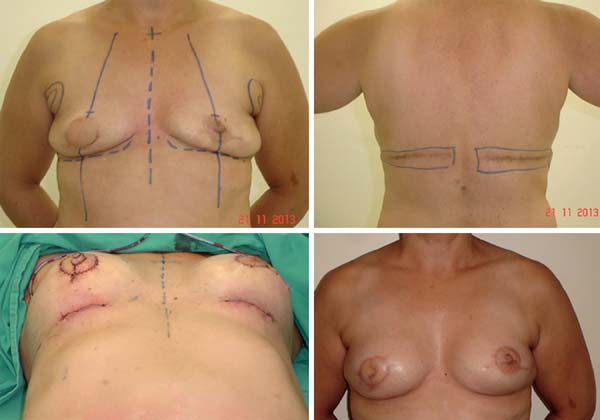
As complicações observadas que exigiram a remoção do implante ou a reabordagem estavam relacionadas a infecção e exposição do implante, necrose da pele residual da mastectomia e distopias dos implantes. Nos casos de perda dos implantes programou-se sua recolocação após tempo adequado, não menos que seis meses; nos casos de distopias dos implantes ou necessidades de ajustes de pele procedeu-se o reparo nos tempos subsequentes da reconstrução (Figura 19).
CONCLUSÃO
Concluímos e comprovamos com o questionário do Breast-Q que a indicação precisa, aliada à técnica de reconstrução com os implantes colocados sob dupla camada muscular (peitoral maior e RGD), propicia uma loja mais segura e estável e diminui o índice de rippling. A simetrização com adenomastectomia subtotal nas pacientes com câncer de mama apresenta resultados muito satisfatórios, uma vez que faz uma citorredução da mama oposta e propicia mamas com melhor simetria em termos de volume, textura, projeção e resultado a longo prazo. O DOF se configura como uma técnica excelente que reconstrói CAPs com resultados favoráveis e que se mantém ao longo dos anos.
COLABORAÇÕES
|
LDPB |
Análise e/ou interpretação dos dados; análise estatística; aprovação final do manuscrito; coleta de dados; conceitualização; concepção e desenho do estudo; gerenciamento de recursos; gerenciamento do projeto; investigação; metodologia; realização das operações e/ou experimentos; redação - preparação do original; redação - revisão e edição; visualização. |
|
JDLGA |
Análise e/ou interpretação dos dados; análise estatística; aprovação final do manuscrito; aquisição de financiamento; coleta de dados; conceitualização; concepção e desenho do estudo; gerenciamento de recursos; gerenciamento do projeto; investigação; metodologia; redação - revisão e edição; supervisão; visualização. |
|
JCD |
Gerenciamento de recursos; gerenciamento do projeto; metodologia; redação - revisão e edição; supervisão. |
|
LMCD |
Coleta de dados; conceitualização; investigação; redação - preparação do original; redação - revisão e edição. |
|
JGOJ |
Análise e/ou interpretação dos dados; análise estatística; coleta de dados; investigação; metodologia; realização das operações e/ ou experimentos; redação - preparação do original; redação - revisão e edição. |
|
GCS |
Análise e/ou interpretação dos dados; análise estatística; aprovação final do manuscrito; coleta de dados; investigação; realização das operações e/ou experimentos; redação - preparação do original; redação - revisão e edição. |
|
ACC |
Análise e/ou interpretação dos dados; coleta de dados; realização das operações e/ou experimentos; redação - preparação do original; redação - revisão e edição |
|
RCSD |
Análise e/ou interpretação dos dados; análise estatística; coleta de dados; redação - preparação do original; redação - revisão e edição; visualização. |
REFERÊNCIAS
1. Brasil. Instituto Nacional de Câncer José Alencar Gomes da Silva (INCA). Estimativa 2016: Incidência de Câncer no Brasil. Rio de Janeiro: INCA; 2015.
2. Colakoglu S, Khansa I, Curtis MS, Yueh JH, Ogunleye A, Haewyon C, et al. Impact of complications on patient satisfaction in breast reconstruction. Plast Reconstr Surg. 2011 Apr;127(4):1428-36.
3. Daher JC. Breast island flaps. Ann Plast Surg. 1993;30(3):217-23.
4. Holmström H, Lossing C. The lateral thoracodorsal flap in breast reconstruction. Plast Reconstr Surg. 1986;77(6):933-43.
5. Serletti JM, Fosnot J, Nelson JA, Disa JJ, Bucky LP. Breast reconstruction after breast cancer. Plast Reconstr Surg. 2011;127(6):124e-35e.
6. Tansini I. Sopra il mio nuovo processor di amputazione della mammella. (coverage of the anterior chest wall following mastectomy). Guz Mal Ital. 1906;57:141.
7. Bostwick J 3rd, Vasconez LO, Jurkiewicz MJ. Breast reconstruction after a radical mastectomy. Plast Reconstr Surg. 1978;61(5):682-93.
8. Di Lamartine J, Galdino Júnior J, Daher JC, Guimarães GS, Camara Filho JPP, Borgatto MS, et al. Reconstrução mamária com retalho do músculo grande dorsal e materiais aloplásticos: análise de resultados e proposta de nova tática para cobertura do implante. Rev Bras Cir Plást. 2012;27(1):58-66.
9. Hamdi M, Casaer B, Andrades P, Thiessen F, Dancey A, D'Arpa S, et al. Salvage (tertiary) breast reconstruction after implant failure. J Plast Reconstr Aesthet Surg. 2011;64(3):353-9.
10. Leone MS, Priano V, Franchelli S, Puggioni V, Merlo DF, Mannucci M, et al. Factors affecting symmetrization of the contralateral breast: a 7-year unilateral postmastectomy breast reconstruction experience. Aesthetic Plast Surg. 2011;35(4):446-51.
11. Di Lamartine J, Galdino Júnior J, Daher JC, Guimarães GS, Camara Filho JPP, Borgatto MS, et al. Reconstrução mamária com retalho do músculo grande dorsal e materiais aloplásticos: análise de resultados e proposta de nova tática para cobertura do implante. Rev Bras Cir Plást. 2012;27(1):58-66.
12. Drever JM. Total breast reconstruction with either of two abdominal flaps. Plast Reconstr Surg. 1977;59(2):185-90.
13. Hartrampf CR, Scheflan M, Black PW. Breast reconstruction with a transverse abdominal island flap. Plast Reconstr Surg. 1982;69(2):216-25.
14. Gandolfo EA. Breast reconstruction with a lower abdominal myocutaneous flap. Br J Plast Surg. 1982;35(4):452-7.
15. Tansini I. Sopra il mio nuovo processor di amputazione della mammella. (coverage of the anterior chest wall following mastectomy). Guz Mal Ital. 1906;57:141.
16. Bostwick J 3rd, Vasconez LO, Jurkiewicz MJ. Breast reconstruction after a radical mastectomy. Plast Reconstr Surg. 1978;61(5):682-93.
17. Becker H. One stage immediate breast reconstruction with adjustable implants. In: Spear SL, ed. Surgery of the breast: principles and art. 2nd ed. Philadelphia: Lippincott Williams & Wilkins; 2006. p.438-50.
18. Cordeiro PG, Pusic AL, Disa JJ, McCormick B, VanZee K. Irradiation after immediate tissue expander/implant breast reconstruction: outcomes, complications, aesthetic results, and satisfaction among 156 patients. Plast Reconstr Surg. 2004;113(3):877-81.
19. Pedron M, Alves MR, Menk C. Sistematização em mamoplastia oncológica. Rev Soc Bras Cir Plást. 2001;16(3):54-60. Bostwick J 3rd, Paletta C, Hartrampf CR. Conservative treatment for breast cancer. Complications requiring reconstructive surgery. Ann Surg. 1986;203(5):481-90.
20. Torresan RZ, Cabello dos Santos C, Brenelli H, Okamura H, Alvarenga M. Residual glandular tissue after skin-sparing mastectomies. Breast J. 2005;11(5):374-5.
21. Pitanguy I. Surgical treatment of breast hypertrophy. Br J Plast Surg. 1967;20(1):78-85.
22. Sbitany H, Mirzabeigi MN, Kovach SJ, Wu LC, Serletti JM. Strategies for recognizing and managing intraoperative venous congestion in abdominally based autologous breast reconstruction. Plast Reconstr Surg. 2012;129(4):809-15.
23. Di Lamartine J, Cintra Junior R, Daher JC, Cammarota MC, Galdino J, Pedroso DB. Reconstrução do complexo areolopapilar com double opposing flap. Rev Bras Cir Plást. 2013;28(2):233-40.
1. Hospital Daher Lago Sul, Serviço de Cirurgia
Plástica, Brasília, DF, Brasil.
2. Clínica Di Lamartine, Cirurgia Plástica,
Brasília, DF, Brasil.
Autor correspondente: Jefferson Di Lamartine Galdino Amaral, SCN QD.02, Torre A, Salas 1121 e 1123 - 11º Andar - “Shopping Liberty Mall” - Brasília, DF, Brasil, CEP 70712-903. E-mail: jefferson@dilamartine.com.br
Artigo submetido: 12/4/2018.
Artigo aceito: 1/10/2018.
Conflitos de interesse: não há.












 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter