

Original Article - Year 2013 - Volume 28 -
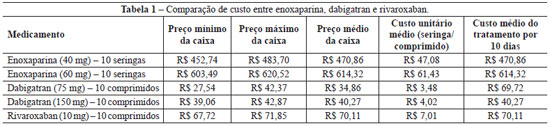
Comparação de custo da enoxaparina e dos novos anticoagulantes orais dabigatran e rivaroxaban na profilaxia do tromboembolismo venoso
Cost comparison between enoxaparin and new oral anticoagulants dabigatran and rivaroxaban in venous thromboembolism prophylaxis
RESUMO
INTRODUÇÃO: O tromboembolismo venoso é uma complicação importante altamente evitável em cirurgia, sendo uma das poucas entidades clínicas em medicina passíveis de profilaxia comprovadamente eficiente, assim como ocorre na profilaxia antibiótica das infecções cirúrgicas. A profilaxia tem por objetivo diminuir a incidência de trombose venosa profunda, minimizar os riscos das complicações a longo prazo da insuficiência venosa crônica e hipertensão pulmonar, bem como prevenir a morte consequente de embolia pulmonar. Este estudo tem por objetivo atualizar os cirurgiões plásticos quanto às medicações que podem ser adotadas na profilaxia do tromboembolismo venoso, bem como comparar o custo dessas medicações (enoxaparina, dabigatran e rivaroxaban).
MÉTODO: Para efeito de comparação foi adotado um esquema de profilaxia iniciado 6 horas após o fim da cirurgia e mantido por 10 dias. A pesquisa foi realizada na internet entre as principais redes farmacêuticas, levando em conta o custo para o consumidor.
RESULTADOS: Os novos anticoagulantes orais dabigatran e rivaroxaban apresentaram custo menor para o paciente.
CONCLUSÕES: Os novos anticoagulantes orais dabigatran e rivaroxaban possuem custo menor na profilaxia do tromboembolismo venoso em comparação à heparina de baixo peso molecular.
Palavras-chave: Tromboembolia. Tromboembolia venosa/prevenção & controle. Anticoagulantes.
ABSTRACT
BACKGROUND: Venous thromboembolism, an important complication that is easily prevented during surgery, is among the few clinical entities wherein the use of prophylaxis has been found to be effective, such as in the case of antibiotic prophylaxis for the prevention of surgical site infections. The objectives of prophylaxis are to reduce the incidence of deep vein thrombosis, minimize the risk of long-term complications such as chronic venous insufficiency and pulmonary hypertension, and prevent death caused by pulmonary embolism. In this study, we aimed to provide current information to plastic surgeons on the therapeutic options for prophylaxis of venous thromboembolism as well as to compare treatment costs of the drugs enoxaparin, dabigatran, and rivaroxaban.
METHOD: For comparison, the prophylaxis regimen was started 6 hours after the surgery and continued for 10 days. The end user price was obtained from an internet search that included leading pharmacy chains.
RESULTS: The patient costs of the new oral anticoagulants dabigatran and rivaroxaban were lower than that of enoxaparin.
CONCLUSIONS:The cost of venous thromboembolism prophylaxis consisting of the new oral anticoagulants dabigatran and rivaroxaban is lower than that of low molecular weight heparin.
Keywords: Thromboembolism. Venous thromboembolism/prevention & control. Anticoagulants.
O tromboembolismo venoso (TEV), espectro de doenças que inclui a trombose venosa profunda (TVP) e a embolia pulmonar (EP), é uma complicação cirúrgica grave, relevante a todos os cirurgiões plásticos1-13. Nos últimos 25 anos, diversos estudos têm repetidamente comprovado a eficácia da profilaxia antitrombótica14,15.
A profilaxia tem por objetivos diminuir a incidência de TVP, minimizar os riscos das complicações a longo prazo da insuficiência venosa crônica e hipertensão pulmonar, bem como prevenir a morte consequente de EP2.
Sem profilaxia, um em cada quatro pacientes com mais de 40 anos de idade submetidos a cirurgia geral de grande porte, com mais de uma hora de duração, desenvolverá TVP2.
Nos Estados Unidos, os casos de TVP correspondem a 250 mil por ano16. A EP é responsável por 150 mil mortes por ano e por 5% de todos os óbitos perioperatórios16.
Em cirurgia plástica, a abdominoplastia tem as maiores taxas de TVP (1,2%) e EP (0,8%); e quando combinada a procedimentos intra-abdominais, como histerectomia, a incidência de EP aumenta para 6,6%16. A lipoaspiração representa 0,6% de TVP e 1,1% de EP5,16, e a ritidoplastia, 0,35% de TVP e 0,14% de EP4,5,16.
A profilaxia antitrombótica pode ser feita com métodos físicos e medicamentosos2. Os métodos mecânicos compreendem a meia elástica e a compressão pneumática intermitente, e são reservados para pacientes de baixo risco trombótico ou com alto risco hemorrágico17. Os métodos farmacológicos são geralmente preferidos para pacientes com risco trombótico moderado a alto ou em procedimentos cirúrgicos que estejam mais relacionados ao TEV17. Podem ser utilizadas a heparina não-fracionada, a heparina de baixo peso molecular, o fondaparinux e os novos anticoagulantes orais17.
O dabigatran foi descoberto a partir de um painel de produtos químicos com estrutura semelhante à do inibidor de trombina baseada na benzamidina α-NAPAP (N-alfa-(2-naphthylsulfonylglycyl)-4-amidinofenilalanina piperidida), conhecida desde a década de 1980 como um potente inibidor de várias serinas proteases, especificamente da trombina, mas também da tripsina18. A adição de um éster de etil e hexiloxicarbonil carbamimida hidrofóbica de cadeias laterais levou à prodroga absorvida por via oral, BIBR 1048 (etexilato de dabigatran)18. O dabigatran é um anticoagulante oral da classe dos inibidores diretos da trombina, fabricado pela Boehringer Ingelheim, sendo aprovado em 2008 pela agência de medicamentos europeia, em 2010 pelo FDA e em 2011, pela ANVISA18.
O rivaroxaban (BAY 59-7939), anticoagulante oral desenvolvido pela Bayer Schering Pharma, é uma oxazolidinona otimizada para inibir o fator Xa livre e o fator Xa ligado ao complexo protrombinase18. Por ser um inibidor seletivo direto do fator Xa, sua ação interrompe as vias intrínseca e extrínseca da cascata de coagulação do sangue, inibindo a formação de trombina e o desenvolvimento de trombos18. O rivaroxaban é o primeiro inibidor direto do fator Xa disponível no mercado18. Ambos os medicamentos permanecem em fase IV (controle pós-marketing), período em que se espera que os efeitos adversos e a toxicidade sejam detectados e reportados às autoridades18.
Com o desenvolvimento de novos anticoagulantes orais que demonstraram mais eficácia e a mesma segurança quando comparados à dose recomendada de enoxaparina na profilaxia do TEV19, tanto a profilaxia como o tratamento dos casos de TEV foram revolucionados.
O dabigatran é administrado via oral 150 mg/dia em dose profilática, e está sendo disponível no mercado sob o nome comercial Pradaxa, em caixas com 10 e 30 comprimidos de 75 mg, caixas de 10 e 60 comprimidos de 110 mg, e caixas de 10, 30 e 60 comprimidos de 150 mg.
O rivaroxaban é administrado via oral 10 mg/dia em dose profilática, e está disponível no mercado sob o nome comercial Xarelto, em caixas de 10 e 30 comprimidos de 10 mg, e caixas de 14 e 28 comprimidos de 15 e 20 mg.
A enoxaparina é administrada por via subcutânea na dose de 40 mg/dia, devendo-se ajustar a dose em pacientes obesos (1 mg/kg/dia), e está disponível no mercado sob os nomes Clexane, Cutenox, Enoxalow, Enoxil, Heptron e Versa, em caixas com 2 e 10 seringas de 40, 60, 80 e 100 mg.
Este trabalho tem por objetivo atualizar os cirurgiões plásticos quanto às medicações que podem ser adotadas na profilaxia do TEV, bem como comparar o custo dessas medicações (enoxaparina, dabigatran e rivaroxaban).
MÉTODO
Para efeito de comparação de custo foi adotado um esquema de profilaxia iniciado 6 horas após o fim da cirurgia e mantido por 10 dias. A pesquisa foi realizada na internet entre as principais redes farmacêuticas nacionais, totalizando 12 empresas. As 2 empresas líderes possuíam drogarias em 9 e 8 estados; as demais redes possuíam um sistema de entrega a domicílio, sendo considerado o preço final para o consumidor nos seguintes estados: Bahia, Distrito Federal, Espírito Santo, Goiás, Mato Grosso, Mato Grosso do Sul, Minas Gerais, Paraná, Rio de Janeiro, Rio Grande do Sul, Santa Catarina e São Paulo.
Foi calculada a média de preço pela soma de todos os valores obtidos na pesquisa, dividida pelo número de resultados encontrados (dabigatran: 12 resultados, rivaroxaban: 8 resultados e enoxaparina: 12 resultados). O custo unitário médio foi estabelecido pela média de preço dividida pelo número de seringas ou comprimidos utilizados nos 10 dias de tratamento.
RESULTADOS
O tratamento com dabigatran 75 mg representa uma economia de 88,65% em relação ao custo da enoxaparina 60 mg e de 85,19% em comparação à enoxaparina 40 mg. O tratamento com dabigatran 150 mg representa uma economia de 93,44% em relação ao custo do tratamento com a enoxaparina 60 mg e de 91,44% quando comparado à enoxaparina 40 mg.
O tratamento com rivaroxaban 10 mg representa uma economia de 88,58% em relação ao custo do tratamento com a enoxaparina 60 mg e de 85,11% quando comparado à enoxaparina 40 mg.
Os novos anticoagulantes orais (dabigatran e rivaroxaban) têm custo menor que a enoxaparina (Tabela 1).
DISCUSSÃO
Se por um lado é consenso entre os cirurgiões plásticos o uso de métodos mecânicos (deambulação precoce, meia elástica e compressão pneumática intermitente) na profilaxia antitrombótica, a profilaxia medicamentosa chega a ser quase que um tabu.
Parte dos cirurgiões plásticos questiona a metodologia, o conflito de interesse de autores que publicam sobre o tema e a chance aumentada de hematoma. Porém, diante da enorme quantidade de estudos randomizados e duplo-cegos realizados nos últimos 25 anos nas mais diversas especialidades cirúrgicas, todos confirmando o benefício da quimioprofilaxia na prevenção do TEV, não deve haver dúvidas quanto a sua utilização.
Apesar de diversos protocolos sugerirem a profilaxia medicamentosa, não há consenso quanto a um protocolo único. Observa-se, porém, que todos os protocolos levam em conta o estresse cirúrgico a que o paciente será submetido (risco baixo, moderado e alto) e a estratificação de risco do próprio paciente (baixo, moderado e alto).
A grande falha dos protocolos, segundo os principais estudiosos de profilaxia antitrombótica, é que não se pode somar as incidências, como acontece no sistema de pontos sugerido pela maioria dos protocolos. Devem-se calcular as incidências separadamente para cada tipo de procedimento e depois adotar um esquema de profilaxia conforme indicado. A artroplastia total de quadril, indicação clássica de profilaxia medicamentosa, tem chance de EP em torno de 6%20,21. Em cirurgia plástica, essa incidência é alcançada quando se realiza dermolipectomia combinada a histerectomia. Esse seria um exemplo de indicação de profilaxia medicamentosa em nossa especialidade, quando a chance de EP é de 6,6%16.
Alguns protocolos chegam a indicar o início da profilaxia 6 horas antes do procedimento cirúrgico. Entretanto, há contraindicações de seu emprego em pacientes submetidos a anestesia peridural. Assim, neste estudo foi sugerido um protocolo de profilaxia, para efeito de comparação de custo, iniciado 6 horas após o fim da cirurgia, pois foi comprovado que não há maior sangramento pós-operatório quando se inicia enoxaparina nesse período22, bem como não haveria problemas relacionados ao tipo de anestesia instituído.
O grande receio do cirurgião plástico na utilização da profilaxia química em ritidoplastias é o hematoma, pois um sangramento pode ser catastrófico, alterando profundamente o resultado estético. Os estudos demonstram que a chance de TVP e EP são de 0,35% e 0,14%, respectivamente4,5,16, apesar de o tempo cirúrgico ser em média de 6 horas. Esse procedimento deve ser classificado como de baixo risco para TVP e EP, sendo exceção o uso de profilaxia medicamentosa (métodos mecânicos sempre), a não ser que o paciente tenha estratificação de risco alta para TEV.
Como os novos anticoagulantes orais não têm método de reversão comprovadamente eficaz, nossa sugestão de protocolo se inicia após 6 horas porque nesse período não se observou maior necessidade de reintervenção cirúrgica. Em caso de sangramento leve, medidas locais associadas à simples suspensão do anticoagulante são a melhor alternativa, em decorrência da meia-vida geralmente de curta duração dessas medicações (7 horas a 14 horas). Em situações dramáticas, com sangramento grave, não há medida eficaz, e as opções existentes são o fator VII ativado recombinante e o concentrado de complexo protrombínico ativado.
O esquema de profilaxia sugerido para efeito de comparação de custo se estende apenas por 10 dias, pois, apesar de existirem relatos de casos que ultrapassam esse período na literatura, não há consenso quanto ao período que se deve fazer a profilaxia pós-operatória. Contudo, sabe-se que o período de maior fatalidade com EP ocorre entre 3 dias e 7 dias após a cirurgia e que 10% das EPs sintomáticas são fatais após 1 hora do início dos sintomas23. Além disso, as medicações são encontradas em caixas de 10 unidades.
Outro aspecto importante que deve ser lembrado é que, no campo legal, os hospitais estão adotando os questionáveis protocolos de pontos, que muitas vezes classificam cirurgias de baixo risco como moderado e até mesmo alto, em decorrência do tempo cirúrgico. Fica difícil provar para um perito que os protocolos sugeridos são questionáveis, caso ocorra alguma complicação de TEV, por isso deve haver uma mobilização por parte dos cirurgiões plásticos para que essas recomendações não sejam adotadas por hospitais, prevalecendo a autonomia médica.
Apesar da facilidade da via oral, do custo mais baixo e de os novos anticoagulantes orais demonstrarem mais eficácia e a mesma segurança quando comparados à dose recomendada de enoxaparina na profilaxia do TEV19, essas drogas não têm método de reversão comprovadamente eficaz.
CONCLUSÕES
A profilaxia antitrombótica deve ser adotada. O custo dos novos anticoagulantes orais, dabigatran e rivaroxaban, é mais baixo que o da enoxaparina, porém essas drogas não têm método de reversão comprovadamente eficaz.
Devem ser realizados mais estudos para cálculo de incidência de TVP e EP para cada procedimento cirúrgico para a elaboração de um protocolo mais fidedigno que indique a quimioprofilaxia em nossa especialidade.
REFERÊNCIAS
1. Comerota AJ, Stewart GJ. Current concepts in etiology of postoperative deep vein thrombosis. In: Callow AD, Ernst CB, eds. Vascular surgery: theory and practice. Stanford: Appleton & Lange; 1999. p. 1453-61.
2. Sandri JL. Profilaxia do tromboembolismo em cirurgia plástica. In: Carreirão S, Cardim V, Goldenberg D, eds. Cirurgia Plástica. Sociedade Brasileira de Cirurgia Plástica. São Paulo: Atheneu; 2005. p. 119-26.
3. McDevitt NB. Deep vein thrombosis prophylaxis. American Society of Plastic and Reconstructive Surgeons. Plast Reconstr Surg. 1999;104(6):1923-8.
4. Reinisch JF, Bresnick SD, Walker JW, Rosso RF. Deep venous thrombosis and pulmonary embolus after face lift: a study of incidence and prophylaxis. Plast Reconstr Surg. 2001;107(6):1570-7.
5. Rohrich RJ, Rios JL. Venous thromboembolism in cosmetic plastic surgery: maximizing patient safety. Plast Reconstr Surg. 2003;112(3):871-2.
6. Davison SP, Venturi ML, Attinger CE, Baker SB, Spear SL. Prevention of venous thromboembolism in the plastic surgery patient. Plast Reconstr Surg. 2004;114(3):43E-51E.
7. Most D, Kozlow J, Heller J, Shermak MA. Thromboembolism in plastic surgery. Plast Reconstr Surg. 2005;115(2):20e-30e.
8. The Doctors Company. Deep venous thrombosis and pulmonary embolism in plastic surgery office procedures. Disponível em: http://www.thedoctors.com. Acesso em: 31/3/2012.
9. Conroy FJ, Thornton DJ, Mather DP, Srinivasan J, Hart NB. Thromboembolic prophylaxis in plastic surgery: a 12-year follow up in the UK. J Plast Reconstr Aesthet Surg. 2006;59(5):510-4.
10. Newall G, Ruiz-Razura A, Mentz HA, Patronella CK, Ibarra FR, Zarak A. A retrospective study on the use of a low-molecular-weight heparin for thromboembolism prophylaxis in large-volume liposuction and body contouring procedures. Aesthetic Plast Surg. 2006;30(1):86-97.
11. Young VL, Watson ME. The need for venous thromboembolism (VTE) prophylaxis in plastic surgery. Aesthet Surg J. 2006;26(2):157-75.
12. Green D. VTE prophylaxis in aesthetic surgery patients. Aesthet Surg J. 2006;26(3):317-24.
13. Broughton G 2nd, Rios JL, Rohrich RJ, Brown SA. Deep venous thrombosis prophylaxis practice and treatment strategies among plastic surgeons: survey results. Plast Reconstr Surg. 2007;119(1):157-74.
14. Collins R, Scrimgeour A, Yusuf S, Peto R. Reduction in fatal pulmonary embolism and venous thrombosis by perioperative administration of subcutaneous heparin. Overview of results of randomized trials in general, orthopedic, and urologic surgery. N Engl J Med. 1988;318(18):1162-73.
15. Mismetti P, Laporte S, Darmon JY, Buchmüller A, Decousus H. Meta-analysis of low molecular weight heparin in the prevention of venous thromboembolism in general surgery. Br J Surg. 2001;88(7):913-30.
16. Most D, Kozlow J, Heller J, Shermak MA. Thromboembolism in plastic surgery. Plast Reconstr Surg. 2005;115(2):20e-30e.
17. Gould MK, Garcia DA, Wren SM, Karanicolas PJ, Arcelus JI, Heit JA, et al. American College of Chest Physicians. Prevention of VTE in non-orthopedic surgical patients: Antithrombotic Therapy and Prevention of Thrombosis. 9th ed. American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012;141(2 Suppl):e227S-77S.
18. Wikipedia. Dabigatran/Rivaroxaban. Disponível em: http://www.en.wikipedia.org Acesso em: 31/3/2012.
19. Nieto JA, Espada NG, Merino RG, González TC. Dabigatran, rivaroxaban and apixaban versus enoxaparin for thomboprophylaxis after total knee or hip arthroplasty: pool-analysis of phase III randomized clinical trials. Thromb Res. 2012;130(2):183-91.
20. Cassone A, Viegas AC, Sguizzatto GT, Cabrita HABA, Aquino MA, Furlaneto ME, et al. Trombose venosa profunda em artroplastia total de quadril. Rev Bras Ortop. 2002;37(5):153-61.
21. Bowler DJ, Bale E, O'Byrne J. Factor V Leiden: prevalence and thromboembolic complications after total hip replacement in Ireland. Ir J Med Sci. 2007;176(4):273-7.
22. Bailey SH, Pannucci C, Dreszer G, Fischer CF, Jaber C, Jaber RM, et al. Post-operative enoxaparin does not increase risk for re-operative hematoma in plastic surgery patients: preliminary results of the Psefs Venous Thromboembolism Prevention Study (Vteps). Plast Reconstr Surg. 2011;127:12.
23. Seruya M, Baker SB. MOC-PS(SM) CME article: venous thromboembolism prophylaxis in plastic surgery patients. Plast Reconstr Surg. 2008;122(3 Suppl):1-9.
1. Cirurgião plástico, membro associado da Sociedade Brasileira de Cirurgia Plástica (SBCP), São Paulo, SP, Brasil
2. Médico formado em Hematologia e Hemoterapia pelo Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo, especialista em Hematologia e Hemoterapia pela Sociedade Brasileira de Hematologia e Hemoterapia, São Paulo, SP, Brasil
3. Cirurgião plástico, membro titular da SBCP, regente do Serviço de Cirurgia Plástica Professor Doutor Oswaldo de Castro, São Paulo, SP, Brasil
Correspondência para:
André Toshiaki Toda Nishimura
Alameda Lorena, 2.015 - Cerqueira César
São Paulo, SP, Brasil - CEP 01424-002
E-mail: andre_nishi@me.com
Artigo submetido pelo SGP (Sistema de Gestão de Publicações) da RBCP.
Artigo recebido: 17/4/2012
Artigo aceito: 1º/7/2012
Trabalho realizado no Serviço de Cirurgia Plástica Professor Doutor Oswaldo de Castro, São Paulo, SP, Brasil.


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter