

Original Article - Year 2013 - Volume 28 -
Protocolo de prevenção de tromboembolismo venoso no Instituto Ivo Pitanguy: eficácia e segurança em 1.351 pacientes
Protocol for the prevention of venous thromboembolism at the Ivo Pitanguy Institute: efficacy and safety in 1351 patients
RESUMO
INTRODUÇÃO: Eventos tromboembólicos causam grande preocupação, em decorrência das altas taxas de morbidade e mortalidade existentes e da possibilidade de apresentação clínica com sintomas escassos e, muitas vezes, inespecíficos. A prevenção é a maneira mais eficaz de lidar com esse tipo de evento, que, uma vez estabelecido, pode levar rapidamente à morte.
MÉTODO: Foi realizado estudo retrospectivo, no período entre maio de 2009 e maio de 2010, com pacientes submetidos a cirurgia plástica no Instituto Ivo Pitanguy. Todos os pacientes foram submetidos ao protocolo de prevenção de tromboembolismo venoso, após serem avaliados quanto aos fatores predisponentes e de risco. A soma desses fatores gerou uma pontuação, que determinou a profilaxia a ser adotada.
RESULTADOS: Foram avaliados 1.351 pacientes durante o período de um ano. Não houve incidência de tromboembolismo venoso. Foram observados 16 casos de hematoma, 9 (56,25%) deles ocorreram após profilaxia com heparina e 7 (43,75%) sem o uso de quimioprofilaxia.
CONCLUSÕES: O protocolo para prevenção de tromboembolismo venoso no Instituto Ivo Pitanguy foi eficaz, sem ocorrência de eventos tromboembólicos e com incidência de hematomas abaixo da encontrada na literatura médica.
Palavras-chave: Tromboembolia venosa/prevenção & controle. Trombose venosa/prevenção & controle. Cirurgia plástica.
ABSTRACT
INTRODUCTION: Thromboembolic events are a serious concern due to the high rates of morbidity and mortality as well as the possibility of existing disease presenting with scarce and often nonspecific symptoms. Prevention is the most effective management method for this kind of event, which can quickly lead to death once it occurs.
METHODS: A retrospective study was conducted between May 2009 and May 2010 on patients undergoing plastic surgery at the Ivo Pitanguy Institute. All patients underwent the protocol for the prevention of venous thromboembolism after being assessed for risk factors. These factors were summed to generate a score, which determined the prophylaxis to be implemented.
RESULTS: During one year, 1351 patients were assessed. There was no incidence of venous thromboembolism. There were 16 cases of hematoma, 9 (56.25%) of which occurred after heparin prophylaxis and 7 (43.75%) of which occurred without the use of prophylaxis.
CONCLUSIONS: The protocol for the prevention of venous thromboembolism at the Ivo Pitanguy Institute was effective, with no occurrence of VTE cases and the incidence of hematomas remained below that found in the medical literature.
Keywords: Venous thromboembolism. Venous thrombosis/prevention & control. Plastic surgery.
Eventos tromboembólicos causam grande preocupação, em decorrência das altas taxas de morbidade e mortalidade existentes e da possibilidade de apresentação clínica com sintomas escassos e, muitas vezes, inespecíficos.
Embolia pulmonar (EP) é a principal causa de óbito em pacientes hospitalizados. Ocorrem 200 mil novos casos por ano, geralmente de início súbito e levando ao óbito nas primeiras 2 horas, antes mesmo de a terapia ser iniciada ou surtir efeito1. A prevenção é, portanto, mais efetiva que o tratamento da doença já estabelecida.
Os procedimentos cirúrgicos são fatores importantes na gênese do tromboembolismo, pois associam diversos fatores predisponentes, como trauma tissular, decúbito, restrição à movimentação, hipovolemia e estase sanguínea. Particularmente no cenário das cirurgias plásticas, é importante ressaltar o fato de que a maioria das cirurgias estéticas é realizada em mulheres em faixas etárias em que o uso de anticoncepcionais ou a reposição hormonal são frequentes.
O risco absoluto de trombose venosa profunda (TVP) em ambiente hospitalar é estimado em 15% a 40% em pacientes cirúrgicos, e estudo publicado em 2009 evidenciou que 80% dos cirurgiões plásticos já vivenciaram TVP e 53%, EP2.
Em 2001, Reinisch et al.3 relataram taxas de 0,35% de TVP e de 0,14% de tromboembolismo pulmonar (TEP) em pacientes submetidos a cirurgia de face. Aly et al.4, em 2003, reportaram incidência de 9,3% de TEP em pacientes submetidos a dermolipectomia circunferencial, e de 6,6% em abdominoplastias associadas a outra cirurgia.
A estratificação de risco para tromboembolismo, muito comum nos estudos clínicos, e na qual vêm sendo baseados algoritmos e protocolos médicos, é essencial para racionalizar custos e minimizar complicações e efeitos adversos.
Weinmann & Salzman5, em 1994, atribuíram uma pontuação aos fatores de risco identificados para o tromboembolismo, e criaram uma classificação em grupos de baixo, moderado e alto riscos, com base na qual definiram conduta preventiva.
Em 1999, a American Society of Plastic and Reconstructive Surgeons6 organizou o que chamou de "força-tarefa", sugerindo algumas medidas profiláticas para tromboembolismo venoso (TEV), mas não foi criado um protocolo.
O American College of Chest Physicians (ACCP), em 2001, definiu algumas diretrizes para prevenção de TEV em pacientes cirúrgicos, como flexão dos joelhos em aproximadamente 5 graus, para maximizar o fluxo sanguíneo nas veias poplíteas, compressão pneumática intermitente em todos os pacientes de risco moderado, heparina de baixo peso molecular (HBPM) em pacientes de alto risco e manutenção da quimioprofilaxia até que o paciente esteja deambulando normalmente.
Em 2003, foi publicado trabalho brasileiro descrevendo o protocolo de prevenção de TVP em cirurgia plástica, desenvolvido no Hospital Israelita Albert Einstein-SP, fruto de um grupo de estudo multidisciplinar instituído em 19997. Esse protocolo empregou a estratificação de riscos já utilizada por Weinmann & Salzman5, em 1994.
Rohrich & Rios8 e Davison et al.9 afirmam que esses cuidados devem ser universais e ressaltam que alguns casos merecem medidas mais agressivas, como pacientes submetidos a abdominoplastias, cirurgias combinadas ou procedimentos com duração > 4 horas. Rohrich & Rios8 defendem a deambulação precoce, no dia da cirurgia, e o uso da HBPM rotineiramente no pré-operatório.
Em nossa instituição foi estabelecido um protocolo de prevenção em 200710, baseado nos trabalhos de Davison et al.9 e Caprini et al.11. Em 2009, porém, com a atualização das diretrizes do ACCP (2008) e a publicação de novos estudos específicos em cirurgia plástica, esse protocolo foi modificado, buscando garantir mais segurança e preconizando o início mais precoce da quimioprofilaxia.
Existe grande resistência dos cirurgiões à adoção da quimioprofilaxia, por receio de aumento de eventos hemorrágicos e de suas complicações.
Este trabalho visa a demonstrar a eficácia do protocolo de prevenção de doenças tromboembólicas instituído no Serviço do Professor Ivo Pitanguy e comprovar a equivalência nas taxas de hematomas com e sem o uso da HBPM.
MÉTODO
Foi realizado estudo retrospectivo, no período entre maio de 2009 e maio de 2010, com pacientes submetidos a cirurgia plástica (estética e reparadora) no Instituto Ivo Pitanguy. Todos os pacientes assinaram o termo de consentimento livre e esclarecido, sendo informados sobre o protocolo vigente de prevenção de TEV.
Todos os pacientes foram avaliados quanto aos fatores de risco - predisponentes ou de exposição - para TEV, classificados quanto ao grau de risco e submetidos à profilaxia indicada.
O protocolo de prevenção do Serviço vigente no período de 2007 a 2009 era baseado nas recomendações do protocolo americano de Davison-Caprini, que classificava os pacientes em 4 categorias de risco: risco baixo (soma total dos fatores de risco = 0 ou 1), risco moderado (2), risco alto (3 e 4) e risco muito alto (> 4). De acordo com esse protocolo, a quimioprofilaxia com HBPM está indicada apenas na categoria risco muito alto e sempre 12 horas após o procedimento cirúrgico12,13.
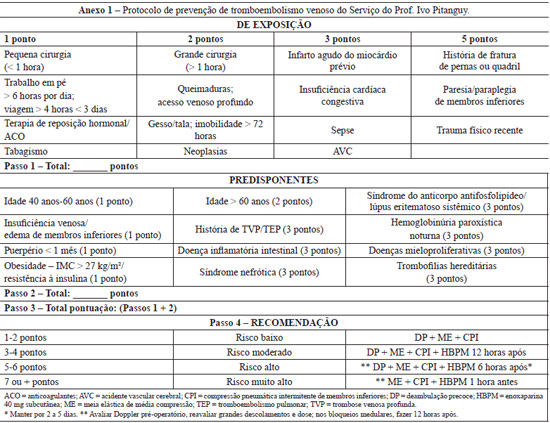
O atual protocolo de prevenção de doença tromboembólica baseia-se nas diretrizes atuais do ACCP, com adaptações, combinando os modelos de Patronella et al.12, Young & Watson13 e Anger et al.7 (Anexo 1). Como se observa no Anexo 1, os pacientes são avaliados quanto aos fatores de risco a que são expostos e aos fatores predisponentes, gerando uma pontuação que determinará a conduta profilática a ser adotada.
A deambulação precoce, no mesmo dia da cirurgia, é estimulada em todos os pacientes. O uso da meia elástica é indicado a todos os pacientes, desde o procedimento e mantido por uma semana. A compressão pneumática é iniciada após a indução anestésica e mantida até o dia seguinte.
Nesse protocolo, os pacientes são estratificados em 4 classes de risco: risco baixo (soma total de pontos até 2), moderado (3 a 4 pontos), alto (5 a 6 pontos) e muito alto (7 pontos ou mais). A profilaxia medicamentosa já está presente no paciente classificado como de risco moderado (12 horas após o procedimento) e vai se aproximando do evento cirúrgico conforme o grau de risco (6 horas após, na classificação de alto risco, e 1 hora antes, no risco muito alto). Os pacientes que apresentarem risco alto e muito alto devem ser avaliados com ecocardiografia Doppler de membros inferiores no pré-operatório, e a HBPM mantida por 2 dias a 5 dias. Nos grandes descolamentos, avalia-se o uso de metade da dose de HBPM, e nos pacientes submetidos a bloqueios medulares aplica-se a HBPM somente 12 horas após.
O protocolo pode ser alterado, reduzindo ou mesmo suspendendo a HBPM, a critério médico, havendo intercorrência cirúrgica.
Desde a introdução do novo protocolo de prevenção de TEV, todos os registros de intercorrências foram feitos de forma meticulosa (observação do momento do hematoma e horário da realização da profilaxia medicamentosa), evitando vieses.
O critério adotado para definição de hematoma foi descrito pelo Subcomitê de Controle de Anticoagulação da Sociedade Internacional de Trombose e Hemostasia, em 2010, que considera hematoma como qualquer sangramento no sítio cirúrgico que necessite de nova intervenção cirúrgica.
RESULTADOS
Foram avaliados 1.351 pacientes, sendo 9,8% do sexo masculino e 90,2% do sexo feminino, com média de idade de 40,8 anos, variando de 2 anos a 86 anos.
Das cirurgias realizadas, 1.246 (92,2%) foram simples e 105 (7,8%) foram combinadas. Quanto ao tipo de cirurgia, a mamaplastia foi mais prevalente, com 19,7% dos casos, seguida de implante mamário (16,9%), abdominoplastia (16,7%), ritidoplastia (13,6%), rinoplastia (7,5%), lipoaspiração (6,4%), blefaroplastia (5%) e outros procedimentos (otoplastias, microimplante capilar, exérese de lesões de pele, implante glúteo, implante de panturrilha, reconstrução de palato e outras), que, somados, equivalem a 14,2% (Figura 1).
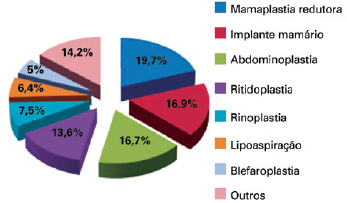
Figura 1 - Porcentagem de cirurgias específicas realizadas.
De acordo com o protocolo, 34,6% dos pacientes foram classificados como risco baixo, 58%, moderado, 6,7%, alto, e 0,7%, muito alto (Figura 2). Houve predominância do grupo de risco moderado, a partir do qual já foi empregado o uso de quimioprofilaxia.
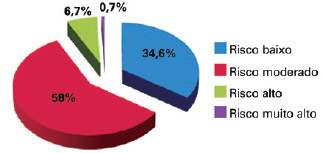
Figura 2 - Distribuição dos pacientes segundo grupo de risco.
Durante o período observado, não houve nenhum caso de TEV. Foram observados 16 (1,18%) casos de hematoma, sendo 9 (56,25%) após profilaxia com heparina e 7 (43,75%) sem o emprego de profilaxia medicamentosa (Figura 3). Foram identificados 8 hematomas após lifting facial, 2 após lipoaspiração, 3 após implante mamário, 1 após mamaplastia, 1 após abdominoplastia e 1 após colocação de expansor em mama. Quanto à distribuição dos hematomas conforme o tipo de profilaxia realizada, 43,75% ocorreram em pacientes que não fizeram uso da heparina, 43,75% com administração de heparina 12 horas após a cirurgia e 12,5% com administração de heparina 6 horas após a cirurgia (Figura 4). Não foram observados hematomas nos pacientes que fizeram uso de heparina 1 hora antes da cirurgia. Dos 16 pacientes que apresentaram hematoma, 5 eram hipertensos e 3, dislipidêmicos em uso de estatinas.
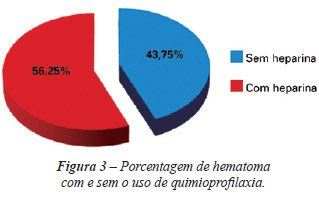
Figura 3 - Porcentagem de hematoma com e sem o uso de quimioprofilaxia.
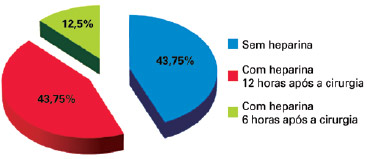
Figura 4 - Porcentagem de hematoma de acordo com a profilaxia utilizada.
DISCUSSÃO
Em nosso serviço, todos os pacientes submetidos a procedimento cirúrgico passam por rigorosa avaliação clínica. Nessa avaliação, considera-se a cirurgia a ser realizada, o tipo de anestesia e o grau de risco do paciente. Definida a profilaxia adequada, é realizado o acompanhamento transoperatório e mantida vigilância pós-operatória.
O protocolo de prevenção é realizado individualizadamente e é base para conduta clínica pós-operatória, podendo ser modificado de acordo com condições excepcionais encontradas pelo cirurgião durante a cirurgia, levando-se em conta o risco pré-operatório previsto e o risco e o benefício das condutas preestabelecidas.
Na primeira consulta, o paciente é também orientado a suspender medicações com potencial trombogênico, como anticoncepcionais orais e terapia de reposição hormonal, um mês antes da cirurgia e retornar seu uso somente 2 semanas após, quando já deve se encontrar deambulando normalmente. Várias orientações pré-operatórias são feitas e, para os pacientes que viajam nos dias que antecedem a cirurgia, são reforçados alguns pontos, como: não ingerir bebida alcoólica 48 horas antes da cirurgia; ingerir líquidos durante a viagem; movimentar as pernas frequentemente e caminhar a cada 2 horas, quando possível; e usar meia elástica de média compressão, caso não haja contraindicação.
Na alta hospitalar, as orientações são de ingesta abundante de líquidos, deambulação frequente e manutenção do uso das meias elásticas por 1 semana.
Segundo as recomendações contidas nas diretrizes do ACCP, de 2008, e conforme estudos publicados, a profilaxia medicamentosa deve ser iniciada antes ou logo após a cirurgia e deve ser continuada até o paciente deambular normalmente. A heparina iniciada 2 horas antes ou 4 horas a 6 horas após a cirurgia com metade da dose usual reduziu a formação de trombos quando comparada com o início 12 horas ou mais após. O risco de eventos hemorrágicos foi igual nos dois grupos. Patronella et al.12 realizaram estudo retrospectivo com 3.871 pacientes, e as recomendações oriundas desse estudo foram: considerar ácido fólico e vitaminas do complexo B, 2 semanas antes da cirurgia; evitar hipotermia; posicionamento no leito com flexão de 5 graus dos joelhos; meias elásticas e compressor pneumático externo de membros inferiores; HBPM 40 mg 1 hora após a cirurgia, nos grupos de risco alto, uma vez por dia, por 72 horas; monitorização do paciente por 4 semanas.
Estudo publicado por Newall et al.14 demonstrou que a HBPM empregada 1 hora após a cirurgia e mantida por 3 dias consecutivos, em pacientes de alto risco, resultou na ausência de TEV, sem aumento das taxas de hematoma em comparação àquelas publicadas na literatura.
Em nosso protocolo, no grupo de alto risco, a heparina é iniciada 1 hora antes da cirurgia, objetivando-se atingir o pico de ação durante o procedimento cirúrgico.
Embora o risco de TEV seja real, ainda há muita relutância no emprego da quimioprofilaxia, pelo receio de complicações hemorrágicas. Somadas a essa dificuldade estão as dúvidas na elaboração de diretrizes, em decorrência dos escassos dados na literatura em cirurgia plástica. Qual é a incidência real de TEV na cirurgia plástica? Qual é a frequência de complicações? Qual é o momento ideal para início da profilaxia? Qual é a dose ideal? Vale lembrar que as diretrizes do ACCP não incluem a cirurgia plástica e que não há estudos com graus de evidência A e B para o estabelecimento de condutas nessa especialidade; entretanto, a necessidade de protocolos de prevenção é imperativa, já que o TEV é a causa mais importante de óbito prevenível após cirurgia.
Uma estratégia preventiva racional deve ser estabelecida com o conhecimento das condições de risco que cada paciente apresenta, papel primordial da avaliação pré-operatória. A ideia de baixo risco de TEV em pacientes de cirurgia plástica é enganosa, já que aproximadamente dois terços dos pacientes com TEV são assintomáticos. A menor importância dada ao assunto deve-se mais ao não reconhecimento do problema, que pode assumir proporções catastróficas, já que muitas vezes o TEP fatal pode ser a primeira e única manifestação da doença.
A demora no início da profilaxia leva a efeito antitrombótico subótimo, sem vantagem de segurança.
Não há evidência de aumento de risco de hematomas com o uso de heparina nas cirurgias plásticas, conforme demonstrado no artigo de Rohrich & Rios8.
Metanálises e ensaios clínicos randomizados duplo-cegos demonstraram pouco ou nenhum aumento da taxa de sangramentos com HBPM em cirurgias2,15.
Em 2008, outro estudo em cirurgia plástica, realizado por Liao et al.16, revelou que não houve aumento do risco de hematomas após reconstrução de mama com TRAM (do inglês transverse rectus abdominis myocutaneous) e utilização de quimioprofilaxia com heparina.
O uso de anticoagulantes em pacientes submetidos a lifting facial é, em geral, muito temido, em decorrência do receio de aumento do sangramento, que pode ocasionar hematoma expansivo, com potencial de necrose tissular.
Um dos princípios da medicina é o da não-maleficência. Pacientes em cirurgia plástica são geralmente saudáveis, têm expectativas elevadas e baixa tolerância a adversidades. Mais do que nunca, o cirurgião plástico deve prezar pela segurança desses pacientes, prevenindo essa temida complicação.
Um estudo de revisão de 126 casos de ritidectomia de um mesmo cirurgião apresentou incidência de 5,6% de hematomas que necessitaram de abordagem cirúrgica e de 16,2% de sangramento pós-operatório com o emprego de HBPM profilática, realizada 2 horas antes da cirurgia17. Nesse estudo, o tempo médio de cirurgia foi de 95 minutos, variando de 45 minutos a 145 minutos.
Pitanguy & Ceravolo18 realizaram estudo sobre hematomas em ritidoplastia, reportando taxas de hematoma na literatura variando de 0,9% a 8%, sem o emprego de heparina profilática.
No presente estudo, não ocorreu nenhum caso de TEV e houve 16 casos de hematoma. Dentre esses, 9 foram observados após profilaxia medicamentosa e 7 casos sem o emprego de quimioprofilaxia. Pacientes que receberam heparina 12 horas após a cirurgia foram o maior grupo, e não foram observados hematomas nos pacientes que fizeram uso de heparina 1 hora antes da cirurgia, o que reforça que os fatores de risco para sangramento são mais importantes do que o uso da heparina no desenvolvimento do hematoma.
Dos 9 pacientes que apresentaram hematoma após o uso da heparina, 3 eram hipertensos e 3 eram dislipidêmicos, estando 1 deles em uso regular de estatinas, que têm efeito anticoagulante. O menor intervalo para o surgimento do hematoma foi de 5 horas após administração de heparina, que coincide com o pico de ação da droga, e o maior, de 16 horas.
É importante lembrar que 43,8% dos casos de hematoma não fizeram uso de medicação anticoagulante.
As taxas de incidência de hematoma em cirurgia plástica publicadas na literatura, e que usamos como referência, são: 1,1% a 2% na mamaplastia de aumento com prótese19, 4,5% a 8% em ritidoplastia, 3% a 4,6% em abdominoplastia20, 2% a 10% em lipoplastias e 0,7% em mamaplastia redutora. Em lipoaspiração não houve diferenciação nos estudos entre seromas e hematomas, dificultando a definição de um porcentual específico para hematoma.
As taxas de incidência de hematoma encontradas no pres ente trabalho foram mais baixas que as descritas na literatura, reforçando que estamos comparando números estatísticos em situações clínicas diferentes, o que corrobora o fato de que, mesmo com o emprego da HBPM, não houve aumento da incidência de hematoma.
CONCLUSÕES
O protocolo de prevenção de TEV no Instituto Ivo Pitanguy foi eficaz, sem ocorrência de eventos tromboembólicos e com incidência de hematomas abaixo da encontrada na literatura médica.
O Serviço do Prof. Ivo Pitanguy sempre se destacou pela excelência e pioneirismo em ensino, pesquisa e prática assistencial em cirurgia plástica estética e reconstrutora. É preciso oferecer ao paciente o melhor resultado cirúrgico, sempre amparado pelas melhores condições de segurança, o que muitas vezes implica mudança de hábitos e condutas. A prevenção bem-feita, com critérios bem estabelecidos, é a solução para evitarmos óbitos e o alto custo de exames e tratamentos complementares.
REFERÊNCIAS
1. King CS, Holley AB, Jackson JL, Shorr AF, Moores LK. Twice vs. three times daily heparin dosing for thromboembolism prophylaxis in the general medical population: a metaanalysis. Chest. 2007;131(2):507-16.
2. Miszkiewicz K, Perreault I, Landes G, Harris PG, Sampalis JS, Dio-nyssopoulos A, et al. Venous thromboembolism in plastic surgery: incidence, current practice and recommendations. J Plast Reconstr Aesthet Surg. 2009;62(5):580-8.
3. Reinisch JF, Bresnick SD, Walker JW, Rosso RF. Deep venous thrombosis and pulmonary embolus after face lift: a study of incidence and prophylaxis. Plast Reconstr Surg. 2001;107(6):1570-5.
4. Aly AS, Cram AE, Chao M, Pang J, McKeon M. Belt lipectomy for circumferential truncal excess: the University of Iowa experience. Plast Reconstr Surg. 2003;111(1):398-413.
5. Weinmann EE, Salzman EW. Deep-vein thrombosis. N Engl J Med. 1994;331(24):1630-41.
6. McDevitt NB. Deep vein thrombosis prophylaxis. American Society of Plastic and Reconstructive Surgeons. Plast Reconstr Surg. 1999;104(6):1923-8.
7. Anger J, Baruzzi ACA, Knobel E. Um protocolo de prevenção de trombose venosa profunda em cirurgia plástica. Rev Bras Cir Plást. 2003;18(1):47-54.
8. Rohrich RJ, Rios JL. Venous thromboembolism in cosmetic plastic surgery: maximizing patient safety. Plast Reconstr Surg. 2003;112(3):871-2.
9. Davison SP, Venturi ML, Attinger CE, Baker SB, Spear SL. Prevention of venous thromboembolism in the plastic surgery patient. Plast Re-constr Surg. 2004;114(3):43e-51e.
10. Paiva RA, Pitanguy I, Amorim NFG, Berger R, Shdick HA, Holanda TA. Tromboembolismo venoso em Cirurgia Plástica: protocolo de prevenção na Clínica Ivo Pitanguy. Rev Bras Cir Plást. 2010;25(4):583-8.
11. Caprini JA, Arcelus JI, Reyna JJ. Effective risk stratification of surgical and nonsurgical patients for venous thromboembolic disease. Semin Hematol. 2001;38(2 Suppl 5):12-9.
12. Patronella CK, Ruiz-Razura A, Newall G, Mentz HA, Arango ML, As-savapokee T, et al. Thromboembolism in high-risk aesthetic surgery: experience with 17 patients in a review of 3871 consecutive cases. Aesthet Surg J. 2008;28(6):648-55.
13. Young V, Watson M. The need for venous thromboembolism (VTE) prophylaxis in plastic surgery. Aesthet Surg J. 2006;26(2):157-75.
14. Newall G, Ruiz-Razura A, Mentz HA, Patronella CK, Ibarra FR, Zarak A. A retrospective study on the use of a low-molecular-weight he-parin for thromboembolism prophylaxis in large-volume liposuction and body contouring procedures. Aesthetic Plast Surg. 2006;30(1):86-95.
15. Levine MN, Raskob G, Beyth RJ, Kearon C, Schulman S. Hemorrhagic complications of anticoagulant treatment: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest. 2004;126(3 suppl):287S-310S.
16. Liao EC, Taghinia AH, Nguyen LP, Yueh JH, May JW Jr, Orgill DP. Incidence of hematoma complication with heparin venous thrombosis prophylaxis after TRAM flap breast reconstruction. Plast Reconstr Surg. 2008;121(4):1101-7.
17. Durnig P, Jungwirth W. Low-molecular-weight heparin and postoperative bleeding in rhytidectomy. Plast Reconstr Surg. 2006;118(2):502-9.
18. Pitanguy I, Ceravolo MP. Hematoma postrhytidectomy: how we treat it. Plast Reconstr Surg. 1981;67(4):526-9.
19. Codner MA, Mejia JD, Locke MB, Mahoney A, Thiels C, Nahai FR, et al. A 15-year experience with primary breast augmentation. Plast Reconstr Surg. 2011;127(3):1300-10.
20. Stewart KJ, Stewart DA, Coghlan B, Harrison DH, Jones BM, Wa-terhouse N. Complications of278 consecutive abdominoplasties. J Plast Reconstr Aesthet Surg. 2006;59(11):1152-5.
1. Mestre em Medicina Intensiva pela Universidade Federal do Rio de Janeiro, especialista em Medicina Intensiva, chefe de Serviço de Medicina Intensiva no Instituto Ivo Pitanguy, Rio de Janeiro, RJ, Brasil.
2. Médico cardiologista formado pelo Instituto Nacional de Cardiologia do Rio de Janeiro, membro do corpo clínico do Serviço de Medicina Intensiva no Instituto Ivo Pitanguy, Rio de Janeiro, RJ, Brasil
3. Membro titular da Sociedade Brasileira de Cirurgia Plástica (SBCP), professora assistente no Departamento de Cirurgia Plástica da Pontifícia Universidade Católica do Rio de Janeiro (PUC-Rio), Rio de Janeiro, RJ, Brasil
4. Membro associado da SBCP, professora assistente no Departamento de Cirurgia Plástica da PUC-Rio, Rio de Janeiro, RJ, Brasil
5. Patrono da SBCP, membro da Academia Nacional de Medicina e da Academia Brasileira de Letras, professor titular do Curso de Pós-Graduação em Cirurgia Plástica da PUC-Rio e do Instituto Carlos Chagas, Rio de Janeiro, RJ, Brasil
Correspondência para:
Rita Azevedo de Paiva
Rua Visconde de Pirajá, 330 - ap. 604 - Ipanema
Rio de Janeiro, RJ, Brasil - CEP 22410-001
E-mail: ritaazevedodepaiva@hotmail.com
Artigo submetido pelo SGP (Sistema de Gestão de Publicações) da RBCP.
Artigo recebido: 14/8/2012
Artigo aceito: 13/1/2013
Trabalho realizado no Instituto Ivo Pitanguy, Rio de Janeiro, RJ, Brasil.


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter