ABSTRACT
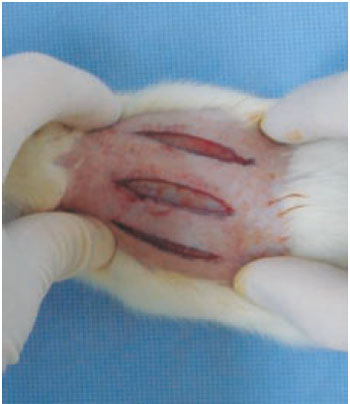
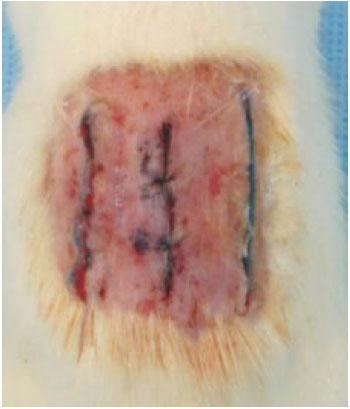
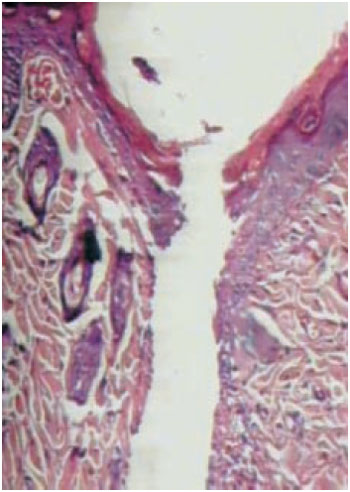
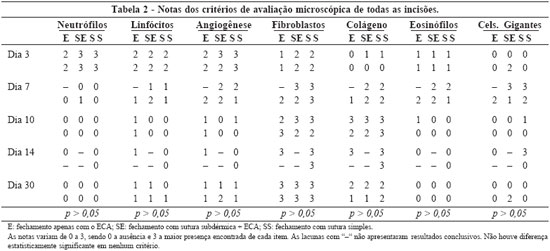
Background: The Ethyl-2-cyanoacrylate (ECA) is a synthetic tissue adhesive used by some physicians in clinical practice in wound closures. They polymerize rapidly to adhere tightly to proteinaceous surfaces, form a strong and flexible bond. This study was performed to evaluate the efficacy and biocompatibility of this polymer (Epiglu®, of Meyer-Haake company, Germany) in skin wound closures, in rat model. Methods: Ten male Wistar rats were subjected to three incisions which were closed using different treatments. The central incision was treated witch Simple suture of nylon 4.0 (control group). Left incision was treated with sub-dermis suture associated with ECA, and right incision only with ECA. Rats were sacrificed on days 3, 7, 14, 21 and 30 after the intervention. The biocompatibility was evaluated due to direct observation: necrosis, inflammation, dermatitis, infection and dehiscence; and microscopy: inflammatory process, angiogenesis, number of fibroblasts, collagen, giants cells and eosynophils. Results: The wound closured only with ECA presented a higher dehiscence level (p < 0.05). It was not observed another macro or microscopic significant difference comparing to the control group (p > 0.05). Conclusion: The use of the ECA is a good option to the skin closure, with good biocompatibility. Special attention must receive the wounds with some tension, where the association with a sub-dermis suture becomes imperative.
Keywords:
Cyanoacrylates. Tissue adhesives. Suture techniques.
RESUMO
Introdução: O Etil-2-cianoacrilato (ECA) é um adesivo tecidual utilizado por alguns médicos na prática clínica para fechamento de lesões de pele. São substâncias que se autopolimerizam quando em contato com a ferida, formando uma cola forte e flexível. Este trabalho foi realizado visando à avaliação da eficácia e da biocompatibilidade deste polímero (Epiglu®, da empresa Meyer- Haake, Alemanha) na síntese de pele, em modelo experimental. Método: Dez ratos Wistar machos foram submetidos a três incisões longitudinais no dorso. A incisão central foi tratada com sutura de pontos simples de nylon 4.0 (grupo controle), a esquerda com sutura subdérmica de nylon 4.0 associado ao ECA, e a direita apenas o ECA. Os animais foram sacrificados nos dias 3, 7, 14, 21 e 30 pós-operatórios. A biocompatibilidade foi avaliada sob observação direta: necrose, inflamação, dermatite de contato, infecção e deiscência; e à microscopia: reação inflamatória, angiogênese, fibroblastos, colágeno, células gigantes e eosinófilos. Resultados: As sínteses realizadas apenas com o ECA apresentaram maior índice de deiscência (p < 0,05). Todos os outros critérios macro e microscópicos avaliados não apresentaram diferenças estatísticas em relação ao controle (p > 0,05). Conclusão: O uso do ECA é uma boa opção de síntese da pele, com boa biocompatibilidade. Atenção deve ser feita às lesões que apresentem algum grau de tensão, onde a associação com a sutura subdérmica torna-se obrigatória.
Palavras-chave:
Cianoacrilatos. Adesivos teciduais. Técnicas de sutura.