

Review Article - Year 2021 - Volume 36 -
Qual o papel dos testes rápidos de diagnóstico de COVID-19 IgM/IgG no pré-operatório de cirurgia plástica estética?
What is the role of rapid diagnostic tests for COVID-19 IgM/IgG in the pre-operative period of cosmetic plastic surgery?
RESUMO
Introdução: A doença pelo novo coronavírus 2019 (COVID-19) surgiu na China e se espalhou globalmente com transmissão mundial sustentada de humano para humano. Os testes de diagnóstico rápido COVID-19 IgM/IgG realizados no momento da admissão hospitalar, antes de cirurgia eletiva, estão entre os métodos de rastreamento pré-operatórios mais amplamente utilizados.
Objetivos: O objetivo deste estudo é avaliar o papel do teste rápido de anticorpos COVID-19 como triagem em pacientes ambulatoriais em cirurgia plástica estética.
Métodos: Uma revisão sistemática foi realizada para estudos publicados desde dezembro de 2019, com vários termos de pesquisa relacionados ao teste rápido de anticorpos para COVID-19 e SARS-CoV-2. Os artigos relevantes foram selecionados por meio da avaliação de títulos e resumos. Artigos pertinentes foram revisados. Dados sobre o nível de evidência, sensibilidade e especificidade foram coletados.
Resultados: A estratégia de revisão produziu 409 manuscritos. Um total de 357 estudos foram duplicados ou mostraram-se não relevantes para a questão de pesquisa. Entre os artigos restantes, 28 eram estudos sem informações sobre precisão e 24 eram manuscritos descrevendo medidas de precisão. A sensibilidade variou de 18,4 a 100%, o valor preditivo positivo variou entre 19,7 e 100%, a especificidade variou entre 94 e 100%, e o valor preditivo negativo ficou entre 20 e 100%.
Conclusão: Os testes de diagnóstico rápido COVID-19 IgM/IgG podem ser imprecisos. Não encontramos nenhuma evidência para apoiar o teste rápido de anticorpos COVID-19 ou SARS-CoV-2 para pacientes ambulatoriais em cirurgia plástica estética.
Palavras-chave: Infecções por coronavírus; Cuidados pré-operatórios; Cirurgia plástica; Epidemiologia; Síndrome respiratória aguda grave.
ABSTRACT
Introduction: The disease by the new coronavirus 2019 (COVID-19) emerged in China and spread globally with sustained worldwide transmission from human to human. The COVID-19 IgM/IgG rapid diagnostic tests performed at the time of hospital admission, before elective surgery, are among the most widely used pre-operative screening methods.
Objectives: This study aims to evaluate the role of the rapid test of COVID-19 antibodies as screening in outpatients in aesthetic plastic surgery. Methods: A systematic review was carried out for studies published since December 2019, with several search terms related to the rapid antibody test for COVID-19 and SARS-CoV-2. The relevant articles were selected through the evaluation of titles and abstracts. Relevant articles have been revised. Data on the level of evidence, sensitivity, and specificity were collected.
Results: The review strategy produced 409 manuscripts. A total of 357 studies were duplicated or proved to be irrelevant to the research question. Among the remaining articles, 28 were studies without precision information, and 24 were manuscripts describing precision measures. The sensitivity varied from 18.4 to 100%; the positive predictive value between 19.7 and 100%; specificity between 94 and 100%; and the negative predictive value between 20 and 100%.
Conclusion: COVID-19 IgM / IgG rapid diagnostic tests may be inaccurate. We found no evidence to support the rapid antibody test COVID-19 or SARS-CoV-2 for outpatients in cosmetic plastic surgery.
Keywords: Coronavirus infections; Pre-operative care; Plastic surgery; Epidemiology; Severe acute respiratory syndrome
INTRODUÇÃO
A doença pelo coronavírus 2019 (COVID-19) surgiu na China e espalhou-se globalmente com transmissão sustentada entre humanos1. Devido à sua natureza altamente contagiosa, disseminação global sem precedentes, sua apresentação clínica agressiva e a falta de tratamento efetivo, a síndrome da infecção respiratória aguda por coronavírus 2 (SARS-CoV-2) está causando a perda de milhares de vidas e ocasionando repercussões incomparáveis nos sistemas de saúde em todo o mundo2.
A infecção causada pelo COVID-19 é uma doença altamente transmissível que apresenta risco significativo tanto para os pacientes, quanto para os profissionais de saúde3. Recentemente, foi demonstrado que altos níveis do vírus estão presentes nas secreções respiratórias durante o período pré-sintomático, que podem durar desde dias até semanas antes dos sintomas característicos da COVID-194. Essa capacidade do vírus de ser transmitido por pessoas sem sintomas é um dos principais motivos da pandemia5.
O diagnóstico de COVID-19 é feito usando características clínicas, laboratoriais e radiológicas6. Como os sintomas e os achados radiológicos do COVID-19 são inespecíficos, a infecção por SARS-CoV-2 deve ser confirmada por testes laboratoriais. Os testes de reação em cadeia da polimerase com transcriptase reversa (RT-PCR) são o padrão ouro para o diagnóstico de COVID- 19, no entanto, é um exame de difícil coleta e seus resultados não são imediatamente disponíveis7. Os testes de diagnóstico rápido para COVID-19 IgM/IgG foram desenvolvidos usando a tecnologia de fluxo lateral para encontrar antígenos do vírus SARS-CoV-2 e detectar anticorpos produzidos por pacientes infectados com COVID-198.
Os testes de triagem são amplamente utilizados para avaliar a probabilidade de membros de uma população definida terem uma doença específica, com poucas exceções, os testes de triagem não diagnosticam a doença9. O teste diagnóstico rápido sorológico realizado no momento da admissão, antes da cirurgia eletiva, está entre os métodos de rastreamento pré-operatório para COVID-19 mais amplamente utilizados10-18.
OBJETIVOS
O objetivo deste estudo é avaliar o papel dos testes rápidos de anticorpos COVID-19 em pacientes ambulatoriais sendo admitidos para a realização de cirurgia plástica estética.
MÉTODOS
Foi realizada uma revisão sistemática da literatura usando os mecanismos de busca em periódicos PubMed, Web of Science e SciELO, para estudos com animais e humanos publicados de dezembro de 2019 a 30 de julho de 2020. Consideramos termos específicos sobre COVID-19 ou SARS-CoV-2 e cirurgia plástica. Foram utilizados os seguintes descritores: “cirurgia plástica”, “cirurgia eletiva”, “COVID-19”, “teste de diagnóstico COVID-19”, “teste de anticorpos sanguíneos COVID-19”, “SARS-CoV-2 teste”. Muitos termos e palavras foram exibidos de maneira semelhante ao procurar artigos. Palavras como “pré-operatório”, “cirúrgico” e “cirurgia” apresentaram resultados semelhantes. Os resultados das palavras e frases investigadas foram analisados por quantidade e qualidade. Documentos escritos em inglês, espanhol, francês, italiano e português foram incluídos. Vídeos, pôsteres e cartas ao editor foram desconsiderados. Dois pesquisadores independentemente selecionaram os artigos relevantes através da avaliação de títulos e resumos. Artigos pertinentes foram revisados pelo terceiro pesquisador. Dados sobre o nível de evidência, sensibilidade, especificidade e valores preditivos de testes diagnósticos rápidos foram coletados.
Este estudo está em conformidade com a declaração de Helsinki e prescinde de avaliação em comitê de ética, visto que não envolve diretamente coleta de dados ou tecidos de seres humanos, apenas pesquisa realizada exclusivamente com textos científicos.
RESULTADOS
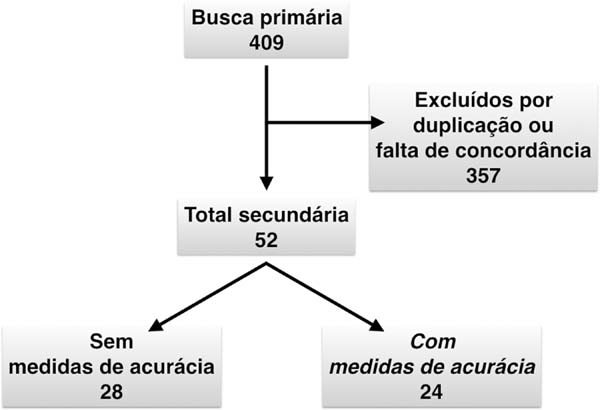
Usando nossa estratégia de busca ativa, a revisão do banco de dados encontrou 409 artigos (Figura 1). Um total de 357 estudos foram duplicados ou considerados não relevantes para a nossa questão de pesquisa. Entre os artigos restantes, 28 eram estudos sem informações sobre a precisão dos testes diagnósticos rápidos e 24 eram estudos descrevendo medidas de acurácia7,8,19-40.
O nível de evidência variou de V a III. A sensibilidade variou de 18,4 a 100%, a especificidade variou de 94 a 100%, o valor preditivo positivo variou entre 19,7 e 100%, e o valor preditivo negativo ficou entre 20 e 100%.
DISCUSSÃO
A experiência limitada acumulada durante a pandemia da COVID-19 demonstrou que o gerenciamento de todas as condições médicas, incluindo cirurgias eletivas, sofreu algum grau de alteração2. Todos nós queremos voltar a trabalhar sem o espectro da COVID-19. Durante as condições extraordinárias da pandemia de COVID-19, as estratégias ideais para o tratamento de pacientes estéticos de maneira individualizada são desconhecidas. Não há consenso na literatura a respeito dos cuidados pré-operatórios, exceto que todos os pacientes devem ser rastreados quanto aos sintomas, antes de serem apresentados ao centro cirúrgico, e os que relatam sintomas de COVID-19 devem ser encaminhados para avaliação adicional.
O teste diagnóstico rápido pode ser produzido de forma rápida e barata. Esse teste qualitativo é pequeno e portátil, geralmente parecido com um teste de gravidez, mostrando ao usuário linhas coloridas para indicar resultados positivos ou negativos8. Os testes diagnósticos rápidos não medem a quantidade de anticorpos no soro do paciente ou se esses anticorpos são capazes de proteger contra futuras infecções, mas eles têm a capacidade de detectar exposição e podem identificar pessoas assintomáticas e pessoas que eliminaram o vírus. Muitos dos testes diagnósticos rápidos disponíveis até o momento carecem de desempenho analítico em relação à sensibilidade e especificidade e precisam ser melhor validados antes de serem empregados no pré-operatório21.
Para o diagnóstico médico, a sensibilidade do teste é a capacidade dele identificar corretamente aqueles com a doença (taxa positiva verdadeira), enquanto a especificidade do teste é a sua capacidade de identificar corretamente aqueles sem a doença (taxa negativa verdadeira). Nesta pesquisa, a sensibilidade variou de 18,4 a 100%, refletindo uma potencial incapacidade de identificar corretamente pessoas que possuem anticorpos para COVID-19. A especificidade variou na faixa de 94 e 100%, demonstrando uma alta capacidade de identificar todos os pacientes que não possuem anticorpos COVID-19.
O valor preditivo negativo é a probabilidade de que pacientes com um resultado negativo num teste diagnóstico rápido realmente não possuam anticorpos COVID-19; em nossa pesquisa, seus valores estavam entre 20 e 100%, podemos afirmar que, em algumas circunstâncias, 80% dos indivíduos com teste negativo podem ter anticorpos COVID-19. Valor preditivo positivo é a probabilidade dos indivíduos com um teste diagnóstico rápido de triagem positivo realmente apresentarem a doença; em nossa pesquisa sua variação ficou entre 60 e 100%, consequentemente, podemos afirmar que, em algumas circunstâncias, 40% dos indivíduos com teste rápido positivo podem não ter anticorpos para COVID- 19. Portanto, os resultados dos testes rápidos parecem ser cientificamente não-confiáveis, e a recomendação da realização desta testagem de forma generalizada, por parte de pacientes ou instituições hospitalares, parece ser inadequada.
Estima-se que anticorpos SARS-CoV-2 IgM possam ser detectados em uma amostra de sangue após 3 dias e anticorpos IgG após 8 dias do início dos sintomas7. A taxa de soroconversão para IgM e IgG foi descrita como 82,7% e 64,7%, respectivamente5. Até o momento, não sabemos se todas as pessoas que se recuperaram da COVID-19 desenvolveram anticorpos e não sabemos até que ponto esses anticorpos protegem os pacientes da reinfecção. Os testes de anticorpos não detectam uma infecção ativa, mas procuram sinais de que uma pessoa foi infectada anteriormente, como mostrado pelos anticorpos que seu sistema imunológico produziu para combater o coronavírus. Com outras doenças, a presença de anticorpos geralmente significa imunidade adquirida por pelo menos algum período de tempo, mas isso ainda não é conhecido no caso da COVID-194.
Os pacientes devem ser submetidos à testagem de screening apenas se um teste positivo resultar em ação imperativa. Este não é o caso dos testes diagnósticos rápidos para COVID-19 antes de uma cirurgia estética, porque o procedimento será realizado independentemente do status de detecção de anticorpos. No caso do novo vírus COVID-19 e da doença SARS-CoV-2 que ele causa em humanos, o objetivo da testagem pré-operatória seria muito simples: identificar pacientes infectados e isolá-los adiando suas cirurgias, tentando reduzir as morbidades do procedimento e reduzindo, assim, o risco de infecção dos profissionais de saúde8. Mas sem um teste perfeito, falsos positivos e falsos negativos podem levar a desfechos significativamente piores.
Tanto os falsos positivos quanto os falsos negativos representam seus próprios perigos únicos, onde quer que ocorra qualquer tipo de teste, mas os falsos negativos são particularmente perigosos para a COVID-19. Duas semanas após a cirurgia, alguns pacientes podem apresentar resultado positivo para COVID-19, apesar do resultado negativo no pré-operatório e podem surgir importantes implicações médico-legais. A infecção foi contraída durante a internação hospitalar? O cirurgião ou sua equipe contaminaram o paciente no acompanhamento ambulatorial pós-operatório? A soroconversão ocorreu porque a cirurgia induziu uma imunossupressão? Um resultado negativo em um teste de diagnóstico rápido para a COVID-19 realizado no pré-operatório pode ser uma evidência médico-legal perigosa para os cirurgiões e entidades hospitalares.
Testes de anticorpos são polivalentes: esses exames sorológicos são de importância crítica para determinar a soroprevalência, a exposição prévia e identificar doadores humanos altamente reativos para a geração de soro convalescente terapêutico4. Eles também apoiarão o rastreamento e a triagem de contato dos profissionais de saúde para identificar aqueles que já estão imunes.
É plausível que várias limitações possam ter influenciado os resultados obtidos nesta pesquisa. A exclusão de artigos em idiomas asiáticos é uma delas, visto que muito do conhecimento sobre a COVID-19 vem desta área geográfica, contudo não havia entre os pesquisadores algum com conhecimento destas línguas e consideramos que os tradutores eletrônicos não sejam fidedignos. Contudo, muitos destes estudos trariam uma informação com validade externa limitada para pacientes das Américas, visto que as mutações de COVID-19 são frequentes e a maior parte dos testes diagnósticos rápidos utilizados por lá, não estão disponíveis em nosso continente. Uma revisão sistemática bem projetada beneficia a evolução do conhecimento, identificando onde há falta de informações científicas e fornecendo uma sinopse das evidências disponíveis. A credibilidade das revisões sistemáticas pode ser comprometida por viés de relatórios, que surgem quando a divulgação de artigos publicados é influenciada pela natureza dos resultados. Nossos achados baseiam-se em um número limitado de artigos, os resultados de tais análises devem, consequentemente, ser tratados com a máxima cautela.
Faltam ensaios clínicos controlados, e os estudos futuros devem examinar a segurança e a eficácia dos testes diagnósticos rápidos para a COVID-19, visando obter resultados mais consistentes e estabelecer recomendações para seu adequado uso.
CONCLUSÃO
Os testes de diagnóstico rápido COVID-19 IgM/IgG parecem ser imprecisos. Não encontramos nenhuma evidência para apoiar o teste rápido de anticorpos COVID-19 ou SARS-CoV- 2 como triagem de pacientes ambulatoriais de cirurgia plástica estética. Estudos futuros sobre o tema são necessários para validar diferentes testes de diagnóstico laboratorial.
REFERÊNCIAS
1. Contini C, Di Nuzzo M, Barp N, Bonazza A, De Giorgio R, Tognon M, et al. The novel zoonotic COVID-19 pandemic: an expected global health concern. J Infect Dev Ctries. 2020 Mar;14(3):254-64. DOI: https://doi.org/10.3855/jidc.12671
2. Patel V, Jimenez E, Cornwell L, Tran T, Paniagua D, Denktas AE, et al. Cardiac surgery during the COVID-19 pandemic: perioperative considerations and triage recommendations. J Am Heart Assoc. 2020 Jul;9(13):e017042. DOI: https://doi.org/10.1161/jaha.120.017042
3. He W, Yi GY, Zhu Y. Estimation of the basic reproduction number, average incubation time, asymptomatic infection rate, and case fatality rate for COVID-19: meta-analysis and sensitivity analysis. J Med Virol. 2020 Mai;92(1):2543-50. DOI: https://doi.org/10.1002/jmv.26041
4. Kim SE, Jeong HS, Yu Y, Shin SU, Kim S, Oh TH, et al. Viral kinetics of SARS-CoV-2 in asymptomatic carriers and presymptomatic patients. Int J Infect Dis. 2020 Jun;95:441-3.
5. Wong MC, Teoh JY, Huang J, Wong SH. Strengthening early testing and surveillance of COVID-19 to enhance identification of asymptomatic patients. J Infect. 2020 Ago;81(2):E112-3. DOI: https://doi.org/10.1016/j.jinf.2020.05.048
6. Luo N, Zhang H, Zhou Y, Kong ZX, Sun WH, Huang N, et al. Utility of chest CT in diagnosis of COVID-19 pneumonia. Diagn Interv Radiol. 2020 Mai;26:437-42. DOI: https://doi.org/10.5152/dir.2020.20144
7. Li Z, Yi Y, Luo X, Xiong N, Liu Y, Li S, et al. Development and clinical application of a rapid IgM-IgG combined antibody test for SARS-CoV-2 infection diagnosis. J Med Virol. 2020 Fev;92(9):1518-24. DOI: https://doi.org/10.1002/jmv.25727
8. Van Elslande J, Houben E, Depypere M, Bracknier A, Desmet S, André E, et al. Diagnostic performance of 7 rapid IgG/IgM antibody tests and the Euroimmun IgA/IgG ELISA in COVID-19 patients. Clin Microbiol Infect. 2020 Ago;26(8):1082-7. DOI: https://doi.org/10.1016/j.cmi.2020.05.023
9. Maxim LD, Daniel Maxim L, Niebo R, Utell MJ. Screening tests: a review with examples. Inhal Toxicol. 2014 Set;26(13):811-28. DOI: https://doi.org/10.3109/08958378.2014.955932
10. The Aesthetic Society (AS). COVID-19 updates [Internet]. Garden Grove: AS; 2020; [acesso em 2020 Ago 01]. Disponível em: https://www.surgery.org/professionals/covid-19/covid-19-updates
11. Kaye K, Paprottka F, Escudero R, Casabona G, Montes J, Fakin R, et al. Elective, non-urgent procedures and aesthetic surgery in the wake of SARS-COVID-19: considerations regarding safety, feasibility and impact on clinical management. Aesthetic Plast Surg. 2020 Mai;44:1014-42. DOI: https://doi.org/10.1007/s00266-020-01752-9
12. Flexman AM, Abcejo AS, Avitsian R, Sloovere V, Highton D, Juul N, et al. Neuroanesthesia practice during the COVID-19 pandemic: recommendations from Society for Neuroscience in Anesthesiology and Critical Care (SNACC). J Neurosurg Anesthesiol. 2020 Jul;32(3):202-9. DOI: https://doi.org/10.1097/ANA.0000000000000691
13. Zeegen EN, Yates AJ, Jevsevar DS. After the COVID-19 pandemic: returning to normalcy or returning to a new normal?. J Arthroplasty. 2020 Jul;35(7 Supl 1):S37-S41. DOI: https://doi.org/10.1016/j.arth.2020.04.040
14. Liu Z, Zhang Y, Wang X, Zhang D, Diao D, Chandramohan K, et al. Recommendations for surgery during the novel coronavirus (COVID-19) epidemic. Indian J Surg. 2020 Abr;1-5.
15. Paraiso MFR, Brown J, Abrão MS, Dionisi H, Rosenfield RB, Lee TM, et al. Surgical and clinical reactivation for elective procedures during the COVID era: a global perspective. J Minim Invasive Gynecol. 2020 Jul;27(5):1188-95. DOI: https://doi.org/10.1016/j.jmig.2020.05.012
16. Carugno J, Di Spiezio Sardo A, Alonso L, Haimovich S, Campo R, De Angelis C, et al. COVID-19 Pandemic. Impact on hysteroscopic procedures: a consensus statement from the global congress of hysteroscopy scientific committee. J Minim Invasive Gynecol. 2020 Jul;27(5):988-92. DOI: https://doi.org/10.1016/j.jmig.2020.04.023
17. Meng Y, Leng K, Shan L, Guo M, Zhou J, Tian Q, et al. A clinical pathway for pre-operative screening of COVID-19 and its influence on clinical outcome in patients with traumatic fractures. Int Orthop. 2020 Ago;44(8):1549-55.
18. Ren X, Chen B, Hong Y, Liu W, Jiang Q, Yang J, et al. The challenges in colorectal cancer management during COVID- 19 epidemic. Ann Transl Med. 2020 Abr;8(7):498. DOI: https://doi.org/10.21037/atm.2020.03.158
19. Jacofsky D, Jacofsky EM, Jacofsky M. Understanding antibody testing for COVID-19. J Arthroplasty. 2020 Jul;35(7 Supl 1):S74-S81. DOI: https://doi.org/10.1016/j.arth.2020.04.055
20. Ragó Z, Szijjártó L, Duda E, Bella Z. Opportunity of periodic monitoring of COVID-19 patients, asymptomatic virus carriers, and postinfectious individuals with IgM/IgG rapid antibody tests among healthcare workers during SARS-CoV-2 pandemic. Orv Hetil. 2020 Mai;161(21):854-60.
21. Shen B, Zheng Y, Zhang X, Zhang W, Wang D, Jin J, et al. Clinical evaluation of a rapid colloidal gold immunochromatography assay for SARS-Cov-2 IgM/IgG. Am J Transl Res. 2020;12(4):1348-54.
22. Spicuzza L, Montineri A, Manuele R, Crimi C, Pistorio MP, Campisi R, et al. Reliability and usefulness of a rapid IgM-IgG anti- body test for the diagnosis of SARS-CoV-2 infection: a preliminary report. J Infect. 2020 Ago;81(2):53-4. DOI: https://doi.org/10.1016/j.jinf.2020.04.022
23. Cassaniti I, Novazzi F, Giardina F, et al. Performance of VivaDiag COVID-19 IgM/IgG Rapid Test is inadequate for diagnosis of COVID-19 in acute patients referring to emergency room department. J Med Virol. 2020 Mar;92(10):1724-7. DOI: https://doi.org/10.1002/jmv.25800
24. Padoan A, Cosma C, Sciacovelli L, Faggian D, Plebani M. Analytical performances of a chemiluminescence immunoassay for SARS-CoV-2 IgM/IgG and antibody kinetics. Clin Chem Lab Med. 2020;58(7):1081-8. DOI: https://doi.org/10.1515/cclm-2020-0443
25. Rosa MI, Prestes GS, Macedo ACL, Colonetti T, Uggioni MLR, Grande AJ. Accuracy of rapid IgM and IgG antibody test for SARS-CoV-2 infection diagnosis: a systematic review and meta analysis. Braz J Infect Dis. 2020. DOI: https://doi.org/10.37766/inplasy2020.4.0099
26. Pulia MS, O'Brien TP, Hou PC, Schuman A, Sambursky R. Multi-tiered screening and diagnosis strategy for COVID-19: a model for sustainable testing capacity in response to pandemic. Ann Med. 2020 Ago;52(5):207-14.
27. Castro R, Luz PM, Wakimoto MD, Veloso VG, Grinsztejn B, Perazzo H. COVID-19: a meta- analysis of diagnostic test accuracy of commercial assays registered in Brazil. Braz J Infect Dis. 2020 Mar/Abr;24(2):180-7.
28. Saenz-Flor KV, Santafe LM. Concordance of "rapid" serological tests and IgG and IgM chemiluminescence for SARS-COV-2. medRxiv [Internet]. 2020 Jun 03; [Epub preprint]. DOI: https://doi.org/10.1101/2020.06.01.20114884
29. Prazuck T, Colin M, Giachè S, Gubavu C, Seve A, Rzpecki V, et al. Evaluation of performance of two SARS-CoV-2 rapid whole-blood finger-stick IgM-IgG combined antibody tests. medRxiv [Internet]. 2020 May 27; [Epub preprint]. DOI: https://doi.org/10.1101/2020.05.27.20112888
30. Di Lorenzo G, Toniolo P, Lurani C, Foresti L, Carrisi C. Evaluating the adequacy of Prima Covid-19 IgG/IgM Rapid Test for the assessment of exposure to SARS-CoV-2 virus. medRxiv [Internet]. 2020 Jun 03; [Epub preprint]. DOI: https://doi.org/10.1101/2020.05.30.20117424
31. Ying, Yue-Ping L, Bo D, Fei-Fei R, Yue W, Jinya D, et al. Diagnostic indexes of a rapid IgG/IgM combined antibody test for SARS-CoV-2. medRxiv [Internet]. 2020 Mar 30; [Epub preprint]. DOI: https://doi.org/10.1101/2020.03.26.20044883
32. Hoffman T, Nissen K, Krambrich J, Rönnberg B, Akaberi D, Esmaeilzadeh M, et al. Evaluation of a COVID-19 IgM and IgG rapid test; an efficient tool for assessment of past exposure to SARS-CoV-2. Infect Ecol Epidemiol. 2020 Abr;10(1):1754538. DOI: https://doi.org/10.1080/20008686.2020.1754538
33. Pérez-García F, Pérez-Tanoira R, Romanyk J, Arroyo T, Gómez-Hurruz P, Cuadros-González J. Rapid diagnosis of SARS-CoV-2 infection by detecting IgG and IgM antibodies with an immunochromatographic device: a prospective single-center study. medRxiv [Internet]. 2020 Abr 24; [Epub preprint]. DOI: https://doi.org/10.1101/2020.04.11.20062158
34. Minteer C, Casanovas-Massana A, Li T, McDonald D, Wang L, Pan SH, et al. Multi-site validation of a SARS-CoV-2 IgG/IgM rapid antibody detection kit. medRxiv [Internet]. 2020 Mai 26; [Epub preprint]. DOI: https://doi.org/10.1101/2020.05.25.20112227
35. Yangchun F. Optimize clinical laboratory diagnosis of COVID-19 from suspect cases by likelihood ratio of SARS-CoV-2 IgM and IgG antibody. medRxiv [Internet]. 2020 Abr 08; [Epub preprint]. DOI: https://doi.org/10.1101/2020.04.07.20053660
36. Kohmer N, Westhaus S, Rühl C, Ciesek S, Rabenau HF. Clinical performance of SARS-CoV-2 IgG antibody tests and potential protective immunity. medRxiv [Internet]. 2020 Mai 10; [Epub preprint]. DOI: https://doi.org/10.1101/2020.05.08.085506
37. Qu J, Wu C, Li X, Zhang G, Jiang Z, Li X, et al. Profile of immunoglobulin G and IgM antibodies against severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2). Clin Infect Dis. 2020 Out;71(16):2255-8. DOI: https://doi.org/10.1093/cid/ciaa489
38. Capello F, Cipolla M, Cosco L, Gnasso A, Mancini R, Nichelatti M, et al. The VivaDiag COVID-19 lgM/IgG rapid test for the screening and early diagnosis of COVID-19 in patients with no clinical signs of the disease. Int J Endocr Metab Dis. 2020;6(1):1-4. DOI: https://doi.org/10.16966/2380-548x.167
39. Xie J, Ding C, Li J, Wang Y, Guo H, Lu Z, et al. Characteristics of patients with coronavirus disease (COVID-19) confirmed using an IgM-IgG antibody test. J Med Virol. 2020 Abr;92(10:2004-10. DOI: https://doi.org/10.1002/jmv.25930
40. Ma H, Zeng W, He H, Zhao D, Jiang D, Zhou P, et al. Serum IgA, IgM, and IgG responses in COVID-19. Cell Molec Immunol. 2020 Mai;17:773-5. DOI: https://doi.org/10.1038/s41423-020-0474-z
1. Pontificia Universidade Católica do Rio Grande
do Sul, Programa de Pós-Graduação em Medicina e Ciências da Saúde, Porto Alegre,
RS, Brasil.
2 . Sistema de Saúde Mãe de Deus, Hospital Mãe de
Deus Carlos Gomes, Porto Alegre, RS, Brasil.
RKZ Análise e/ou interpretação dos dados, Análise estatística, Aprovação final do manuscrito, Aquisição de financiamento, Coleta de Dados, Conceitualização, Concepção e desenho do estudo, Gerenciamento do Projeto, Investigação, Metodologia, Realização das operações e/ ou experimentos, Redação - Preparação do original
SSV Análise e/ou interpretação dos dados, Análise estatística, Aprovação final do manuscrito, Coleta de Dados, Conceitualização, Concepção e desenho do estudo, Gerenciamento do Projeto, Investigação, Metodologia, Realização das operações e/ou experimentos, Redação - Preparação do original, Visualização
DSV Análise e/ou interpretação dos dados, Análise estatística, Aprovação final do manuscrito, Coleta de Dados, Conceitualização, Concepção e desenho do estudo, Investigação, Metodologia, Realização das operações e/ou experimentos, Redação - Preparação do original, Redação - Revisão e Edição, Supervisão, Visualização
Autor correspondente: Denis Souto Valente Rua Antônio Carlos Berta, 475/702, Jardim Europa, Porto Alegre, RS, Brasil. CEP: 91340-020 E-mail: denisvalentedr@gmail.com
Artigo submetido: 05/07/2020.
Artigo aceito: 10/01/2021.
Conflitos de interesse: não há.




 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter