

Review Article - Year 2006 - Volume 21 -
Antibiotic use in Plastic Surgery
Uso de Antibióticos em Cirurgia Plástica
ABSTRACT
In the last decades, some research had established norms for the correct antibiotic use in the prophylaxis of surgical infection. However, in Plastic Surgery few are the papers published with adjusted scientific methodology. Based on evidences in literature, we praise the world-wide trend of the rational antibiotic use and present the recommendations of Plastic Surgery Division of the Federal University of Rio de Janeiro.
Keywords: Antibiotic prophylaxis, utilization. Antibiotic prophylaxis, methods. Antibiotic prophylaxis, contraindications
RESUMO
Nas últimas décadas, várias pesquisas estabeleceram normas para o correto uso de antibióticos na profilaxia de infecção cirúrgica. Contudo, em Cirurgia Plástica poucos são os trabalhos publicados com metodologia científica adequada quanto ao uso de antibióticos. Sem dúvida, a maioria das cirurgias plásticas pertence ao grupo das cirurgias limpas ou das potencialmente contaminadas. Baseando-se em evidências obtidas de dados publicados na literatura sobre os cuidados pré-operatórios e a antibioticoprofilaxia em diversos tipos de cirurgia, também preconizamos a tendência mundial do uso racional de antibióticos e apresentamos as recomendações do Serviço de Cirurgia Plástica do Hospital Universitário Clementino Fraga Filho da Universidade Federal do Rio de Janeiro (HUCFF - UFRJ).
Palavras-chave: Antibioticoprofilaxia, utilização. Antibioticoprofilaxia, métodos. Antibioticoprofilaxia, contra-indicações
De acordo com a classificação geral das feridas, a maioria das cirurgias plásticas, incluindo aquelas com implante de próteses, pertence ao grupo das cirurgias limpas ou das potencialmente contaminadas e as recomendações para a antibioticoprofilaxia devem estar baseadas nos estudos realizados para esse grupo de cirurgia1, 2.
O risco de infecção cirúrgica é determinado pela relação entre a carga microbiana de contaminação, sua virulência, o grau de injúria aos tecidos da ferida contra a capacidade de resistência do hospedeiro, influenciada pela resposta imune local e sistêmica. Além destes fatores, a presença de corpo estranho na ferida pode comprometer a defesa local dos tecidos, diminuindo o inóculo necessário para o desenvolvimento da infecção e permitindo que microrganismos pouco virulentos, como as micobactérias e estafilococo coagulase negativa, causem infecção.
As características do paciente que podem influenciar negativamente incluem: extremos de idade, diabetes mellitus descompensada, tabagismo, uso de esteróides, desnutrição, obesidade e hospitalização prolongada. Fatores como hiperglicemia, fumo e excesso de peso devem ser corrigidos no pré-operatório.
Em relação ao ato cirúrgico, diversos cuidados têm importância na prevenção da infecção cirúrgica; entre eles, destacamos: anti-sepsia e assepsia adequadas, habilidade do cirurgião, menor tempo operatório, manipulação atraumática dos tecidos e erradicação de espaços mortos, hematomas ou coleções.
Por meio de análise da literatura, preconizamos o uso racional de antibióticos e expomos as recomendações do Serviço de Cirurgia Plástica do HUCFF - UFRJ.
DADOS DA LITERATURA EM CIRURGIA PLÁSTICA
Poucos são os artigos publicados sobre o uso de antibióticos em Cirurgia Plástica3-6. Na literatura médica, em geral, indica-se a antibioticoprofilaxia em cirurgias com complicações infecciosas freqüentes - cirurgias de cólon - cirurgias com complicações infecciosas graves, como em prótese cardiovascular, e naquelas com evidência comprovada cientificamente.
Fática et al.3, após análise de 133 pacientes, concluíram que antibioticoprofilaxia com cefazolina, em cirurgias com duração superior a três horas, pode ser eficaz na redução de infecção cirúrgica por Staphylococcus aureus. Perroti6 comentou o artigo de Fática, ressaltando a existência de comprovações científicas de que a manutenção de antibióticos por período além do profilático não traz benefícios.
Nahabedian et al.7, analisando 168 implantes de silicone realizados para reconstrução mamária, referiram que a possibilidade de infecção foi 4,88 vezes maior quando as pacientes eram submetidas à radioterapia. Relataram, também, evidências de que, havendo esvaziamento linfonodal axilar, o risco de infecção poderia crescer em 6,29 vezes.
Knackmuhs8 relatou quatro casos de pacientes submetidas à ritidectomia que apresentaram infecção por Mycobacterium chelonae, tendo sido identificado como fonte da infecção a contaminação do frasco multidose de azul de metileno utilizado para marcação da pele, sendo o surto controlado com ampolas de uso único.
Perroti6 analisou o uso de antibiótico profilático em 10 tipos de cirurgias plásticas, realizadas por 1767 cirurgiões, nos EUA. Observou ausência de homogeneidade nas indicações, tempo de uso e vias de administração. Houve relatos de uso de antibióticos administrados por via oral no per-operatório e aplicação de antibióticos por irrigação, em mamaplastias, por 21% dos cirurgiões. Na literatura, é muito limitado o número de estudos sobre uso tópico de antibióticos como profilaxia de infecção cirúrgica9. Em situações clínicas específicas, como no tratamento de impetigo, antibiótico tópico mostra eficácia quando utilizado regularmente por vários dias. Entretanto, seu uso para irrigar a ferida durante a cirurgia é conceitualmente errado, pois desse modo estaria sendo usado como um antiséptico. Além disso, a profilaxia antibiótica por via sistêmica tem ação excelente no sítio cirúrgico, não necessitando complementação local.
Outros poucos autores podem ser encontrados apresentando diferentes impressões quanto ao uso de antibióticos em Cirurgia Plástica4,5,10.
RECOMENDAÇÕES PARA A PREVENÇÃO DE INFECÇÃO DE FERIDA CIRÚRGICA
Preparo do paciente
Em 1999, o Centro Norte-Americano para Controle e Prevenção de Doenças - CDC - por meio do estudo de Mangram et al.11, utilizou categorias, baseadas em evidências científicas, teoria racional e aplicabilidade, para serem incluídas nas recomendações de prevenção da infecção cirúrgica. As categorias IA e IB trazem recomendações que são consideradas efetivas, sendo: IA fortemente recomendada e baseada em estudos bem desenhados; e IB, fortemente recomendada baseada em alguns estudos e com forte base teórica. As recomendações da categoria II são baseadas em estudos sugestivos de benefício e possuem menor força que as recomendações das categorias IA e IB.
A partir deste estudo, podemos ressaltar pontos relevantes no preparo do paciente:
Preparo da pele
1. O banho pré-operatório com solução anti-séptica como a clorexidina degermante reduz a flora residente da pele, o que, teoricamente, reduziria o risco de infecção.
2. A remoção de pêlos, considerando-se quanto ao risco de infecção, não se faz necessária. Quando necessária por outro motivo, deve-se fazer tricotomia imediatamente antes da cirurgia e não raspagem com lâminas. O uso de lâminas provoca pequenas lesões na pele que podem tornar-se colonizadas por outra microbiota mais patogênica, particularmente se o procedimento foi feito na véspera, dificultando a desinfecção da pele do paciente e constituindo um microambiente desfavorável para a ferida cirúrgica.
3. Para anti-sepsia da pele do paciente, preferencialmente utilizamos solução de clorexidina degermante 2% ou 4%, seguida de clorexidina alcoólica a 0,5%. A clorexidina apresenta boa ação residual, não é inativada pela presença de sangue e não tinge a pele, o que possibilita melhor controle da viabilidade dos tecidos. Quando não dispomos de clorexidina, utilizamos iodo-povidine (PVP-I) degermante, seguido de solução alcoólica de PVP-I, sabendo que esses não têm ação residual tão boa, são inativados por sangue ou pus e colorem a pele. Deve-se evitar a associação de clorexidina com iodo-povidine durante o preparo da pele11.
Preparo da equipe
1. Os profissionais que entrarão em contato com o paciente durante o procedimento cirúrgico devem lavar as mãos, unhas e antebraços; proceder à desinfecção, com o uso de escovas com cerdas macias, até os cotovelos, utilizando clorexidina ou iodo-povidine degermante por 2 a 5 minutos.
2. A paramentação adequada para toda equipe na sala de cirurgias inclui gorro, máscara e capote cirúrgico. Não existem evidências que o uso de sapatilhas sobre os sapatos seja necessário para reduzir a infecção cirúrgica12. O uso de sapatilhas impermeáveis está indicado para proteger os sapatos do profissional de saúde contra a exposição à matéria orgânica. O uso de calçados impermeáveis exclusivos para o centro cirúrgico também está correto.
Caso seja preciso sair do centro cirúrgico usando-se o vestuário destinado para tal ambiente, se estiver visivelmente limpo, não é necessária a sua retirada13. Recomenda-se vestir sobre este um jaleco abotoado.
PROFILAXIA ANTIBIÓTICA
A pele íntegra constitui-se na principal barreira contra infecções. Terminada a cirurgia, a síntese adequada dos tecidos e a resposta inflamatória ao trauma restabelecem a barreira orgânica contra infecções, não havendo, na maioria dos casos, indicação de manutenção do uso de antibióticos.
Estudos bem corroborados mostraram que a eficácia da antibioticoprofilaxia é perdida se a administração da droga for feita muito antes da cirurgia e reduzida após o seu início2,14. Para máxima eficácia profilática, é fundamental que o antibiótico seja feito na indução anestésica, em dose elevada e por via parenteral, para assegurar níveis terapêuticos de antibiótico nos tecidos manipulados e no exsudato da ferida, enquanto durar o ato cirúrgico.
A indicação para antibioticoprofilaxia se enquadra nas cirurgias plásticas que tenham duração superior a três horas e quando há enxertos ou implante de próteses15.
O antibiótico deve ser administrado 30 minutos antes da incisão e, conforme a meia vida do antibiótico, repetido no intra-operatório nas cirurgias longas. Nas cirurgias limpas, as cefalosporinas de 1a geração, particularmente a cefazolina devido sua maior meia vida, têm excelente indicação, pois cobrem o principal causador de infecção, o S. aureus. Além disso, apresentam ação bactericida, baixa toxicidade e excelente penetração tecidual. Em cirurgias com duração de 4h ou mais, a cefazolina deve ser repetida a cada 4h. Portanto, na maior parte das cirurgias está indicado o uso de 1 a 2 doses de cefazolina. As exceções são as cirurgias com inserção de prótese ou enxerto, nas quais a cefazolina é utilizada 1g a cada 8h, nas 24h a 48h seguintes ao procedimento. Em cirurgias potencialmente contaminadas, indicamos a associação de amoxicilina/clavulanato de potássio (Clavulin®) (Quadro 1).
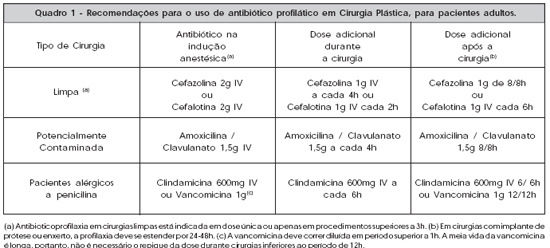
Pacientes alérgicos à penicilina podem apresentar reação cruzada às cefalosporinas, numa incidência de 1% a 10%. Nestes casos, indicamos clindamicina 600 mg IV, a cada 6h, quando indicada, por 24h. Outra opção é a vancomicina em dose única de 1g, o que proporciona cobertura por 12 horas, a qual deve ser administrada diluída e lentamente.
TERAPIA ANTIBIÓTICA
Quando utilizado por períodos superiores ao que foi descrito, o antibiótico deixa de ser profilático e passa a ser terapêutico. Sendo o S. aureus o principal agente causador, está indicado o uso de uma cefalosporina, por via intravenosa, a cefazolina - 1 a 2g a cada 8h - ou a cefalotina - 1 a 2g a cada 4 a 6h. Infecções cirúrgicas de pequena gravidade podem ser tratadas por via oral com uma cefalosporina, como a cefalexina - 500 a 750 mg a cada 6h - ou o cefadroxil - 0,5 a 1 grama de 12/12h. Como no tratamento de outras infecções cutâneas e partes moles sem complicação, a duração do tratamento deve ser de 7 a 14 dias, no máximo.
Nas cirurgias contaminadas ou no paciente com risco de microbiota selecionada hospitalar, é necessário conhecer o perfil da microbiota causadora de infecção da Instituição e do setor. É aconselhável consultar a Comissão de Controle de Infecção Hospitalar para se tratar de forma adequada o paciente.
CONSIDERAÇÕES GERAIS E SITUAÇÕES ESPECIAIS
Alguns aspectos locais são relevantes para a boa evolução do sítio cirúrgico e quanto ao risco de infecção. Por exemplo, áreas bem vascularizadas, como a face, infectam menos do que regiões com reduzido aporte sangüíneo. Sendo assim, é evidente que a presença de tecidos isquêmicos, necrosados, com crostas e bolhas, aumenta o risco de infecção e deve ser avaliadas, precocemente quanto à indicação de desbridamento.
Feridas abertas e com tecido de granulação em formação apresentam colonização semelhante à pele normal - microbiota residente - podendo ser lavadas durante o banho, o que facilita a limpeza e acelera a cicatrização.
O dreno cirúrgico, quando utilizado, deve ser de sistema fechado e mantido pelo mínimo de tempo possível. Não há recomendações na literatura para se prolongar o uso do antibiótico ou mantê-lo durante a persistência do dreno.
Se a infecção cirúrgica surgir em vigência ou logo após a antibioticoprofilaxia, é necessário considerar que o patógeno causador seja resistente ao antibiótico usado. Está indicada a coleta de material para a coloração pelo Gram e para cultura. No caso de uso de cotonete estéril, coletar de preferência duas amostras, uma para cada exame. A coleta ideal do material para o exame bacteriológico, evitando-se a contaminação da superfície da lesão, é através da punção com aspiração da ferida. Mesmo na ausência de coleção, o material sero-sangüíneo obtido pela punção deve ser enviado para a cultura, sendo, entretanto, menor a positividade do Gram. Na coleta por cotonete, a ferida deve ser aberta para se obter o material. Entretanto, se a ferida já estiver aberta, há grande possibilidade de contaminação por outras bactérias não responsáveis pela infecção. Para se evitar a contaminação durante a coleta, deve-se coletar o material de um plano profundo, após o local ser limpo com soro fisiológico, e ao redor da lesão com solução anti-séptica degermante como o PVP-I. O cotonete deve ter um meio de transporte (gel) para não ressecar, na indisponibilidade desse meio de transporte, umidificá-lo com soro fisiológico antes da coleta.
Quando há infecção evidente, utilizamos os mesmos cuidados universais indicados em outras especialidades cirúrgicas: abrir, drenar e lavar a ferida. Infecção localizada, sem repercussão sistêmica e sem gravidade após drenagem e limpeza da ferida evoluem bem. Não há evidências da necessidade do uso de antibióticos nessas situações. A drenagem da secreção, a limpeza do sítio infectado e o acompanhamento criterioso são medidas mais importantes que a administração de antibióticos.
Pacientes vítimas de queimaduras e em tratamento em Centros de Queimados apresentam peculiaridades relativas a este tipo de injúria. Devem ser acompanhados por uma Comissão de Controle de Infecção Hospitalar para indicar e adequar o uso de antibióticos.
Por fim, observamos que, especialmente em Cirurgia Plástica, há tendência ao uso excessivo de antibióticos, tanto para profilaxia quanto para terapêutica. Particularmente em cirurgias estéticas, o risco da infecção cirúrgica, temido como uma catástrofe, é superestimado. Devemos aplicar as recomendações da medicina baseada em evidências científicas, preservando, em primeiro lugar, a saúde do paciente, e considerando que o uso indiscriminado de antibióticos pode selecionar bactérias resistentes.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Gonçalves LF, Franco D. Curativos. In: Franco T, Franco D, Gonçalves LF, eds. Princípios de cirurgia plástica. São Paulo;Atheneu;2002, p.159-71.
2. Andenaes K, Lingaas E, Amland PF, Giercksky KE, Abyholm F. Preoperative bacterial colonization and its influence on postoperative wound infections in plastic surgery. J Hosp Infect. 1996;34(4):291-9.
3. Fatica CA, Gordon SM, Zins JE. The role of preoperative antibiotic prophylaxis in cosmetic surgery. Plast Reconstr Surg. 2002;109(7):2570-3.
4. Lineaweaver W, Hui K, Yim K, Ruyle M, Shuster B, Eggleston J et al. The role of the plastic surgeon in the management of surgical infection. Plast Reconstr Surg. 1999;103(6):1553-60.
5. Peled IJ, Dvir G, Berger J, Ramon I, Ullmann Y, Nachlieli T. Prophylactic antibiotics in aesthetic and reconstructive surgery. Aesthetic Plast Surg. 2000;24(4):299-302.
6. Perrotti J. The role of preoperative antibiotic prophylaxis in cosmetic surgery by Fatica C, Gordon SM, Zins JE. Plast Reconstr Surg. 2002;109(7):2574-5.
7. Nahabedian MY, Tsangaris T, Momen B, Manson PN. Infectious complications following breast reconstruction with expanders and implants. Plast Reconstr Surg. 2003;112(2):467-76.
8. Knackmuhs G. Centers for Disease Control and Prevention (CDC). Mycobacterium chelonae infections associated with face lifts -New Jersey, 2002-2003. MMWR Morb Mortal Wkly Rep.. 2004;53(9):192-4.
9. Adams WP Jr, Rios JL, Smith SJ. Enhancing patient outcomes in aesthetic and reconstructive breast surgery using triple antibiotic breast irrigation: six-year prospective clinical study. Plast Reconstr Surg. 2006;117(1):30-6.
10. Baran CN, Sensoz Ö, Ulusoy MG. Prophylactic antibiotics in plastic and reconstructive surgery. Plast Reconstr Surg. 1999;103(6):1561-6.
11. Mangram AJ, Horan TC, Pearson ML, Silver LC, Jarvis WR. Guideline for prevention of surgical site infection, 1999. Hospital Infection Control Practices Advisory Committee. Infect Control Hosp Epidemiol. 1999;20(4):250-80.
12. Humphreys H, Marshall RJ, Ricketts VE, Russel AJ, Reeves DS. Theatre over-shoes do not reduce operating theatre floor bacterial counts. J Hosp Infect. 1991;17(2):117-23.
13. Kaplan C, Mendiola R, Ndjatou V, Chapnick E, Minkoff H. The role of covering gowns in reducing rates of bacterial contamination of scrub suits. Am J Obstet Gynecol. 2003;188(5):1154-5.
14. Burke JF. The effective period of preventive antibiotic action in experimental incisions and dermal lesions. Surgery. 1961;50:161-8.
15. Marangoni DV. Profilaxia antibiótica. In: Scheter M, Marangoni DV, eds. Doenças infecciosas: conduta diagnóstica e terapêutica. Rio de Janeiro:Guanabara Koogan;1994. p.40-4.
I. Membro Titular da SBCP; Mestre em Cirurgia Plástica pela Universidade Federal do Rio de Janeiro (UFRJ); Doutor em Cirurgia Plástica pela UFRJ; Professor Adjunto de Cirurgia Plástica do Hospital Universitário Clementino Fraga Filho (HUCFF).
II. Membro da Coordenação de Controle de Infecção Hospitalar do HUCFF- UFRJ. Diploma em Medicina Tropical pela Universidade de Liverpool, Mestre em Imunologia das Doenças Infecciosas pela Universidade de Londres; Doutor em Doenças Infecto-Parasitárias pela UFRJ.
III. Membro Titular da SBCP; Professora Titular da UFRJ; Membro da Academia Nacional de Medicina; Chefe do Serviço de Cirurgia Plástica do HUCFF.
Correspondência para:
Diogo Franco
Praia de Botafogo, 528 apto 1304 - A - Botafogo
Rio de Janeiro, RJ - CEP 22250-040
E.mail: diogo@openlink.com.br
Trabalho realizado no Serviço de Cirurgia Plástica do Hospital Universitário Clementino Fraga Filho da Universidade Federal do Rio de Janeiro (HUCFF - UFRJ), Rio de Janeiro, RJ.
Artigo recebido: 27/01/2006
Artigo aprovado: 19/05/2006


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter