

Original Article - Year 2005 - Volume 20 -
Venous occlusion after limb replantation: a new experimental model in rats
Oclusão Venosa Em Reimplante de Membro: Um Novo Modelo Experimental Em Ratos - Prêmio Sirlei Rinaldi 2002
ABSTRACT
Background: Venous occlusion may have pronounced circulatory effects leading to decreased viability of flaps and limb replantations. It was tested a new venous occlusion model in rats. Method: Amputation with preservation of vessels and nerves of the right hind limb was proceeded in 100 rats. The model groups were submitted to 0, 1, 2, 3 and 4 hours of venous occlusion. The limbs were observed for 7 days and the survival limb rates. Results: Trans-operatory mortality rates in model groups were 0, 10, 15, 30 e 60% respectively and the post-operatory mortality rates were 5; 11,1; 11,7; 14,2 e 100% respectively. The survival limb rates were 100%, 87,5%, 80% e 66,67% respectively. Model groups were statistically different except for G2 and G3 in transoperatory mortality rates. There were no statistical difference between model groups except for G4 and G5. Model groups groups were statistically different except for G2 and G3 in survival limb rates. Conclusions: The model tested showed time-response curves in trans-operatory mortality and viability limb rates.
Keywords: Ischemia, physiopathology. Graft survival. Veins
RESUMO
Introdução: A oclusão venosa pode levar a efeitos na microcirculação com comprometimento da viabilidade de retalhos e membros reimplantados. Foi testado um novo modelo experimental de oclusão venosa após reimplante de membro. Método: Amputações com preservação dos vasos e nervos do membro posterior direito foram realizadas em 100 ratos. Os grupos experimentais foram submetidos a tempos de oclusão venosa de 0, 1, 2, 3 e 4 horas. Os resultados foram analisados estatisticamente pelo teste do Qui-quadrado (p < 0,05). Resultados: As taxas de mortalidade transoperatórias dos grupos modelos foram 0, 10, 15, 30 e 60%, respectivamente. As taxas de mortalidade pós-operatórias foram 5; 11,1; 11,7; 14,2 e 100%, respectivamente. As taxas de viabilidade dos membros isquêmicos após 7 dias de avaliação foram 100%, 87,5%, 80% e 66,67%. As taxas de mortalidade transoperatórias foram diferentes estatisticamente com exceção de G2 e G3. As taxas de mortalidade pós-operatórias não foram diferentes com exceção de G4 e G5. As taxas de viabilidade dos grupos G1, G2, G3, G4 e G5 foram diferentes entre si, exceto os grupos G2 e G3. Conclusão: Observa-se uma curva tempo-resposta na mortalidade transoperatória e viabilidade dos membros no modelo testado.
Palavras-chave: Isquemia, fisiopatologia. Sobrevivência do enxerto. Veias
A oclusão arterial ou venosa no período pós-operatório pode ocorrer em retalhos microcirúrgicos e reimplantes1. Trabalhos relatam que a oclusão venosa pós-operatória é mais deletéria que a oclusão global ou arterial. Pequenos períodos de oclusão venosa podem levar a efeitos pronunciados e de longa duração na microcirculação, levando ao comprometimento da viabilidade de retalhos e membros2-4. Su et al.5, em 1982, estudaram retalhos de pele em ratos e observaram uma menor viabilidade dos retalhos após a oclusão venosa do que após a oclusão arterial. Hedén et al.4 utilizaram o laser doppler para avaliar o fluxo sangüíneo em retalhos de pele em porcos e observaram que a redução do fluxo é maior após a oclusão venosa do que após a oclusão arterial e este efeito poderia ser secundário ao edema tecidual, agregação plaquetária ou microtromboses.
O músculo esquelético é mais sensível à oclusão venosa do que a pele. Harashima et al.6 observaram 100% de necrose em retalhos de pele em ratos após 8 horas de oclusão venosa. Gabriel et al.2, em 2001, observaram que lesões teciduais irreversíveis ocorrem após breves períodos de oclusão venosa no retalho do músculo grácil em ratos. Alterações na microcirculação, utilização do oxigênio, metabolismo energético e lesão de isquemia e reperfusão são possíveis mecanismos de lesão propostos para a oclusão venosa total.
Diversos modelos experimentais de retalho cutâneo e musculares foram desenvolvidos em ratos e porcos para o estudo da fisiopatologia da oclusão venosa. Poucos trabalhos estudaram os efeitos da oclusão venosa em tecidos compostos e membros. Nakamura et al.7 estudaram os efeitos da oclusão venosa em um modelo de reimplante de membro em coelhos. Um modelo experimental em ratos para estudo da oclusão venosa em reimplante de membro ainda não foi descrito. O presente trabalho pretende testar um novo modelo de oclusão venosa após reimplante de membro em ratos.
MÉTODO
O projeto desta pesquisa (Nº 298/02) foi aprovado pela Comissão de Ética para Análise de Projetos de Pesquisa da Faculdade de Medicina da USP (CAPPesq). Foram utilizados 100 ratos Wistar machos, pesando entre 290 e 310g, ração e água ad libitum e período claro/escuro de 12/12 horas.
Os animais foram anestesiados com tiopental sódico (50mg/kg) intraperitonial. Procedeu-se à incisão circular na porção média da coxa, abrangendo pele, tecido celular subcutâneo e musculatura após hemostasia com eletrocautério bipolar8,9. A osteotomia do fêmur no terço médio foi realizada com serra manual (Figura 1). Procedeu-se à síntese óssea com fixação intramedular do fêmur com segmento de agulha 30X7 e cola de éster de cianoacrilato, síntese da musculatura e aplicou-se o clipe microvascular atraumático na veia femoral, antes da emergência dos vasos epigástricos superficiais caudais, evitando-se incluir o nervo e artéria femorais (Figura 2). Observou-se a interrupção do fluxo sangüíneo da veia femoral através do teste de enchimento negativo e realizou-se a síntese da pele e reposição volêmica através da injeção subcutânea de 50ml/kg de solução fisiológica de NaCl a 0,9%.
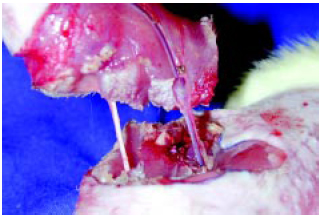
Figura 1 - Amputação do membro posterior direito com preservação de vasos e nervos.
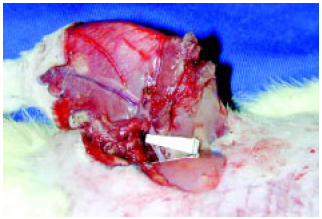
Figura 2 - Reimplante com posicionamento do clipe vascular em veia femoral direita.
Os animais foram submetidos a tempos de oclusão venosa quente (25ºC) a partir do pinçamento da veia (Figura 3). Realizou-se Incisão vertical em região inguinal esquerda com dissecção, canulação da veia epigástrica superficial caudal com agulha 29G e injeção de 1ml de solução salina (Figura 4). A sutura vertical da pele do membro posterior direito foi aberta e retirado o clipe vascular. Foi observada a permeabilidade da veia femoral através do teste de enchimento positivo e ausência de trombos ao exame com o microscópio cirúrgico e procedeu-se à síntese da pele.
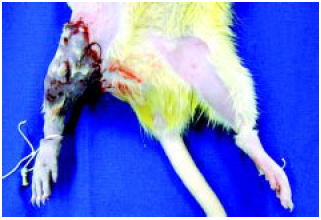
Figura 3 - Membro congesto após clipagem da veia femoral direita.
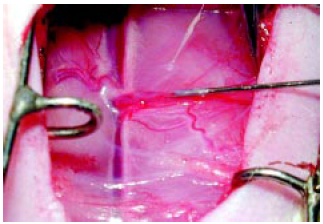
Figura 4 - Canulação da veia epigástrica caudal esquerda com injeção de solução salina.
Os animais foram divididos em 5 grupos experimentais (Tabela 1).
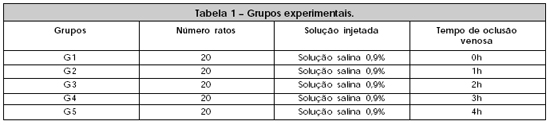
Os animais foram observados diariamente por um período de sete dias. Os óbitos observados foram divididos de acordo com o período em que ocorreram: período transoperatório (óbitos ocorridos durante o procedimento cirúrgico desde o início da anestesia até a liberação do clipe vascular) e período pós-operatório (óbitos ocorridos desde a liberação do clipe vascular até o 7º dia de pós-operatório). A viabilidade dos membros foi determinada através de exame clínico e os membros foram classificados em membros viáveis ou membros não viáveis (Figuras 5 a 7). Os animais foram sacrificados após sete dias através de superdose de éter inalatório.
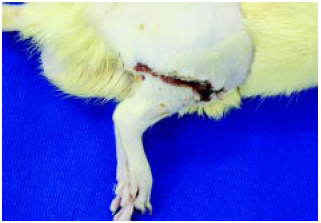
Figura 5 - Membro viável após 7 dias: viabilidade total.
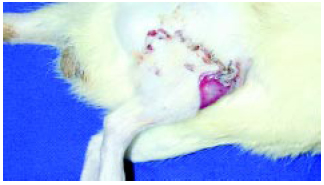
Figura 6 - Membro viável após 7 dias: viabilidade total da musculatura com pequena área de necrose de pele atribuídas ao desenluvamento distal da pele.
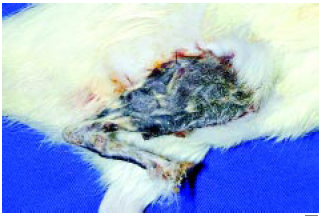
Figura 7 - Membro inviável: necrose total do membro.
Os resultados foram transformados em taxas (porcentagens) de mortalidade e viabilidade do membro por grupo. Os grupos foram comparados entre si e analisados estatisticamente pelo teste do Qui-quadrado. O nível de significância adotado foi de 5% (p< 0,05).
RESULTADOS
Quarenta e sete ratos foram a óbito durante o estudo, 27 durante o período transoperatório e 20 até o sétimo dia de pósoperatório, levando a uma mortalidade total de 33,8%.
As mortalidades pós-operatórias e transoperatórias dos grupos experimentais estão representadas na Tabela 2 e Figuras 8 e 9. As diferenças entre as taxas de mortalidade no período pós-operatório dos grupos G1 e G2, G2 e G3, G3 e G4 não foram significantes estatisticamente. G4 e G5 evoluíram com taxas de mortalidade pós-operatórias diferentes estatisticamente (p< 0,001) - Tabela 2 e Figura 8.
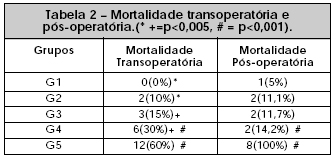
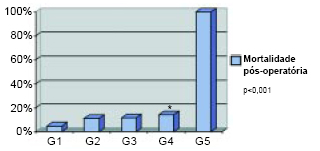
Figura 8 - Mortalidade pós-operatória.
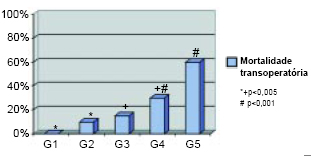
Figura 9 - Mortalidade transoperatória.
As taxas de mortalidade, no período transoperatório, foram diferentes significativamente entre os grupos G1 e G2 (p< 0,005), G3 e G4 (p< 0,005) e G4 e G5 (p< 0,001). As taxas de mortalidade, no período transoperatório, dos grupos G2 e G3 não foram diferentes estatisticamente (p< 0,5) - Tabela 2 e Figura 9.
A viabilidade do membro encontrada foi do tipo tudo ou nada e estão representadas na Tabela 3 e Figura 10. Os grupos G1 e G2 (p< 0,001), G3 e G4 (p< 0,05) foram diferentes estatisticamente. Os grupos G2 e G3 não foram diferentes estatisticamente (p< 0,5%) - Tabela 3 e Figura 10.
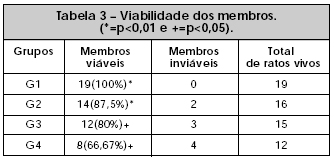
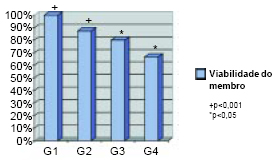
Figura 10 - Viabilidade dos membros.
DISCUSSÃO
Vários modelos de retalhos têm sido propostos para o estudo da lesão tecidual por oclusão venosa. Harashina et al.6, em 1977, foram os primeiros a desenvolverem um modelo de oclusão venosa em retalhos de pele em ratos. Daniel et al.10, em 1982, desenvolveram um modelo de oclusão venosa em retalhos cutâneos de porcos. Ao final da década de 80, o interesse pelo estudo da congestão, em particular seus efeitos sobre o músculo, foi ampliado e foram desenvolvidos novos modelos de retalhos miocutâneos2,11-13. No final da década de 90, surgiu o interesse pelos efeitos da oclusão venosa em retalhos compostos e membros. Nakamura et al.7, em 1998, desenvolveram um modelo de reimplante de membro posterior de coelhos com preservação de vasos para o estudo do superóxido, após a clipagem da veia femoral. Um modelo de oclusão venosa em reimplante de membro em ratos ainda não foi testado.
O presente trabalho desenvolveu um modelo de amputação parcial mantendo o pedículo vascular e nervoso do membro semelhante aos modelos utilizados por Concannon et al.14 e Cunha et al.15-17 para estudos de isquemia. A manutenção do pedículo vascular evitou anastomoses microvasculares e uma nova variável para o estudo da isquemia. A manutenção dos nervos evitou a perda de sensibilidade e autofagia do membro. A reposição volêmica foi realizada com 50ml/kg de solução fisiológica de NaCl a 0,9% e também foi utilizada por Lipson et al.8 e Cunha et al.15,16. A perda sangüínea através da medula óssea em fixação intramedular foi relatada como causa de óbito por Ferreira et al.18 em reimplante experimental em ratos. A utilização de cola na síntese óssea evitou a perda sangüínea através da medula óssea e também foi utilizada por Cunha et al.15,16. O clipe vascular microcirúrgico foi utilizado para interromper o fluxo venoso na veia femoral. O clipe vascular microcirúrgico tem sido amplamente utilizado para proporcionar períodos de isquemia arterial ou congestão venosa em modelos de retalhos e membros3,4,14,15.
A mortalidade foi estudada em dois momentos. A mortalidade transoperatória reflete os óbitos secundários às complicações anestésicas e efeitos sistêmicos da congestão venosa. O aumento gradual e significante das mortalidades transoperatórias reflete o aumento dos efeitos deletérios da congestão através de uma curva-tempo de oclusão venosa e mortalidade. O grupo G5 se destacou pela grande diferença estatística do grupo G4. O tempo de 3 horas de oclusão venosa parece ser um tempo crítico para os efeitos sistêmicos da congestão venosa do membro.
A mortalidade pós-operatória reflete os óbitos secundários à reperfusão do membro e infecção maciça. A diferença estatisticamente significante apenas entre os G4 e G5 sugere que os efeitos sistêmicos da reperfusão do membro não são importantes até o tempo de 3 horas (tempo crítico) e se tornam importantes no tempo de 4 horas (G5) em que as lesões se tornam irreversíveis. Nakamura et al.7 estudaram um modelo de oclusão venosa em membros amputados com preservação dos vasos em coelhos. Durante o estudo piloto, testaram períodos de oclusão venosa de 2, 3 e 4h. Observaram taxas de mortalidade de 0% no tempo de 2 horas, 50% no tempo de 3 horas e 100% no tempo de 4 horas. Consideraram o tempo de 4 horas o período de irreversibilidade da lesão tecidual.
A resposta tipo tudo ou nada encontrada tem sido relatada em modelos de reimplantes isquêmicos de membro14. A mortalidade de 100% do G5 excluiu este grupo do estudo da viabilidade. A redução significativa das viabilidades ao longo dos grupos sugere uma curva tempo de oclusão venosa e viabilidade dos membros, tornando o modelo de oclusão venosa confiável.
CONCLUSÕES
O grupo G4 (3 horas de oclusão venosa) pode ser considerado tempo crítico para o modelo estudado. Tempos maiores de oclusão podem levar a altas mortalidades transoperatórias e pós-operatórias. Este grupo poderá ser utilizado para estudo de efeito de medicações e tratamentos para reduzir a lesão tecidual da oclusão venosa.
REFERÊNCIAS BIBLIOGRÁFICAS
1. van Adrichem LNA, Gultuna I, Mulder D. Differences between arterial and venous occlusion in microvascular surgery. Scand J Plast Reconstr Hand Surg. 1993;27:23-7.
2. Gabriel A, Chaney N, Stephenson LL, Zamboni WA. Effect of total venous occlusion on capillary flow and necrosis in skeletal muscle. Plast Reconstr Surg. 2001;108(2):430-3.
3. Kerrigan CL, Wizman P, Hjortdal VE, Sampalis J. Global flap ischemia: a comparison of arterial versus venous etiology. Plast Reconstr Surg. 1994;93(7):1485-97.
4. Hedén P, Sollevi A. Circulatory and metabolic events in pig island skin flaps after arterial or venous occlusion. Plast Reconstr Surg. 1989;84(3):475-83.
5. Su CT, Im MJ, Hoopes JE. Tissue glucose and lactate following vascular occlusion in island skin flaps. Plast Reconstr Surg. 1982;70(2):202-5.
6. Harashima T, Sawada Y, Watanabe S. The relationship between venous occlusion time in island skin flaps and flap survivals. Plast Reconstr Surg. 1977;60:92.
7. Nakamura K, Yokoyama K, Kimura M, Nakamura K, Itoman M. Time course of superoxide generation in reperfusion after arterial ischaemia and venous congestion. Br J Plast Surg. 1998;51(8):633-6.
8. Lipson RA, Kawano H, Halloran PF, McKee NH, Pritzker KP, Langer F. Vascularized limb transplantation in the rat. Results with syngeneic grafts. Transplantation. 1983;35(4):293-9.
9. Lipson RA, Kawano H, Halloran PF, Pritzker KP, Kandel R, Langer F. Vascularized limb transplantation in the rat. Results with allogeneic grafts. Transplantation. 1983;35(4):300-4.
10. Daniel RK, Kerrigan CL. The omnipotential pig buttock flap. Plast Reconstr Surg. 1982;70(1):11-6.
11. Kerrigan CL, Zelt RG, Thomson JG, Diano E. The pig as an experimental animal in plastic surgery research for the study of skin flaps, myocutaneous flaps and fasciocutaneous flaps. Lab Anim Sci. 1986;36(4):408-12.
12. Hjortdal VE, Sinclair T, Kerrigan CL, Solymoss S. Venous ischemia in skin flaps: microcirculatory intravascular thombosis. Plast Reconstr Surg. 1994;93(2):366-74.
13. Hjortdal VE, Hansen ES, Hauge E. Myocutaneous flap ischemia: flow dynamics following venous and arterial obstruction. Plast Reconstr Surg. 1992;89(6):1083-91.
14. Concannon MJ, Dooley TW, Puckett CL. Improved survival in a replantation model containing ischemic muscle. Microsurgery. 1991;12(1):18-22.
15. Cunha MS, Silva JC, Nakamoto HA, Ferreira MC. Study of warm ischemia followed by reperfusion on a lower limb model in rats: effect of allopurinol and streptokinase. Clinics. 2005;60(3):213-20.
16. Cunha MS, Silva JC, Nakamoto H. Effect of allopurinol and hyperbaric oxigen therapy in a limb replantation model after warm ischemia in rats. Rev Col Bras Cir. 2005;32(2):64-8.
17. Cunha MS. Efeito de inibidores da glicoproteína IIb-IIIa em modelo de amputação subtotal de membro submetido a isquemia quente: estudo experimental em ratos [Tese de doutorado]. São Paulo: Universidade de São Paulo, Faculdade de Medicina, 2003.84p.
18. Ferreira MC, Leão PP. Reimplante experimental de membro com microcirurgia vascular. Rev Assoc Med Bras. 1977;23(1):3-6.
I. Assistente Doutor do Serviço de Cirurgia Plástica do Hospital Universitário Prof. Edgard Santos da Faculdade de Medicina da Universidade Federal da BA, Titular da SBCP.
II. Residente da Disciplina de Cirurgia Plástica FMUSP.
III. Membro especialista da SBCP.
IV. Professor Titular da Disciplina de Cirurgia Plástica FMUSP.
Correspondência para:
Marcelo Sacramento Cunha
Rua João das Botas, 89, Apto 601, Canela
Salvador, BA, Brasil - CEP: 40110-160
Tel: 0xx71-3328-4884 - Fax: 0xx71-3328-7781
E-mail: cunha.ms@pop.com.br
Trabalho realizado na Disciplina de Cirurgia Plástica da Faculdade de Medicina da Universidade de São Paulo. Laboratório de Cirurgia Plástica e Microcirurgia da Faculdade de Medicina da Universidade de São Paulo (LIM 04).
Trabalho apresentado no XXXIX Congresso Brasileiro de Cirurgia Plástica 2002 em Salvador - Bahia e Vencedor do Prêmio Sirlei Rinald 2002.
Artigo recebido: 04/07/2005


 Read in Portuguese
Read in Portuguese
 Read in English
Read in English
 PDF PT
PDF PT
 Print
Print
 Send this article by email
Send this article by email
 How to Cite
How to Cite
 Mendeley
Mendeley
 Pocket
Pocket
 Twitter
Twitter